цитолиз при беременности что это
Цитолиз при беременности что это
Физиологические изменения печени во время беременности
Нормально протекающая беременность не сопровождается нарушением функционального состояния печени. Однако при беременности мобилизуются функциональные резервы печени для обезвреживания продуктов жизнедеятельности плода и обеспечения его пластическим материалом. Существенно увеличивается продукция многих гормонов, особенно эстрогенов и прогестерона. Отклонения отдельных показателей от нормы следует рассматривать как выражение повышенной метаболической активности и адаптации организма беременной.
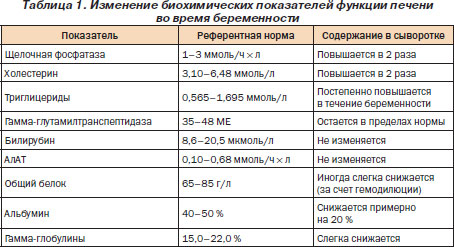
При осмотре женщин с нормальным течением беременности можно обнаружить эритему ладоней и сосудистые звездочки. Печень не пальпируется. Биохимическое исследование сыворотки крови в III триметре беременности выявляет умеренное повышение активности щелочной фосфатазы (а именно ее плацентарной фракции), уровня холестерина, триглицеридов. При этом активность ГГТП остается в пределах нормы. Уровень желчных кислот незначительно повышен. Уровень билирубина и активность аминотрансфераз сохраняются в пределах нормы. Уровни альбумина, мочевины и мочевой кислоты в сыворотке снижаются (табл. 1). Функциональные пробы печени нормализуются спустя 2–6 недель после родов. Гистологическое исследование биоптата печени при нормальной беременности не обнаруживает патологических изменений.
Классификация заболеваний печени у беременных
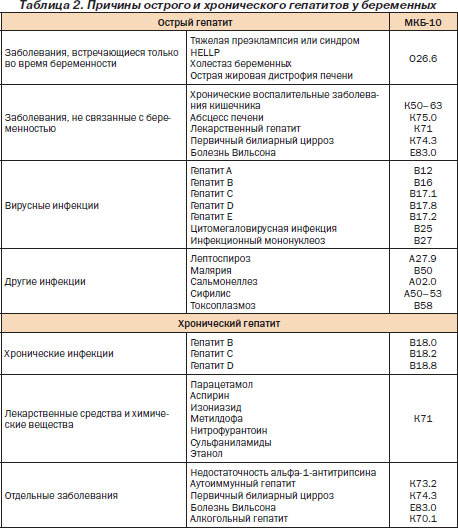
С практической точки зрения целесообразно выделить две группы заболеваний, вызывающих дисфункцию печени у беременных (табл. 2):
1) встречающиеся только во время беременности;
2) встречающиеся и вне беременности.
Наиболее частыми причинами нарушения функции печени у беременных являются вирусные гепатиты (42 %), холестаз беременных (21 %), более редкими причинами являются желчнокаменная болезнь, неукротимая рвота беременных, преэклампсия и HELLP-синдром.
Вирусные гепатиты
Клиническая классификация вирусных гепатитов у беременных (приказ № 676 МЗ Украины, 2004 г.)
Выделяют вирусные гепатиты:
1. Вирусный гепатит А.
2. Вирусный гепатит В.
3. Вирусный гепатит С.
4. Вирусный гепатит Е.
5. Вирусный гепатит D.
6. Вирусный гепатит G.
7. Вирусный гепатит F.
Б. По выраженности клинических проявлений:
1. Бессимптомные формы:
2. Манифестная форма:
В. По цикличности течения:
1. Циклическая форма.
2. Ациклическая форма.
Г. По степени тяжести:
4. Очень тяжелая (фульминантная).
1. Острая и подострая дистрофия печени (острая печеночная энцефалопатия).
2. Функциональные и воспалительные заболевания желчных путей и желчного пузыря.
3. Внепеченочные поражения (индукция иммунокомплексных и аутоиммунных заболеваний).
2. Остаточные признаки патологии (постгепатитная гепатомегалия и гипербилирубинемия, затяжная реконвалесценция — астеновегетативный синдром).
3. Хронический гепатит.
5. Первичный рак печени (гепатоцеллюлярная карцинома).
Классификация острого и хронического гепатита по клинико-биохимическим и гистологическим критериям (приказ № 676 МЗ Украины)
Степень активности (определяется тяжестью воспалительно-некротического процесса):
а) минимальная (увеличение АлАТ не более чем в 3 раза);
б) умеренная (увеличение АлАТ от 3 до 10 раз);
в) выраженная (увеличение АлАТ более чем в 10 раз).
Стадия (определяется распространением фиброза и развитием цирроза печени):
1 — слабо выраженный перипортальный фиброз;
2 — умеренный фиброз с портопортальными септами;
3 — выраженный фиброз с порто-центральными септами;
Примеры формулировки диагноза:
— Острый вирусный гепатит В, высокая степень активности, тяжелое течение.
— Острый вирусный гепатит ни А, ни В, желтушная форма средней тяжести, циклическое течение.
— Хронический вирусный гепатит С (anti-HCV+, HCV-PHK+, 3a-генотип), умеренной степени активности, с выраженным фиброзом (стадия).
— Хронический вирусный гепатит В, НВeАg-позитивный (HBsAg+, HBV ДНК+), выраженной степени активности.
Диагностика гепатитов при беременности
Анамнез (вирусный гепатит В, или С, или D; профессиональные, химические вредные факторы; медикаментозные интоксикации; злоупотребление алкоголем; подпеченочный холестаз; метаболические нарушения и др.).
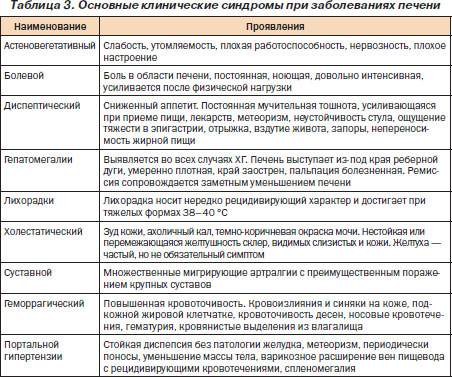
Клинические синдромы патологии печени показаны в табл. 3.
Лабораторные показатели
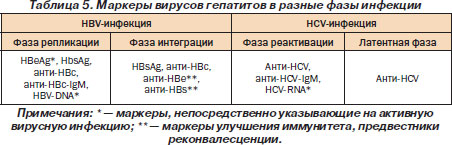
Маркеры вирусных гепатитов (табл. 4):
1) гепатит А — анти-HAV IgM — даже однократное выявление является абсолютным доказательством заболевания (появляется в крови за 4–5 дней до выявления симптомов заболевания и исчезает через 6–8 мес.);
— HBsAg (основной маркер инфицирования НВ-вирусом, выявляется с 3–5-й недели заболевания, в течение 70–80 дней);
— HBeAg (маркер эпидемиологического риска, активной репликации вируса и трансмиссии от матери к плоду; риск заражения плода повышается до 90 %);
— HBcAg (в крови не определяется, но могут быть антитела к нему — анти-HBcIgM и HBcIgG, свидетельствующие об этиологии острого вирусного гепатита В (ОВГВ) и перспективе вирусоносительства, HBcorAg, HBxAg, анти-HBc IgМ;
3) гепатит С — анти-HСV IgM (диагностическое значение при хроническом гепатите);
— HBsAg (маркер активной репликации вируса при остром гепатите);
— анти-HDV IgM (появляется на 10–15-й день заболевания и сохраняется 2,5–3 мес.);
5) гепатит Е — анти-HЕV IgM.
Методом ПЦР (по возможности):
— гепатит А — РНК HAV;
— гепатит В — ДНК HВV;
— гепатит С — РНК HСV;
— гепатит D — РНК HDV;
— гепатит Е — РНК HЕV.
В течении HBV-инфекции выделяют фазу репликации и интеграции (табл. 5).
HCV-инфекция характеризуется чередованием латентной фазы и фазы реактивации.
Исчезновение HВeAg и выявление анти-НBе называется сероконверсией, свидетельствует о включении (интеграции) вирусной ДНК в геном гепатоцита, сопровождается обострением болезни.
Наличие HbsAg в сочетании с анти-НВе класса IgG и/или с анти-НВс характеризует фазу интеграции вируса гепатита В в геном гепатоцита.
Сыворотка крови больных HDV содержит маркеры дельта-антигена (IgE и IgМ-анти-D, а также маркеры В инфекции).
Сывороточной пробы для диагностики ВГG пока не существует.
Биохимические показатели вирусных гепатитов:
— тимоловая проба > 4 МЕ (не изменяется при ОВГВ);
— повышение АлАТ, в меньшей степени АсАТ;
— билирубин > 22 мкмоль/л, преимущественно за счет прямого;
— лейкопения (возможно, лейкоцитоз), лимфопения, снижение СОЭ, тромбоцитопения;
Лекарственный гепатит у беременных. Еремина Е.Ю.
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Уважаемые коллеги! Вы видите, что к нам присоединилась Еремина Елена Юрьевна. Здравствуйте! Спасибо, что вы тоже с нами. И сегодня профессор Еремина познакомит нас с лекарственным гепатитом у беременных.
Елена Юрьевна Еремина, профессор, доктор медицинских наук:
– Добрый день, уважаемая Оксана Михайловна! Добрый день, уважаемые коллеги! Тема моего доклада «Лекарственный гепатит у беременных» пока еще не часто встречается в образовательных проектах, но тем не менее уже стала весьма актуальна для практического здравоохранения. Многообразие причин роста распространенности лекарственных поражений печени в популяции не обошло стороной и такую специфическую категорию пациентов, как беременные женщины.
Развитию лекарственных поражений печени у беременных способствуют многие факторы. Это проведение любой, особенно длительной и поликомпонентной терапии во время беременности или даже до ее наступления, в том числе в связи с длительно не наступающей беременностью или процедурой экстракорпорального оплодотворения.
Это нередко встречающаяся патология беременности, исходно существующая у женщины патология печени, ряд вредных привычек в анамнезе, а также физиологические изменения в организме беременной женщины, которые в результирующей степени сопровождаются повышением функциональной нагрузки на печень; гипоальбуминемия вследствие увеличения объема циркулирующей крови и развития внепеченочного холестаза, который может быть функционально обусловленным беременностью или же быть билиарно опосредованным, в том числе с манифестацией во время беременности.
Внепеченочный холестаз в свою очередь способствует накоплению лекарственных средств и их метаболитов в организме женщины. Наблюдаемые в период беременности гормональные сдвиги способствуют нарушению сократимости желчного пузыря, застою желчи и повышению ее литогенности. Все это создает предпосылки для клинической манифестации гепатобилиарной патологии и ассоциированных с ней состояний.
Распространенность лекарственного гепатита у беременных растет год от года. На данном слайде представлены данные по городу Саранску, Республика Мордовия, в котором проживает чуть более 300 тысяч населения. И это только зарегистрированные случаи. Если вы обратили внимание, то за 2010-2011 год были зарегистрированы 22 случая лекарственного гепатита у беременных, а уже за 2012 год зарегистрировано 23 случая лекарственного гепатита у беременных. И я знаю, что аналогичная картина наблюдается и во многих других регионах страны.
Большинство регистрируемых случаев лекарственных поражений печени у беременных, по нашим данным, ассоциировалось с приемом множества лекарственных препаратов, среди которых превалировали поливитаминно-минеральные комплексы, гормональные эстрогенсодержащие и прогестеронсодержащие препараты, а также препараты железа и кальция.
На сегодняшний день описано четыре основных механизма лекарственных поражений печени. Очевидно, что у беременных имеются и дополнительные, пока досконально не изученные механизмы. Сейчас на базе Мордовского перинатального центра и Института охраны материнства и младенчества города Екатеринбурга активно проводятся научные исследования, посвященные данной проблеме.
Различие механизмов лекарственных поражений печени обусловливает многообразие клинических форм, среди которых у беременных преобладает лекарственный гепатит. Наиболее часто он представлен острым гепатитом с изолированным повышением уровня сывороточных трансаминаз, холестатическим лекарственным гепатитом и несколько реже псевдохирургической формой острого гепатита.
Течение лекарственного гепатита у беременных отличается асимптомностью симптоматики или ее малосимптомностью с манифестацией на стадии уже выраженных нарушений функций печени. Характерно превалирование смешанного – цитолитического и холестатического – синдрома с тенденцией к прогрессированию цитолиза (особенно быстрому в III триместре). Это способствует высокой вероятности развития осложнений беременности, среди который наиболее частыми являются коагулопатия, гестоз, острая жировая печень беременных, HELLP-синдром, синдром Бадда-Киари. И не случайно появились работы литовских авторов о том, что каждый пятый случай острой жировой печени беременных ассоциируется именно с приемом лекарственных препаратов.
К особенностям лекарственного гепатита относится сложная дифференциальная диагностика заболевания вследствие его частой коморбидности, необходимости выполнения множества исследований в короткий срок при ограниченных возможностях диагностики во время беременности. Кроме того, необходимо проводить динамический, а при высокой активности процесса – ежедневный многокомпонентный мониторинг показателей функций печени, показателей функций почек и гемостаза.
Тактика ведения беременных с лекарственным гепатитом требует высокой врачебной ответственности при принятии решения о пролонгировании беременности или же о ее прерывании, о возможности кормления ребенка грудью, определения вида родоразрешения, анестезиологического пособия и ведении пациентки в послеродовом периоде.
Диагностика лекарственного гепатита у беременных соответствует традиционному алгоритму при заболеваниях печени, включающему в себя биохимические маркеры цитолиза и холестаза, функциональной состоятельности печени, показатели функции почек и гемостаза, проведение ультразвукового исследования с центральным допплеровским сканированием сосудов органов брюшной полости для исключения веноокклюзионной болезни или синдрома Бадда-Киари, а также скрининговых методов диагностики вирусных, аутоиммунных заболеваний печени и по показаниям наследственных гепатозов.
Лечение лекарственного гепатита у беременных представляет собой сложный, тернистый путь между Сциллой и Харибдой. И основными требованиями к терапии лекарственного гепатита является прежде всего безопасность используемых лекарственных средств для беременной и плода, отсутствие противопоказаний для применения лекарственных средств в период беременности. Или, если этот препарат необходим для приема, то подписание информированного согласия пациентки. Необходимым требованием является минимизация медикаментозной терапии, в том числе допустим «период ожидания», когда эта терапия может оказаться эффективной. Должны использоваться лекарственные средства, имеющие серьезную доказательную базу и, конечно, желателен собственный клинический опыт доктора.
К базовым препаратам, используемым при лекарственных гепатитах у беременных, относится Урсодеоксихолевая кислота, и при высокой активности цитолиза – Глюкокортикостероиды.
В своей клинической практике в качестве препарата Урсодеоксихолевой кислоты мы используем Урсосан, поскольку длительное время он был единственным из этой категории препаратов, строго не противопоказанных во время беременности. Накоплен достаточно большой опыт его применения при различных патологиях печени, в том числе у беременных. Основным его преимуществом является возможность безопасного применения при всех формах лекарственного поражения печени, особенно при наличии холестаза, когда значительная часть других препаратов с гепатопротективными свойствами является противопоказанной. Препарат способствует экскреции гепатотоксических метаболитов лекарств, улучшает функционирование печени, снижает транспорт токсичных желчных кислот к плоду и уменьшает риск его токсичного поражения.
Согласно инструкции, Урсодеоксихолевая кислота может применяться во втором и третьем триместре беременности. Однако при наличии показаний она может быть использована и в первом триместре, но, конечно, при подписании информированного согласия пациентки.
Тактика ведения беременной с лекарственным гепатитом в значительной степени определяется активностью процесса и сроком беременности. При этом учитывается, что наиболее тяжелое течение заболевания отмечается при его развитии в третьем триместре беременности. В первом триместре прогноз, как правило, менее серьезен. И при условии динамического наблюдения за пациенткой и ответа на проводимое лечение допустимо пролонгирование беременности. Следует учитывать, что холестатический вариант лекарственного гепатита разрешается значительно медленнее, и чаще вызывает коагулопатию. И наконец, наиболее неблагоприятный прогноз ассоциирован с выраженным цитолизом, гипербилирубинемией и желтухой.
В первом триместре при бессимптомном повышении активности трансаминаз в пределах трех норм и отсутствии противопоказаний допустимо использование растительных гепатопротекторов в стандартных терапевтических дозах при отмене другой медикаментозной терапии. Это желательное условие. Лечение может проводиться амбулаторно при еженедельном или даже более частом биохимическом мониторинге. При более высокой активности цитолиза и наличии холестаза требуется госпитализация пациентки и назначение препарата урсодеоксихолевой кислоты. Кроме того, в ряде случаев приходится решать вопрос об использовании глюкокортикостероидов или даже о прерывании беременности.
Тактика лечения беременной во втором триместре при наличии у нее лекарственного гепатита также определяется уровнем цитолитических процессов. При уровне сывороточных трансаминаз в пределах 10 норм назначается Урсосан в дозе 12-13 миллиграмм/килограмм/сутки в 2-3 приема. При более высокой активности сывороточных трансаминаз доза Урсосана составляет 13 миллиграмм/килограмм/сутки, и она, как правило, дополняется пероральным приемом Преднизолона в дозе до 20 миллиграмм/сутки.
При отсутствии положительной динамики, при этом ожидание составляет обычно до 10 дней, если выраженный цитолиз – необходимо прерывать беременность.
Наиболее активная тактика лечения в третьем триместре. При уровне сывороточных трансаминаз в пределах 5 норм назначается Урсосан в дозе 13 миллиграмм/килограмм/сутки. Уровень сывороточных трансаминаз в пределах от 5 до 10 норм требует добавления Преднизолона в дозе до 30 миллиграмм/сутки пероз или внутривенно 60-90 миллиграмм/сутки.
При прогрессирующем росте сывороточных трансаминаз свыше 10 норм на фоне продолжающейся терапии срок ожидания составляет обычно не более 5 дней – в этом случае требуется досрочное родоразрешение в связи с высоким риском развития осложнений беременности.
В послеродовом периоде наблюдение за пациенткой должно быть продолжено, поскольку последствия перенесенного лекарственного гепатита во время беременности пока еще недостаточно изучены. Следует учитывать, что после родов, как правило, отмечается кратковременное прогрессирование цитолиза, поэтому терапия должна продолжаться после родоразрешения до нормализации печеночных проб.
Мы в своей практике используем активную передачу пациентки в поликлинику по месту жительства для продолжения ее лечения и динамического наблюдения. Поскольку исходом лекарственного гепатита у беременной может быть формирование хронического лекарственного гепатита, аутоиммунного заболевания печени или другой гепатобилиарной патологии.
И в заключение хотелось бы еще раз подчеркнуть, что любые лекарственные средства, растительные препараты у беременной могут вызвать лекарственный гепатит. Поэтому все лекарственные средства, все растительные препараты, биологически активные добавки должны назначаться беременным только по строгим клиническим показаниям!
При этом следует избегать полипрагмазии и корректировать дозы применяемых лекарственных средств, исходя из состояния печени. Надо учитывать генетическую предрасположенность, анамнез и факторы риска развития лекарственных поражений печени у пациентки. При отклонениях печеночных показателей от нормы необходим тщательный мониторинг медикаментозной терапии с ежемесячным или более частым определением уровня сывороточных трансаминаз, щелочной фосфатазы, гамма-глутамилтранспептидазы и билирубина. И в ряде случаев, во втором, третьем триместре, при необходимости продолжения лекарственных препаратов целесообразно использование препарата Урсодеоксихолевой кислоты с целью профилактики прогрессирования печеночной патологии.
Цитолитический синдром
Цитолитический синдром – это комплекс симптомов, который развивается в ответ на разрушение гепатоцитов (клеток печени). При повреждении гепатоцитов их внутриклеточное содержимое поступает в кровеносное русло.
Цитолитический синдром может развиться по ряду причин:
Симптомы цитолитического синдрома
Проявления цитолитического синдрома могут широко варьироваться. Это зависит от причин, по которым происходит разрушение гепатоцитов. Синдрому могут сопутствовать следующие проявления:
Проявления цитолитического синдрома не ограничиваются перечисленными симптомами и могут наблюдаться в разных комбинациях. Поэтому даже один из таких признаков – повод обратиться к врачу и пройти комплексное обследование.
С учетом того, что цитолитический синдром не самостоятельное заболевание, а проявление какой-либо существующей патологии, необходимо устранение его причин (основного заболевания) и последствий. С этой целью в лечении, кроме гепатолога, могут принимать участие врачи разных специальностей (эндокринолог, кардиолог и пр.). Пациенту назначаются различные медикаментозные препараты, в числе которых может быть Фосфоглив*.
Фосфоглив* —
1. Настоящая информация основана на исследованиях, проводимых ООО «Ипсос Комкон», и действительна по состоянию на декабрь 2016 года
2. Распоряжение правительства РФ от 28 декабря 2016 г. № 2885-р «Об утверждении перечней жизненно необходимых и важнейших лекарственных препаратов для медицинского применения на 2017 год»
3. Ивашкин В.Т., Бакулин И.Г., Богомолов П.О., Мациевич М.В. и др., 2017 г.
4. Бакулин И.Г., Бохан Н.А., Богомолов П.О., Гейвандова Н.И. и др., 2017 г.
5. Буеверов А.О., 2014 г.
6. Филимонкова Н.Н., Воробьева Ю.В., Топычканова Е.П., 2013 г.
7. Новикова Т.И., Новиков В.С., 2011 г.
8. Приказ МЗ РФ от 10.11.2011 г. № 1340н «Об утверждении Перечня лекарственных средств, отпускаемых по рецептам врача (фельдшера) при оказании дополнительной бесплатной медицинской помощи отдельным категориям граждан, имеющим право на получение государственной социальной помощи»
9. Приказ Минздрава РФ от 09.11.2012 N 772н «Об утверждении стандарта специализированной медицинской помощи при других заболеваниях печени»
10. Инструкция по медицинскому применению
11. И.Г. Никитин, И.Е. Байкова, В.М. Волынкина и соавторы, 2009г.
Интерпретация биохимического анализа крови при патологии печени. Синдром цитолиза. Часть 1.
Опубликовано в журнале:
«Практика педиатра» июнь, 2017г.
М. Г. Ипатова 1, 2 к.м.н., Ю. Г. Мухина 1 д.м.н. профессор, П. В. Шумилов 1 д.м.н., профессор
1 Российский национальный исследовательский медицинский университет им. Н. И. Пирогова
МЗ РФ, Москва
2 Детская Городская Клиническая Больница № 13 им. Н. Ф. Филатова, Москва
Ключевые слова: печень, синдром цитолиза, аланинаминотрансфераза, аспартатамино—трансфераза, гепатопротективные препараты
В статье изложены биохимические лабораторные показатели и их клиническое значение при заболеваниях печени, протекающих с синдромом цитолиза. Отдельное внимание уделено механизмам действия гепатопротективных препаратов, применяемых при цитолитическом синдроме.
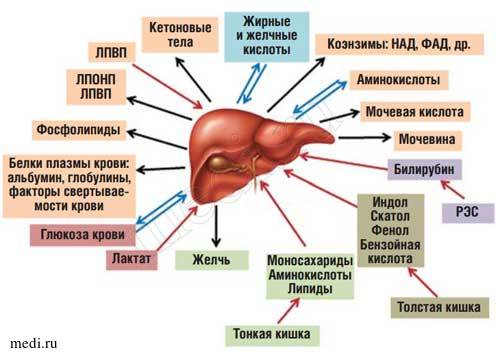
Рис. 1. Роль печени в обмене веществ.
Печень представляет собой центральный орган химического гомеостаза организма, где создается единый обменный и энергетический пул для метаболизма почти всех классов веществ [1]. К основным функциям печени относятся: метаболическая, депонирующая, барьерная, экскреторная, гомеостатическая и детоксицирующая [2]. Печень может обезвреживать как чужеродные экзогенные вещества, обладающие токсическими свойствами, так и синтезированные эндогенно.
Таблица 2. Причины повышения уровня аминотрансфераз
Печеночные причины
Внепеченочные причины
•Вирусные гепатиты (В, С, ЦМВ и др.)
•Хронические инфекции и паразитарные
заболевания (эхинококкоз, токсоплазмоз и др.)
•Неалкогольный стеатогепатит
•Аутоиммунные заболевания печени
•Злоупотребление алкоголем
•Прием лекарственных препаратов
(статины, некоторые антибиотики, противогрибковые препараты, нестероидные
противовоспалительные препараты,
глюкокортикостероиды, другие)
•Метаболические заболевания печени
(галактоземия, фруктоземия, гликогенозы,
дефицит альфа1-антитрипсина,
аминоацидопатии, нарушение цикла мочевины, нарушение окисления жирных кислот, митохондриальная гепатопатия, некоторые лизосомные заболевания (болезнь
Гоше, болезнь Ниманна-Пика, дефицит кислой липазы и др.), муковисцидоз, синдром Швахмана-Даймонда, гемохроматоз, болезнь Вильсона и др.)
•врожденные и приобретенные дефекты
сосудов системы воротной вены (болезнь
Бадда-Киари и др.)
•Цирроз печени
•Опухоли печени
•Патология сердца (острый инфаркт
миокарда, миокардит)
•Повышенная физическая нагрузка
•Наследственные нарушения мышечного
метаболизма
•Приобретенные мышечные заболевания
•Травма и некроз мышц
•Целиакия
•Гипертиреоз
•Тяжелые ожоги
•Гемолиз эритроцитов
•Нарушение кислотно-щелочного равновесия
•Сепсис
Находясь между портальным и большим кругами кровообращения, печень выполняет функцию большого биофильтра. Через воротную вену в нее поступает более 70% крови, остальная кровь попадает через печеночную артерию. Большая часть веществ, всасывающихся в пищеварительном тракте (кроме липидов, транспорт которых в основном осуществляется через лимфатическую систему), поступает по воротной вене в печень [2]. Таким образом, печень функционирует как первичный регулятор содержания в крови веществ, поступающих в организм с пищей (рис 1).
Большое разнообразие функций гепатоцитов приводит к тому, что при патологических состояниях печени нарушаются биохимические константы, отражающие изменения многих видов обмена. Поэтому стандартный биохимический анализ крови включает определение различных параметров, отражающих состояние белкового, углеводного, липидного и минерального обмена, а также активность некоторых ключевых ферментов.
Концентрация ферментов в клетках значительно выше, чем в плазме крови; в норме только очень незначительная часть определяется в крови. Наиболее частыми причинами повышения уровня ферментов в сыворотке крови являются: прямое поражение клеточных мембран, в частности вирусами и химическими соединениями, гипоксия и ишемия тканей. Иногда активность ферментов увеличивается в результате их повышенного синтеза в тканях. Определение активности тех или других ферментов в сыворотке крови позволяет судить о характере и глубине поражения различных компонентов гепатоцитов [3, 4].
Ферменты в зависимости от их локализации можно разделить на несколько групп:
1) универсально распространенные ферменты, активность которых обнаруживается не только в печени, но и в других органах – амино-трансферазы, фруктозо-1-6-дифосфатальдолаза;
2) печеночноспецифические (органоспе-цифические) ферменты; их активность исключительно или наиболее высоко выявляется в печени. К ним относятся холинэстераза, орнитин-карбамилтрансфераза, сорбитдегидрогеназа и др.;
3) клеточноспецифические ферменты печени относят преимущественно к гепатоцитам,
купферовским клеткам или желчным канальцам (5-нуклеотидаза, аденозинтрифосфатаза);
4) органеллоспецифические ферменты, являются маркерами определенных органелл
гепатоцита: митохондриальные (глутаматде-гидрогеназа, сукцинатдегидрогеназа, цитохромоксидаза), лизосомальные (кислая фос фатаза, дезоксирибонуклеаза, рибонуклеаза), микросомальные (глюкозо-6-фосфатаза).
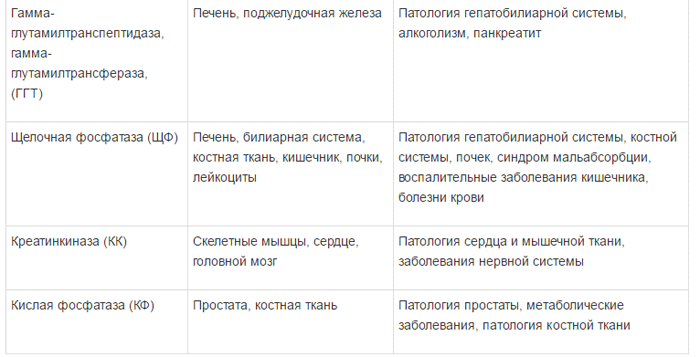
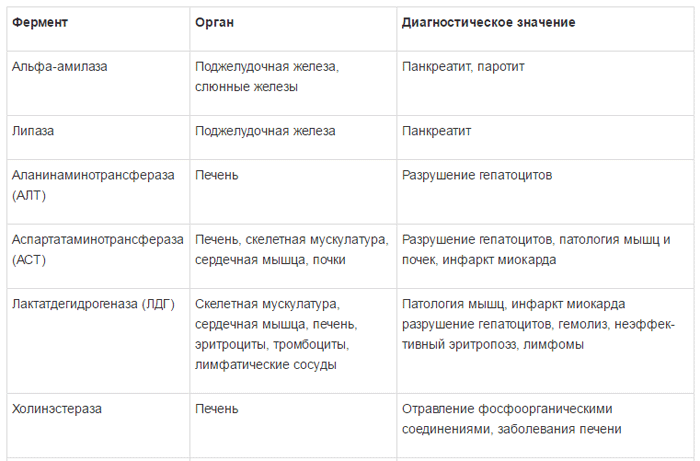
Специфичность ферментов и их диагностическое значение представлено в таблице 1 [5].
Исходя из выше изложенного, следует, что в большинстве случаев отклонения активности сывороточных ферментов от «нормы» неспецифичны и могут быть вызваны различными причинами. Поэтому нужно с большой осторожностью относиться к интерпретации этих отклонений, сопоставляя их с клинической картиной заболевания и данными других лабораторных и инструментальных методов исследования [5, 6].
В связи с использованием в клинических лабораториях разных методов исследования ферментов и единиц измерения их активности целесообразно каждый раз, получив результаты анализа, уточнить, каким методом и в каких единицах была измерена активность фермента, и сопоставить полученное значение с «нормой», принятой в данной лаборатории.
Отдельное место занимает макроэнзиме-мия – редкое и крайне сложное для дифференциальной диагностики состояние, при котором происходит комплексирование молекул того или иного энзима с иммуноглобулинами или небелковыми веществами. Описаны клинические наблюдения макро-КФК-емии, макро-ЛДГ-емии, макро-АСТ-емии, макро-ГГТ-емии, макроамилаземии. Макро-энзимемии сложны для диагностики и дифференциальной диагностики и ведут к проведению инвазивных методов обследования и необоснованному лечению.
В основе выявления макроэнзимемии лежит выявление отличий молекулы макрофермента от молекулы обычного энзима. Некоторые из этих методов являются прямыми, т. е. такими, которые позволяют непосредственно определить присутствие в крови ферментного комплекса, имеющего гораздо более высокий молекулярный вес, чем молекула нормального фермента. В основу прямого метода положено разделение белков сыворотки по молекулярному весу. Другие же методы являются непрямыми, так как выявление макроэнзима в крови проводится не путем выявления самого ферментного комплекса, а основываются на выявлении какого-либо из свойств макроэнзима. Прямые тесты имеют большее диагностическое значение и влекут за собой меньше технических и диагностических ошибок.
В некоторых ситуациях повышение ферментов является физиологическим: уровень щелочной фосфатазы повышен у подростков в период вытяжения (период ускорения роста), у здоровых женщин во время третьего триместра беременности (за счет плаценты). Однако очень высокую активность щелочной фосфатазы наблюдают у женщин с преэк-лампсией, что связно с нарушением кровообращения плаценты [7].
Большое значение в диагностике заболеваний печени имеют анамнестические данные и клиническая картина заболевания. Из анамнеза следует попытаться узнать о факторах риска заболеваний печени, обращая особое внимание на семейный анамнез, прием лекарств, витаминов, растительных добавок, наркотиков, алкоголя, трансфузии препаратов крови, патологические результаты печеночных проб в прошлом и симптоматику заболеваний печени. Клиническое обследование позволяет диагностировать до 50–60% патологических состояний. Более детальная дифференциальная диагностика основана на иммунохимических методах. Они позволяют детализировать характер вирусной, а также паразитарной инфекции, определить локализацию неопластического процесса, определить этиологию аутоиммунного заболевания, уточнить вид нарушения наследственных заболеваний обмена веществ.
При патологии печени в биохимическом анализе крови выделяют 4 синдрома:
• Синдром печеночно-клеточной недостаточности
• Мезенхиально-воспалительный синдром.
В данной статье мы подробно разберем по
казатели, характерные для синдрома цитолиза.
Синдром цитолиза – это синдром, обусловленный нарушением проницаемости клеточных мембран, распадом мембранных структур или некрозом гепатоцитов с выходом в плазму ферментов (АЛТ, АСТ, ЛДГ, альдолазы и др.).
АМИНОТРАНСФЕРАЗЫ: аспартатаминотрансфераза и аланинаминотрансфераза
Референтные значения: у новорожденных детей до 1 мес. – менее 80 Ед/л; от 2 мес. до 12 мес. – менее 70 Ед/л., с 1 года до 14 лет – менее 45 Ед/л, у женщин – менее 35 Ед/л, у мужчин – менее 50 Ед/л.
В клинической практике широко применяется одновременное определение уровня двух трансаминаз – аспартатаминотрансферазы (AСT) и аланинаминотрансферазы (АЛТ) в сыворотке крови.
Ферменты АЛТ и АСТ содержатся практически во всех клетках человеческого организма. Однако самый высокий уровень фермента АЛТ содержится в печени, поэтому уровень данного энзима служит специфическим маркером поражения печени. В свою очередь, АСТ помимо печени (в порядке снижения концентрации) содержится в сердечной и скелетных мышцах, почках, поджелудочной железе, легких, лейкоцитах и эритроцитах [6, 7, 8].
В печени АЛТ присутствует только в цитоплазме гепатоцитов, а АСТ – в цитоплазме и в митохондриях. Более 80% печеночной АСТ представлено именно митохондриальной фракцией [6, 7, 8].
В норме постоянство концентрации транс-аминаз в плазме крови отражает равновесие между их высвобождением вследствие физиологического апоптоза состарившихся гепатоци-тов и элиминацией. Соотношение синтеза АСТ/ АЛТ в печени равно 2,5/1. Однако при нормальном обновлении гепатоцитов уровни АСТ и АЛТ в плазме крови практически одинаковы (30–40 Ед/л) из-за более короткого периода полувыведения АСТ (18 ч против 36 ч у АЛТ).
При заболеваниях печени в первую очередь и наиболее значительно повышается активность АЛТ по сравнению с АСТ. Например, при остром гепатите, независимо от его этиологии, активность аминотрансфераз повышается у всех больных, однако преобладает уровень АЛТ, содержащейся в цитоплазме, вследствие ее быстрого выхода из клетки и поступления в кровяное русло. Таким образом, по уровню АЛТ судят о биохимической активности заболевания печени. Повышение показателя в 1,5–5 раз от верхней границы нормы свидетельствует о низкой активности процесса, в 6–10 раз – об умеренной и более 10 раз – о высокой биохимической активности. Повышение активности трансаминаз более 6 месяцев является биохимическим признаком хронического гепатита [6, 7].
Некоторые лекарственные препараты (например, вальпроевая кислота) метаболизируются в митохондриях гепатоцитов [9], поэтому ранним лабораторным маркером гепатотоксичности может быть лишь изолированное повышение АСТ.
Помимо патологии печени АСТ служит одним из ранних маркеров повреждения сердечной мышцы (повышается у 93–98% больных инфарктом миокарда до 2–20 норм); специфичность его не высока. Уровень ACT в сыворотке крови возрастает через 6–8 часов после начала болевого приступа, пик приходится на 18–24 часа, активность снижается до нормальных значений на 4–5 день. Нарастание активности фермента в динамике может свидетельствовать о расширении очага некроза, вовлечении в патологический процесс других органов и тканей, например, печени [7].
Интенсивные мышечные упражнения с чрезмерной нагрузкой также могут вызвать преходящее увеличение уровня ACT в сыворотке крови. Миопатии, дерматомиозиты и другие заболевания мышечной ткани вызывают повышение трансаминаз, преимущественно за счет АСТ.
Умеренное увеличение активности АСТ (в 2–5 раз от верхней границы нормы) отмечается при острых панкреатитах и гемолитических анемиях.
При латентных формах цирроза печени повышения активности ферментов, как правило, не наблюдают. При активных формах цирроза стойкий незначительный подъем аминотрансфераз выявляют в 74–77% случаев, и, как правило, преобладает активность АСТ над АЛТ в два и более раз.
Снижение активности АЛТ и АСТ имеет место при недостаточности пиридоксина (витамина В6), при почечной недостаточности, беременности.
Ниже приведены печеночные и внепеченочные причины повышения активности аминотрансфераз в сыворотке крови (табл. 2).
Помимо оценки уровня трансаминаз в клинической практике широко применяется коэффициент де Ритиса – отношение АСТ к АЛТ (АСТ/АЛТ). В норме значение этого кэффициента составляет 0,8–1,33. Следует отметить, что расчет коэффициента де Ритиса целесообразен только при выходе АСТ и/или АЛТ за пределы референтных значений.
У новорожденных детей соотношение АСТ/АЛТ обычно превышает 3,0, однако к пятому дню жизни снижается до 2,0 и ниже.
При поражениях печени с разрушением гепатоцитов преимущественно повышается АЛТ, коэффициент де Ритиса снижается до 0,2–0,5. При патологии сердца преобладает уровень АСТ, и коэффициент де Ритиса повышается. Однако для точной дифференциальной диагностики этот коэффициент непригоден, так как нередко при алкогольном поражении печени, неалкогольном стеатогепатите, циррозе печени также преобладает повышение АСТ и коэффициент де Ритиса составляет 2,0–4,0 и более. Значение данного коэффициента выше нормы часто наблюдается при обтурационных желтухах, холециститах, когда абсолютные значения АЛТ и АСТ невелики.
1. При остром вирусном и хроническом гепатитах, особенно на ранних стадиях, активность АЛТ выше, чем АСТ (коэффициент де Ритиса меньше 1,0). Тяжелое поражение паренхимы печени может изменить это соотношение.
2. При алкогольном гепатите и циррозе нередко активность АСТ оказывается выше, чем АЛТ (коэффициент де Ритиса больше 1,0).
3. При остром ИМ активность АСТ выше, чем АЛТ (коэффициент де Ритиса больше 1,5).
ЛАКТАТДЕГИДРОГЕНАЗА
Референтные значения ЛДГ для новорожденных – до 600 Ед/л, у детей с 1 года до 12 лет активность ЛДГ – 115 – 300 Ед/л, для детей старше 12 лет и у взрослых норма ЛДГ – до 230 Ед/л.
Лактатдегидрогеназа (ЛДГ) – гликолитический цинксодержащий фермент, обратимо катализирующий окисление L-лактата в пируват, широко распространен в организме человека. Наибольшая активность ЛДГ обнаружена в почках, сердечной мышце, скелетной мускулатуре и печени. ЛДГ содержится не только в сыворотке, но и в значительном количестве в эритроцитах, поэтому сыворотка для исследования должна быть без следов гемолиза [7].
При электрофорезе или хроматографии удается обнаружить 5 изоферментов ЛДГ, отличающихся по своим физико-химическим свойствам. Наибольшее значение имеют два изофермента – ЛДГ1 и ЛДГ5. Фракция ЛДГ1 более активно катализирует обратную реакцию превращения лактата в пируват. Она в большей степени локализуется в сердечной мышце и некоторых других тканях, в норме функционирующих в аэробных условиях. В связи с этим миокардиальные клетки, обладающие богатой митохондриальной системой, окисляют в цикле трикарбоновых кислот не только пируват, образующийся в результате протекающего в них самих процесса гликолиза, но и лактат, образующийся в других тканях. Фракция ЛДГ5 более эффективно катализирует прямую реакцию восстановления пирувата в лактат. Она локализуется преимущественно в печени, в скелетных мышцах. Последние нередко вынуждены функционировать в анаэробных условиях (при значительной физической нагрузке и быстро наступающем утомлении). Образующийся при этом лактат с кровотоком попадает в печень, в которой он используется для процесса глюконеогенеза (ресинтеза глюкозы), а также в сердце и другие ткани, где происходит его преобразование в пируват и вовлечение в цикл трикарбоновых кислот (цикл Кребса). Любое повреждение клеток тканей, содержащих большое количество ЛДГ (сердце, скелетные мышцы, печень, эритроциты), приводит к повышению активности ЛДГ и ее изо-ферментов в сыворотке крови. Наиболее частыми причинами повышения активности ЛДГ являются:
1. Поражение сердца (острый инфаркт миокарда, миокардит, застойная сердечная недостаточность); в этих случаях обычно преобладает повышение активности ЛДГ1 и/или ЛДГ2.
2. Поражение печени (острые и хронические гепатиты, цирроз печени, опухоли и метастазы печени), когда преимущественно увеличивается изофермент ЛДГ5, ЛДГ2, ЛДГ4.
3. Повреждение скелетных мышц, воспалительные и дегенеративные заболевания
скелетных мышц (преимущественно увеличение изофермента ЛДГ1, ЛДГ2, ЛДГ3).
4. Заболевания крови, сопровождающиеся распадом клеток крови: острый лейкоз, гемолитическая анемия, В12-дефицитная анемия, серповидноклеточная анемия, а также заболевания и патологические состояния, сопровождающиеся разрушением тромбоцитов (массивная гемотрансфузия, эмболия легочной артерии, шок и др.). В этих случаях может преобладать повышение активности ЛДГ2, ЛДГ3.
5. Острый панкреатит.
6. Заболевания легких (пневмония и др.)
8. Опухоли (повышенный уровень ЛДГ наблюдается в 27% случаев опухолей в I стадии и в 55% – метастатических семином).
Следует помнить, что многие заболевания сердца, скелетных мышц, печени и крови могут сопровождаться повышением активности в сыворотке крови общей ЛДГ без отчетливого преобладания какого-либо из ее изоферментов.
Таблица 3. Эффективность гепатопротекторов при синдроме цитолиза (по С. В. Морозову с соавт., 2011 г. и Н. Б. Губергриц, 2012 г.) [10]