цитолиз печени что это такое
Цитолитический синдром
Цитолитический синдром – это комплекс симптомов, который развивается в ответ на разрушение гепатоцитов (клеток печени). При повреждении гепатоцитов их внутриклеточное содержимое поступает в кровеносное русло.
Цитолитический синдром может развиться по ряду причин:
Симптомы цитолитического синдрома
Проявления цитолитического синдрома могут широко варьироваться. Это зависит от причин, по которым происходит разрушение гепатоцитов. Синдрому могут сопутствовать следующие проявления:
Проявления цитолитического синдрома не ограничиваются перечисленными симптомами и могут наблюдаться в разных комбинациях. Поэтому даже один из таких признаков – повод обратиться к врачу и пройти комплексное обследование.
С учетом того, что цитолитический синдром не самостоятельное заболевание, а проявление какой-либо существующей патологии, необходимо устранение его причин (основного заболевания) и последствий. С этой целью в лечении, кроме гепатолога, могут принимать участие врачи разных специальностей (эндокринолог, кардиолог и пр.). Пациенту назначаются различные медикаментозные препараты, в числе которых может быть Фосфоглив*.
Фосфоглив* —
1. Настоящая информация основана на исследованиях, проводимых ООО «Ипсос Комкон», и действительна по состоянию на декабрь 2016 года
2. Распоряжение правительства РФ от 28 декабря 2016 г. № 2885-р «Об утверждении перечней жизненно необходимых и важнейших лекарственных препаратов для медицинского применения на 2017 год»
3. Ивашкин В.Т., Бакулин И.Г., Богомолов П.О., Мациевич М.В. и др., 2017 г.
4. Бакулин И.Г., Бохан Н.А., Богомолов П.О., Гейвандова Н.И. и др., 2017 г.
5. Буеверов А.О., 2014 г.
6. Филимонкова Н.Н., Воробьева Ю.В., Топычканова Е.П., 2013 г.
7. Новикова Т.И., Новиков В.С., 2011 г.
8. Приказ МЗ РФ от 10.11.2011 г. № 1340н «Об утверждении Перечня лекарственных средств, отпускаемых по рецептам врача (фельдшера) при оказании дополнительной бесплатной медицинской помощи отдельным категориям граждан, имеющим право на получение государственной социальной помощи»
9. Приказ Минздрава РФ от 09.11.2012 N 772н «Об утверждении стандарта специализированной медицинской помощи при других заболеваниях печени»
10. Инструкция по медицинскому применению
11. И.Г. Никитин, И.Е. Байкова, В.М. Волынкина и соавторы, 2009г.
Интерпретация биохимического анализа крови при патологии печени. Синдром цитолиза. Часть 1.
Опубликовано в журнале:
«Практика педиатра» июнь, 2017г.
М. Г. Ипатова 1, 2 к.м.н., Ю. Г. Мухина 1 д.м.н. профессор, П. В. Шумилов 1 д.м.н., профессор
1 Российский национальный исследовательский медицинский университет им. Н. И. Пирогова
МЗ РФ, Москва
2 Детская Городская Клиническая Больница № 13 им. Н. Ф. Филатова, Москва
Ключевые слова: печень, синдром цитолиза, аланинаминотрансфераза, аспартатамино—трансфераза, гепатопротективные препараты
В статье изложены биохимические лабораторные показатели и их клиническое значение при заболеваниях печени, протекающих с синдромом цитолиза. Отдельное внимание уделено механизмам действия гепатопротективных препаратов, применяемых при цитолитическом синдроме.
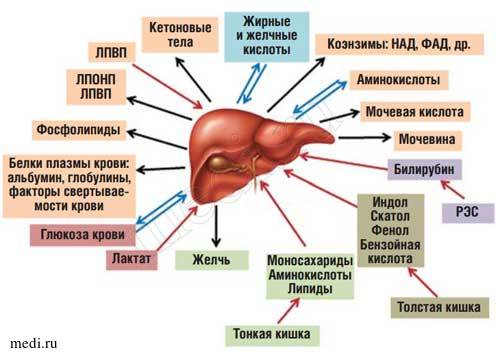
Рис. 1. Роль печени в обмене веществ.
Печень представляет собой центральный орган химического гомеостаза организма, где создается единый обменный и энергетический пул для метаболизма почти всех классов веществ [1]. К основным функциям печени относятся: метаболическая, депонирующая, барьерная, экскреторная, гомеостатическая и детоксицирующая [2]. Печень может обезвреживать как чужеродные экзогенные вещества, обладающие токсическими свойствами, так и синтезированные эндогенно.
Таблица 2. Причины повышения уровня аминотрансфераз
Печеночные причины
Внепеченочные причины
•Вирусные гепатиты (В, С, ЦМВ и др.)
•Хронические инфекции и паразитарные
заболевания (эхинококкоз, токсоплазмоз и др.)
•Неалкогольный стеатогепатит
•Аутоиммунные заболевания печени
•Злоупотребление алкоголем
•Прием лекарственных препаратов
(статины, некоторые антибиотики, противогрибковые препараты, нестероидные
противовоспалительные препараты,
глюкокортикостероиды, другие)
•Метаболические заболевания печени
(галактоземия, фруктоземия, гликогенозы,
дефицит альфа1-антитрипсина,
аминоацидопатии, нарушение цикла мочевины, нарушение окисления жирных кислот, митохондриальная гепатопатия, некоторые лизосомные заболевания (болезнь
Гоше, болезнь Ниманна-Пика, дефицит кислой липазы и др.), муковисцидоз, синдром Швахмана-Даймонда, гемохроматоз, болезнь Вильсона и др.)
•врожденные и приобретенные дефекты
сосудов системы воротной вены (болезнь
Бадда-Киари и др.)
•Цирроз печени
•Опухоли печени
•Патология сердца (острый инфаркт
миокарда, миокардит)
•Повышенная физическая нагрузка
•Наследственные нарушения мышечного
метаболизма
•Приобретенные мышечные заболевания
•Травма и некроз мышц
•Целиакия
•Гипертиреоз
•Тяжелые ожоги
•Гемолиз эритроцитов
•Нарушение кислотно-щелочного равновесия
•Сепсис
Находясь между портальным и большим кругами кровообращения, печень выполняет функцию большого биофильтра. Через воротную вену в нее поступает более 70% крови, остальная кровь попадает через печеночную артерию. Большая часть веществ, всасывающихся в пищеварительном тракте (кроме липидов, транспорт которых в основном осуществляется через лимфатическую систему), поступает по воротной вене в печень [2]. Таким образом, печень функционирует как первичный регулятор содержания в крови веществ, поступающих в организм с пищей (рис 1).
Большое разнообразие функций гепатоцитов приводит к тому, что при патологических состояниях печени нарушаются биохимические константы, отражающие изменения многих видов обмена. Поэтому стандартный биохимический анализ крови включает определение различных параметров, отражающих состояние белкового, углеводного, липидного и минерального обмена, а также активность некоторых ключевых ферментов.
Концентрация ферментов в клетках значительно выше, чем в плазме крови; в норме только очень незначительная часть определяется в крови. Наиболее частыми причинами повышения уровня ферментов в сыворотке крови являются: прямое поражение клеточных мембран, в частности вирусами и химическими соединениями, гипоксия и ишемия тканей. Иногда активность ферментов увеличивается в результате их повышенного синтеза в тканях. Определение активности тех или других ферментов в сыворотке крови позволяет судить о характере и глубине поражения различных компонентов гепатоцитов [3, 4].
Ферменты в зависимости от их локализации можно разделить на несколько групп:
1) универсально распространенные ферменты, активность которых обнаруживается не только в печени, но и в других органах – амино-трансферазы, фруктозо-1-6-дифосфатальдолаза;
2) печеночноспецифические (органоспе-цифические) ферменты; их активность исключительно или наиболее высоко выявляется в печени. К ним относятся холинэстераза, орнитин-карбамилтрансфераза, сорбитдегидрогеназа и др.;
3) клеточноспецифические ферменты печени относят преимущественно к гепатоцитам,
купферовским клеткам или желчным канальцам (5-нуклеотидаза, аденозинтрифосфатаза);
4) органеллоспецифические ферменты, являются маркерами определенных органелл
гепатоцита: митохондриальные (глутаматде-гидрогеназа, сукцинатдегидрогеназа, цитохромоксидаза), лизосомальные (кислая фос фатаза, дезоксирибонуклеаза, рибонуклеаза), микросомальные (глюкозо-6-фосфатаза).
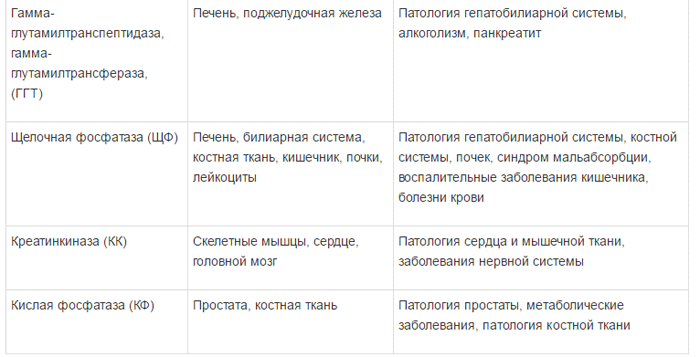
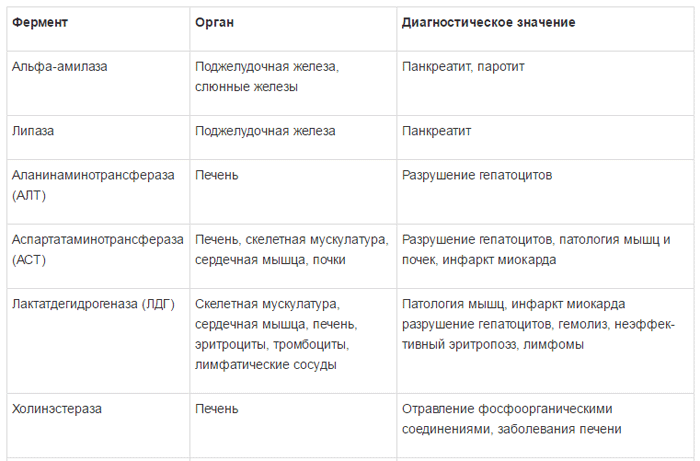
Специфичность ферментов и их диагностическое значение представлено в таблице 1 [5].
Исходя из выше изложенного, следует, что в большинстве случаев отклонения активности сывороточных ферментов от «нормы» неспецифичны и могут быть вызваны различными причинами. Поэтому нужно с большой осторожностью относиться к интерпретации этих отклонений, сопоставляя их с клинической картиной заболевания и данными других лабораторных и инструментальных методов исследования [5, 6].
В связи с использованием в клинических лабораториях разных методов исследования ферментов и единиц измерения их активности целесообразно каждый раз, получив результаты анализа, уточнить, каким методом и в каких единицах была измерена активность фермента, и сопоставить полученное значение с «нормой», принятой в данной лаборатории.
Отдельное место занимает макроэнзиме-мия – редкое и крайне сложное для дифференциальной диагностики состояние, при котором происходит комплексирование молекул того или иного энзима с иммуноглобулинами или небелковыми веществами. Описаны клинические наблюдения макро-КФК-емии, макро-ЛДГ-емии, макро-АСТ-емии, макро-ГГТ-емии, макроамилаземии. Макро-энзимемии сложны для диагностики и дифференциальной диагностики и ведут к проведению инвазивных методов обследования и необоснованному лечению.
В основе выявления макроэнзимемии лежит выявление отличий молекулы макрофермента от молекулы обычного энзима. Некоторые из этих методов являются прямыми, т. е. такими, которые позволяют непосредственно определить присутствие в крови ферментного комплекса, имеющего гораздо более высокий молекулярный вес, чем молекула нормального фермента. В основу прямого метода положено разделение белков сыворотки по молекулярному весу. Другие же методы являются непрямыми, так как выявление макроэнзима в крови проводится не путем выявления самого ферментного комплекса, а основываются на выявлении какого-либо из свойств макроэнзима. Прямые тесты имеют большее диагностическое значение и влекут за собой меньше технических и диагностических ошибок.
В некоторых ситуациях повышение ферментов является физиологическим: уровень щелочной фосфатазы повышен у подростков в период вытяжения (период ускорения роста), у здоровых женщин во время третьего триместра беременности (за счет плаценты). Однако очень высокую активность щелочной фосфатазы наблюдают у женщин с преэк-лампсией, что связно с нарушением кровообращения плаценты [7].
Большое значение в диагностике заболеваний печени имеют анамнестические данные и клиническая картина заболевания. Из анамнеза следует попытаться узнать о факторах риска заболеваний печени, обращая особое внимание на семейный анамнез, прием лекарств, витаминов, растительных добавок, наркотиков, алкоголя, трансфузии препаратов крови, патологические результаты печеночных проб в прошлом и симптоматику заболеваний печени. Клиническое обследование позволяет диагностировать до 50–60% патологических состояний. Более детальная дифференциальная диагностика основана на иммунохимических методах. Они позволяют детализировать характер вирусной, а также паразитарной инфекции, определить локализацию неопластического процесса, определить этиологию аутоиммунного заболевания, уточнить вид нарушения наследственных заболеваний обмена веществ.
При патологии печени в биохимическом анализе крови выделяют 4 синдрома:
• Синдром печеночно-клеточной недостаточности
• Мезенхиально-воспалительный синдром.
В данной статье мы подробно разберем по
казатели, характерные для синдрома цитолиза.
Синдром цитолиза – это синдром, обусловленный нарушением проницаемости клеточных мембран, распадом мембранных структур или некрозом гепатоцитов с выходом в плазму ферментов (АЛТ, АСТ, ЛДГ, альдолазы и др.).
АМИНОТРАНСФЕРАЗЫ: аспартатаминотрансфераза и аланинаминотрансфераза
Референтные значения: у новорожденных детей до 1 мес. – менее 80 Ед/л; от 2 мес. до 12 мес. – менее 70 Ед/л., с 1 года до 14 лет – менее 45 Ед/л, у женщин – менее 35 Ед/л, у мужчин – менее 50 Ед/л.
В клинической практике широко применяется одновременное определение уровня двух трансаминаз – аспартатаминотрансферазы (AСT) и аланинаминотрансферазы (АЛТ) в сыворотке крови.
Ферменты АЛТ и АСТ содержатся практически во всех клетках человеческого организма. Однако самый высокий уровень фермента АЛТ содержится в печени, поэтому уровень данного энзима служит специфическим маркером поражения печени. В свою очередь, АСТ помимо печени (в порядке снижения концентрации) содержится в сердечной и скелетных мышцах, почках, поджелудочной железе, легких, лейкоцитах и эритроцитах [6, 7, 8].
В печени АЛТ присутствует только в цитоплазме гепатоцитов, а АСТ – в цитоплазме и в митохондриях. Более 80% печеночной АСТ представлено именно митохондриальной фракцией [6, 7, 8].
В норме постоянство концентрации транс-аминаз в плазме крови отражает равновесие между их высвобождением вследствие физиологического апоптоза состарившихся гепатоци-тов и элиминацией. Соотношение синтеза АСТ/ АЛТ в печени равно 2,5/1. Однако при нормальном обновлении гепатоцитов уровни АСТ и АЛТ в плазме крови практически одинаковы (30–40 Ед/л) из-за более короткого периода полувыведения АСТ (18 ч против 36 ч у АЛТ).
При заболеваниях печени в первую очередь и наиболее значительно повышается активность АЛТ по сравнению с АСТ. Например, при остром гепатите, независимо от его этиологии, активность аминотрансфераз повышается у всех больных, однако преобладает уровень АЛТ, содержащейся в цитоплазме, вследствие ее быстрого выхода из клетки и поступления в кровяное русло. Таким образом, по уровню АЛТ судят о биохимической активности заболевания печени. Повышение показателя в 1,5–5 раз от верхней границы нормы свидетельствует о низкой активности процесса, в 6–10 раз – об умеренной и более 10 раз – о высокой биохимической активности. Повышение активности трансаминаз более 6 месяцев является биохимическим признаком хронического гепатита [6, 7].
Некоторые лекарственные препараты (например, вальпроевая кислота) метаболизируются в митохондриях гепатоцитов [9], поэтому ранним лабораторным маркером гепатотоксичности может быть лишь изолированное повышение АСТ.
Помимо патологии печени АСТ служит одним из ранних маркеров повреждения сердечной мышцы (повышается у 93–98% больных инфарктом миокарда до 2–20 норм); специфичность его не высока. Уровень ACT в сыворотке крови возрастает через 6–8 часов после начала болевого приступа, пик приходится на 18–24 часа, активность снижается до нормальных значений на 4–5 день. Нарастание активности фермента в динамике может свидетельствовать о расширении очага некроза, вовлечении в патологический процесс других органов и тканей, например, печени [7].
Интенсивные мышечные упражнения с чрезмерной нагрузкой также могут вызвать преходящее увеличение уровня ACT в сыворотке крови. Миопатии, дерматомиозиты и другие заболевания мышечной ткани вызывают повышение трансаминаз, преимущественно за счет АСТ.
Умеренное увеличение активности АСТ (в 2–5 раз от верхней границы нормы) отмечается при острых панкреатитах и гемолитических анемиях.
При латентных формах цирроза печени повышения активности ферментов, как правило, не наблюдают. При активных формах цирроза стойкий незначительный подъем аминотрансфераз выявляют в 74–77% случаев, и, как правило, преобладает активность АСТ над АЛТ в два и более раз.
Снижение активности АЛТ и АСТ имеет место при недостаточности пиридоксина (витамина В6), при почечной недостаточности, беременности.
Ниже приведены печеночные и внепеченочные причины повышения активности аминотрансфераз в сыворотке крови (табл. 2).
Помимо оценки уровня трансаминаз в клинической практике широко применяется коэффициент де Ритиса – отношение АСТ к АЛТ (АСТ/АЛТ). В норме значение этого кэффициента составляет 0,8–1,33. Следует отметить, что расчет коэффициента де Ритиса целесообразен только при выходе АСТ и/или АЛТ за пределы референтных значений.
У новорожденных детей соотношение АСТ/АЛТ обычно превышает 3,0, однако к пятому дню жизни снижается до 2,0 и ниже.
При поражениях печени с разрушением гепатоцитов преимущественно повышается АЛТ, коэффициент де Ритиса снижается до 0,2–0,5. При патологии сердца преобладает уровень АСТ, и коэффициент де Ритиса повышается. Однако для точной дифференциальной диагностики этот коэффициент непригоден, так как нередко при алкогольном поражении печени, неалкогольном стеатогепатите, циррозе печени также преобладает повышение АСТ и коэффициент де Ритиса составляет 2,0–4,0 и более. Значение данного коэффициента выше нормы часто наблюдается при обтурационных желтухах, холециститах, когда абсолютные значения АЛТ и АСТ невелики.
1. При остром вирусном и хроническом гепатитах, особенно на ранних стадиях, активность АЛТ выше, чем АСТ (коэффициент де Ритиса меньше 1,0). Тяжелое поражение паренхимы печени может изменить это соотношение.
2. При алкогольном гепатите и циррозе нередко активность АСТ оказывается выше, чем АЛТ (коэффициент де Ритиса больше 1,0).
3. При остром ИМ активность АСТ выше, чем АЛТ (коэффициент де Ритиса больше 1,5).
ЛАКТАТДЕГИДРОГЕНАЗА
Референтные значения ЛДГ для новорожденных – до 600 Ед/л, у детей с 1 года до 12 лет активность ЛДГ – 115 – 300 Ед/л, для детей старше 12 лет и у взрослых норма ЛДГ – до 230 Ед/л.
Лактатдегидрогеназа (ЛДГ) – гликолитический цинксодержащий фермент, обратимо катализирующий окисление L-лактата в пируват, широко распространен в организме человека. Наибольшая активность ЛДГ обнаружена в почках, сердечной мышце, скелетной мускулатуре и печени. ЛДГ содержится не только в сыворотке, но и в значительном количестве в эритроцитах, поэтому сыворотка для исследования должна быть без следов гемолиза [7].
При электрофорезе или хроматографии удается обнаружить 5 изоферментов ЛДГ, отличающихся по своим физико-химическим свойствам. Наибольшее значение имеют два изофермента – ЛДГ1 и ЛДГ5. Фракция ЛДГ1 более активно катализирует обратную реакцию превращения лактата в пируват. Она в большей степени локализуется в сердечной мышце и некоторых других тканях, в норме функционирующих в аэробных условиях. В связи с этим миокардиальные клетки, обладающие богатой митохондриальной системой, окисляют в цикле трикарбоновых кислот не только пируват, образующийся в результате протекающего в них самих процесса гликолиза, но и лактат, образующийся в других тканях. Фракция ЛДГ5 более эффективно катализирует прямую реакцию восстановления пирувата в лактат. Она локализуется преимущественно в печени, в скелетных мышцах. Последние нередко вынуждены функционировать в анаэробных условиях (при значительной физической нагрузке и быстро наступающем утомлении). Образующийся при этом лактат с кровотоком попадает в печень, в которой он используется для процесса глюконеогенеза (ресинтеза глюкозы), а также в сердце и другие ткани, где происходит его преобразование в пируват и вовлечение в цикл трикарбоновых кислот (цикл Кребса). Любое повреждение клеток тканей, содержащих большое количество ЛДГ (сердце, скелетные мышцы, печень, эритроциты), приводит к повышению активности ЛДГ и ее изо-ферментов в сыворотке крови. Наиболее частыми причинами повышения активности ЛДГ являются:
1. Поражение сердца (острый инфаркт миокарда, миокардит, застойная сердечная недостаточность); в этих случаях обычно преобладает повышение активности ЛДГ1 и/или ЛДГ2.
2. Поражение печени (острые и хронические гепатиты, цирроз печени, опухоли и метастазы печени), когда преимущественно увеличивается изофермент ЛДГ5, ЛДГ2, ЛДГ4.
3. Повреждение скелетных мышц, воспалительные и дегенеративные заболевания
скелетных мышц (преимущественно увеличение изофермента ЛДГ1, ЛДГ2, ЛДГ3).
4. Заболевания крови, сопровождающиеся распадом клеток крови: острый лейкоз, гемолитическая анемия, В12-дефицитная анемия, серповидноклеточная анемия, а также заболевания и патологические состояния, сопровождающиеся разрушением тромбоцитов (массивная гемотрансфузия, эмболия легочной артерии, шок и др.). В этих случаях может преобладать повышение активности ЛДГ2, ЛДГ3.
5. Острый панкреатит.
6. Заболевания легких (пневмония и др.)
8. Опухоли (повышенный уровень ЛДГ наблюдается в 27% случаев опухолей в I стадии и в 55% – метастатических семином).
Следует помнить, что многие заболевания сердца, скелетных мышц, печени и крови могут сопровождаться повышением активности в сыворотке крови общей ЛДГ без отчетливого преобладания какого-либо из ее изоферментов.
Таблица 3. Эффективность гепатопротекторов при синдроме цитолиза (по С. В. Морозову с соавт., 2011 г. и Н. Б. Губергриц, 2012 г.) [10]
Цитолиз печени что это такое
Омская государственная медицинская академия
Омская государственная медицинская академия
Цитолитический синдром в клинической практике
Журнал: Доказательная гастроэнтерология. 2014;3(1): 43-47
Саламахина О. Ф., Ливзан М. А. Цитолитический синдром в клинической практике. Доказательная гастроэнтерология. 2014;3(1):43-47.
Salamakhina O F, Livzan M A. Cytolytic syndrome in the clinical practice. Russian Journal of Evidence-Based Gastroenterology. 2014;3(1):43-47.
Омская государственная медицинская академия
Цитолитический синдром — важный в клинике лабораторный синдром. Зачастую именно он венчает начало диагностического поиска для уточнения характера и причины поражения печени. Следует помнить, что развитию синдрома цитолиза у пациента одновременно могут способствовать несколько причин.
Омская государственная медицинская академия
Омская государственная медицинская академия
Хронический гепатит (ХГ) относится к заболеваниям, протекающим со скудной клинической симптоматикой. И только наличие цитолитического синдрома позволяет установить диагноз [1, 2]. ХГ — мультифакториальное заболевание: по-прежнему гепатотропные вирусы, ожирение и алкоголь относятся к наиболее частым причинам этой болезни [3—5]. В Западно-Сибирском регионе одной из причин остается описторхоз [6, 7]. В последние годы часто приходится сталкиваться с тем, что у одного пациента имеет место сочетание нескольких причин одновременно. Оценить вклад каждой причины в развитие болезни иногда достаточно сложно.
Приводим ниже клинический случай, демонстрирующий трудности в этиологической диагностике ХГ.
Пациент А., 37 лет, обратился с жалобами на ноющую боль в правом подреберье, усиливающуюся после приема алкоголя, изжогу, боль в эпигастрии после приема пищи, невыраженную общую слабость.
Из анамнеза известно, что около 10 лет назад при проведении профилактического осмотра были впервые выявлены суммарные антитела к вирусному гепатиту (ВГ) С. Эти же результаты были зафиксированы и во время последующих профилактических осмотров, но, учитывая отсутствие изменений в биохимическом анализе крови, дальнейшего обследования не проводилось. Около 5—6 лет назад пациента стали периодически беспокоить ноющие боли в правом подреберье; наибольшую их интенсивность он связывал с приемом алкоголя. В последние 1,5 года боли в правом подреберье стали беспокоить чаще, что и послужило поводом для обращения к гастроэнтерологу. Кроме того, при детальном расспросе выяснилось, что в детском возрасте лечился у педиатра с диагнозом хронический гастрит. Многие годы никаких жалоб не предъявлял, однако в последние 3—4 года стал отмечать неинтенсивные боли в эпигастрии без четкой связи с характером и временем приема пищи.
Из анамнеза жизни: туберкулез, вирусный гепатит отрицает. Имел в прошлом незащищенные половые контакты. Употребление наркотических препаратов отрицает. Алкоголем злоупотребляет периодически в течение последних 10—12 лет, что объясняет своей профессиональной деятельностью. Аллергических реакций не было. Хронические заболевания: хронический гастрит, хронический дуоденит, артериальная гипертензия (АГ) I стадии, остеохондроз распространенный. Лекарственных препаратов в постоянном режиме не принимает. Из других заболеваний отмечает дважды перенесенную пневмонию. Гемотрансфузия проводилась однократно в 1975 г., во время лечения пневмонии в роддоме, без осложнений. Операции: аппендэктомия в 1990 г. Серьезных травм не было. Наследственность: отец страдает язвенной болезнью двенадцатиперстной кишки, бронхиальной астмой, у матери — А.Г. Эпидемиологический анамнез: употребляет в пищу рыбу семейства карповых в вяленом, сушеном виде.
При осмотре состояние удовлетворительное. Кожные покровы смуглые, без высыпаний. Видимые слизистые губ, носа, ротовой полости влажные, высыпаний нет. Язык влажный, обложен у корня белым налетом. Астенического телосложения. Питание: ожирение II степени (рост 182 см, масса тела 119 кг, индекс массы тела — 35,9 кг/м 2 ). Периферические лимфатические узлы не увеличены. Щитовидная железа 0 стадии (ВОЗ), пальпируется мягкоэластичный, безболезненный перешеек. При перкуссии легких — ясный, легочный звук. При аускультации выслушивается везикулярное дыхание, хрипов нет. Частота дыхания 15 в мин. Пульс 71 уд/мин, полный, не напряжен. Артериальное давление 140/90 мм рт.ст. Границы относительной сердечной тупости в пределах нормы. Тоны сердца несколько приглушены, ритмичные. Живот увеличен в объеме за счет подкожно-жировой клетчатки, толщина жировой складки на уровне пупка — 6 см. При поверхностной пальпации живот мягкий, «чувствительный» в правом подреберье. Отделы толстой кишки при глубокой пальпации без особенностей. Печень выступает на 1,5 см из-под края реберной дуги. Перкуторно размеры печени по Курлову 14×10×6 см. Симптомы желчного пузыря — отрицательные. Селезенка не увеличена и не пальпируется. Почки не пальпируются. Симптом поколачивания отрицательный.
При лабораторном обследовании патологических изменений в общих анализах крови и мочи не выявлено. В биохимическом анализе крови выявлены отклонения: повышение аланинаминотрансферазы (АЛТ) до 74 Ед/л (норма АЛТ для мужчин до 42 Ед/л), повышение аспартатаминотрансферазы (АСТ) до 49 Ед/л (норма АСТ для мужчин до 37 Ед/л), повышение гамма-глутамилтранспептидазы (ГГТП) до 98 Ед/л (норма ГГТП у мужчин до 55 Ед/л), повышение щелочной фосфатазы (ЩФ) до 290 Ед/л (норма — до 270 Ед/л). Остальные показатели биохимического анализа крови в пределах нормы. Копрограмма — без патологических изменений.
Ультразвуковое исследование (УЗИ) органов брюшной полости и почек показало признаки гепатомегалии, диффузных изменений печени и поджелудочной железы, характерных для стеатоза.
Заключение фиброгастродуоденоскопии (ФГДС) следующее: «Эритематозный (экссудативный) гастрит с поражением антрума, патологические изменения умеренные. Хронические эрозии антрального отдела. Дуоденогастральный рефлюкс. Дуоденит проксимальный поверхностный. Дуоденит дистальный поверхностный. Взяты 2 биоптата из тела желудка и антрального отдела».
Получено заключение гистологического исследования биоптатов: «Морфологические признаки воспаления средней степени (тела и антрума), без атрофии, без кишечной метаплазии. Морфологические признаки хеликобактерной колонизации отсутствуют».
Учитывая наличие цитолитического, невыраженного холестатического синдромов, данных анамнеза (незащищенные половые контакты, гемотрансфузия, отягощенный эпидемиологический анамнез) была предпринята попытка исключить вирусную природу гепатита, описторхозную инвазию и ВИЧ-инфекцию.
Описторхоз — природно-очаговый зооантропоноз. Распространен в виде очагов различной интенсивности. Возбудитель описторхоза обнаружен у кошек, собак, лисиц и других животных, а также у моллюсков и рыб семейства карповых во многих странах Европы: Австрии, Албании, Болгарии, Венгрии, Германии, Греции, Голландии, Испании, Италии, Польше, Румынии, Турции, Финляндии, Франции. Однако подавляющая часть современного мирового ареала возбудителя описторхоза сосредоточена на территории России и Украины, а точнее — в трех основных очагах: Обь-Иртышском, Волго-Камском и Днепровском. Эндемичной по описторхозу территорией является Западная Сибирь и Казахстан по Оби, Иртышу, Тоболу и их притокам, а также очаги по Волге, Каме и их притокам, по Неману, Северной Двине, Припяти, бассейну Дона.
Источником инвазии при описторхозе является окончательный хозяин — человек и домашние животные (кошки, собаки, свиньи и др.). Нельзя недооценивать и роль диких животных (волк, лисица, кабан, ондатра, водяная полевка и другие) в сохранении и поддержании природных очагов, а следовательно, и возбудителя описторхоза. С испражнениями окончательного хозяина яйца описторхов попадают в водоем разными путями: при сбросе сточных вод, смыве нечистот дождевыми и талыми водами с берегов и так далее.
Продолжительность жизни свободноплавающих церкарий Opistorсhis felineus не превышает двух суток. Заражение карповых рыб зависит от численности моллюсков, эмиссии церкарий, гидрологических особенностей водоема.
Описторхозом заражаются люди любого возраста, но чаще в возрасте 20—40 лет, особенно рыбаки, члены их семей, рабочие рыболовецких артелей, рыбообрабатывающих предприятий, плавсостав, бакенщики, т. е. люди, профессионально связанные с выловом или обработкой рыбы. Они составляют основную группу риска.
Заражение происходит при употреблении в пищу недостаточно термически обработанной, а также малосоленой, вяленой, сырой рыбы. Метацеркарии отличаются высокой жизнестойкостью: при температуре 3—12 °С сохраняются до 25 дней, при 30—40 °С — 5—6 ч. Они менее устойчивы к действию высоких температур и крепкого посола.
Острая фаза. Заболевание начинается через 5—42 дня после заражения, однако в среднем инкубационный период составляет 21 день. Чаще наблюдается острое начало болезни, реже — постепенное, с проявлением недомогания, слабости, потливости, субфебрилитета. В дальнейшем описторхоз может протекать субклинически, малосимптомно, сопровождаясь кратковременным подъемом температуры до 38 °C, эозинофилией до 15—20% на фоне умеренного лейкоцитоза. Острый описторхоз средней тяжести (встречается у 40—50% больных) характеризуется высокой лихорадкой с постепенным нарастанием температуры до 39—39,5 °С, катаральными явлениями в верхних дыхательных путях. Эозинофилия достигает 25—60%, нарастает лейкоцитоз, умеренно повышается СОЭ до 20—40 мм/ч.
У больных легкой и средней тяжести течения через 1—2 нед наступает улучшение, а далее — латентный период болезни, который переходит в хроническую форму.
При тяжелом течении острого описторхоза (у 10—20% больных) выделяют тифоподобный, гепатохолангитический, гастро-энтероколитический варианты и вариант с преимущественным поражением дыхательных путей в виде астмоидного бронхита или пневмонии.
В некоторых случаях отмечается затяжное течение острой стадии — лихорадка затягивается до 2 и более месяцев, сохраняются признаки поражения печени, легочный синдром.
По мере стихания проявлений острой стадии состояние больного улучшается, болезнь переходит в хроническую фазу чаще с проявлениями дискинезии желчных путей, хронического холангиохолецистита, хронического панкреатита.
Дискинезия желчных путей и холестаз способствуют присоединению вторичной бактериальной инфекции. В этих случаях возможно развитие тяжелого поражения гепатобилиарной системы по типу холангиогепатита с выраженным болевым синдромом, увеличением печени, желтухой, нарушением функциональных проб. Чаще это персистирующий гепатит с симптомами «малой печеночной недостаточности» и астеновегетативного синдрома. В случаях присоединения поражения поджелудочной железы выявляются симптомы панкреатита.
Превалируют явления астенизации организма за счет угнетения и даже истощения гипофизарно-надпочечниковой системы.
В тяжелых случаях прогноз становится серьезным. К числу осложнений описторхоза относятся цирроз печени, желчный перитонит, первичный рак печени и поджелудочной железы.
В хронической фазе описторхоза также часто отмечаются эозинофилия, но менее выраженная; лейкопения, умеренная гипохромная анемия.
У местных жителей очагов распространения описторхов отмечается субклиническое течение инвазии с умеренными проявлениями астеновегетативного или диспепсического синдрома, случаи острой фазы регистрируются редко. Наиболее частой формой описторхоза является холангиогепатит.
Диагностика описторхоза
Диагностика описторхоза в ранней фазе затруднительна, так как яйца паразитов в желчи и в кале обнаруживаются только через 4—6 нед с момента заражения. Поэтому диагноз острого описторхоза основывается на данных эпидемиологического анамнеза (пребывание в очаге, употребление в пищу сырой, вяленой, малосоленой рыбы) и клинических проявлениях острого аллергического заболевания с лихорадкой, кожными высыпаниями, миалгией, артралгией, катаральными другими явлениями на фоне лейкоцитоза и эозинофилии.
Учитывая высокую концентрацию сывороточных специфических иммуноглобулинов преимущественно класса IgM, можно использовать серологические методы диагностики острого описторхоза. Реакции, к сожалению, могут давать ложноположительные результаты с сывороткой инвазированных фасциолами, дикроцелиями и другими гельминтами.
Для диагностики хронической фазы используют паразитологический метод, основанный на обнаружении яиц описторхов в дуоденальном содержимом или фекалиях через 1—1,5 мес после заражения, а также определении специфических IgG и IgM.
Наиболее эффективными методами копроскопической диагностики являются метод эфир-формалинового осаждения яиц, метод эфир-уксусного осаждения и толстый мазок по Като.
Лечение
Этапность в схеме лечения предусматривает подготовку, назначение антигельминтного препарата (празиквантель) на фоне патогенетической терапии, реабилитацию, диспансеризацию, контроль эффективности лечения [6, 7].
Возвращаясь к рассматриваемому выше клиническому случаю, при исследовании крови пациента на антитела к возможным патогенным агентам были получены следующие результаты.
Антитела суммарные к ВГ С определены методом иммуноферментного анализа (ИФА) — положительно. РНК ВГ С в крови методом амплификации — отрицательно.
Антитела к ВГ В методом ИФА (HBsAg, Анти-HBs, HBеAg, Анти-HBе, Анти-НВсоrе, IgM и IgG) — отрицательно.
Антитела к ВИЧ методом ИФА — отрицательно.
Антитела к O. felineus (IgG и IgМ) — отрицательные. Кал на яйца O. felineus исследовался эфирно-уксусным методом 2-кратно — отрицательно (от 3-го исследования пациент отказался из-за отъезда в командировку).
На основании полученных результатов было сделано диагностическое заключение: «Хронический гепатит смешанной этиологии (стеатогепатит, алкогольный), клинико-биохимическая активность минимальная. Дискинезия желчного пузыря. Хронический гастрит, неатрофический, НР-негативный, рефлюксный, с эрозиями в антральном отделе, обострение. Хронический дуоденит поверхностный, тотальный, обострение. ГЭРБ, эндоскопически негативная».
Рекомендовано проведение гипокалорийной диеты (энергетическая ценность суточного рациона — 1800 ккал/сут) с исключением жирной, жареной, копченой, острой пищи, алкоголя. Назначена лекарственная терапия: S-аденозил-L-метионин в дозе 800 мг внутривенно медленно ежедневно в количестве 10 инъекций, далее по 1 таблетке (400 мг) внутрь 2 раза в день утром и в обед в течение 20 дней. Назначение аденозил-L-метионина продиктовано высоким уровнем доказательной базы (1, A) в отношении этого препарата (Гептрал) [8]. Кроме того, рабепразол по 20 мг 2 раза в день за 30 мин до еды в течение 10 дней, далее по 20 мг за 30 мин до завтрака в течение последующих 10 дней; висмута трикалия дицитрат по 2 таблетки 2 раза в день за 40 мин до еды в течение 3 нед; итоприда гидрохлорид по 1 таблетке (50 мг) 3 раза в день за 30 мин до еды в течение 2 нед.
На повторном приеме через 1 мес пациент жалоб на изжогу и боль в эпигастрии не предъявлял, боль в правом подреберье уменьшилась. Диету соблюдал строго, алкоголь не употреблял. Отмечена нормализация АЛТ, АСТ, ЩФ, снижение ГГТП до 56 МЕ/л. По результатам ФГДС — полная эпителизация эрозий. Рекомендован контроль биохимического анализа крови через 3 мес.
Через 3 мес на приеме у гастроэнтеролога пациент отметил снижение массы тела на 7 кг. Он сообщил о сокращении количества принимаемого алкоголя в 2—3 раза. Лабораторные показатели: АСТ в норме, ЩФ на верхней границе нормы, АЛТ — до 47 Ед/л, ГГТП— до 48 МЕ/л. Рекомендован полный отказ от алкоголя. Контроль биохимического анализа крови, УЗИ органов брюшной полости провести через полгода.
В течение последующего времени пациент самостоятельно проходил санаторно-курортное лечение, где при проведении дуоденального зондирования обнаруживали описторхоз. Проводилась дегельментизация: празиквантель 80 мг/кг массы тела в 3 приема в условиях стационара. В контроле при дуоденальном зондировании через 3 мес паразитов не выявили.
На приеме через 6 мес пациент вновь пожаловался на боль в правом подреберье. Масса тела снизилась еще на 5 кг. Полного отказа от приема алкоголя нет. В анализах отмечается повышение АЛТ, АСТ, ГГТП, повышение общего холестерина до 6,25 ммоль/л; в динамике на УЗИ уменьшение размеров печени до нормальных в сочетании со снижением выраженности признаков жирового гепатоза.
Выполнялась эластометрия печени на аппарате «Фиброскан». Заключение: стадии F0 — 5,1 кПА (по METAVIR).
Вновь были назначены гепатопротекторы: S-аденозил-L-метионин 800 мг внутривенно медленно ежедневно в количестве 10 инъекций, далее по 1 таблетке (400 мг) внутрь 2 раза в день утром и в обед в течение 20 дней, а также эссенциальные фосфолипиды с альфа-токоферолом по 2 капсулы 3 раза в день до еды в течение 2 мес [8, 9].
Впоследствии пациент самостоятельно обращался на прием через 10 мес с болью и тяжестью в правом подреберье. Сохранялся цитолитический синдром: АСТ — 48 Ед/л, АЛТ — 56 Ед/л, значения ГГТП и ЩФ соответствовали нормальным.
Учитывая тот факт, что клинические проявления и дебют заболевания при аутоиммунном гепатите, по данным большинства авторов [4, 10], в 34—60% случаев бывает «неклассическим» — «хроническим» или бессимптомным — выполнено исследование крови на наличие аутоантител класса IgG печени методом иммуноблота. Получены следующие результаты:
— AMA-M2 (пируватдегидрогеназный комплекс) IgG —слабоположительно;
— LKM-1 (микросомы печени и почек, цитохром Р450II D) IgG — отрицательно;
— LC (цитозольный печеночный антиген типа I, форминотрансфераза-циклодезаминаза) IgG — положительно;
— SLA/LP (растворимый печеночный антиген/антиген печени и поджелудочной железы) IgG — положительно.
Для исключения других возможных причин ХГ, оценки индекса гистологической активности и степени фиброза было принято решение о проведении биопсии печени.
Описание. Биоптат представлен фрагментом ткани печени с двумя портальными трактами. Умеренная гидропическая и жировая дистрофия, единичные фокальные некрозы гепатоцитов. Внутридольковая инфильтрация лимфоцитами и единичными полиморфно-ядерными лейкоцитам выражена слабо. Портальные тракты расширены, содержат умеренный лимфоидный инфильтрат с примесью единичных гранулоцитов и распространением в перипортальную зону. Формируются единичные тонкие порто-портальные септы. Заключение. Хронический гепатит, неактивный. Фиброз I—II стадии.
Выполнено исследование РНК ВГ С в ткани печени методом амплификации — отрицательно, ДНК ВГ В — положительно, РНК ВГ D — отрицательно, РНК ВГ G — отрицательно.
Учитывая полученные данные проведено исследование ДНК ВГ В в крови методом амплификации (результат 5 копий/мл).
Диагноз пересмотрен: «Хронический гепатит смешанной этиологии (вирусный — гепатит В — фаза интеграции, вирусная нагрузка 5 копий/мл; стеатогепатит; алкогольный), клинико-биохимическая активность минимальная, фиброз I—II стадии (гистологически). Описторхоз, резидуальный период (дегельминтизация, 2012 г.). Дискинезия желчного пузыря. Хронический гастрит, неатрофический, НР-негативный, рефлюксный, ремиссия. Хронический дуоденит поверхностный, тотальный, ремиссия. ГЭРБ, эндоскопически негативная».
Пациенту даны рекомендации:
1) полный отказ от алкоголя;
2) гипокалорийная диета (1800 ккал/сут) с исключением жирной, жареной, копченой, острой пищи, а также дозированные аэробные физические нагрузки для нормализации массы тела;
3) (фосфолипиды + натрия глицирризинат) по 2 капсулы 3 раза в день в течение 2 мес в сочетании с S-аденозил-L-метионином по 1 капсуле 2 раз в день в течение 1 мес;
4) наблюдение гастроэнтеролога 2 раза в год.
Выводы
1. Поиск причины ХГ при наличии цитолитического синдрома требует всестороннего обследования пациента и нередко сопряжен с определенными трудностями.
2. Одной из частых причин цитолитического синдрома в Западно-Сибирском регионе является описторхоз.
3. Лечение гепатитов смешанной этиологии включает модификацию образа жизни, устранение причины и назначение гепатопротекторов, выбор которых определяется особенностями клинической ситуации. Их назначают курсами по 1—2 мес не менее 2 раз в год.