кальций горит каким цветом
Восстановление легких после коронавируса
Восстанавливаются ли легкие после COVID-19? Да. Но нужно не пропустить сроки реабилитации и серьёзно отнестись к рекомендациям врача.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, недостаточно изучена, однако ясно, что она наносит вред всем органам и тканям человека. Вирус проникает в организм через слизистые оболочки носа, глаз, глотки. Первые симптомы появляются на 2-14 день. Обычно это повышение температуры выше 37.5 градусов Цельсия, насморк, потеря обоняния, сухой кашель, послабление стула, слабость и головная боль. На 6–10 сутки от момента появления первых симптомов могут начать беспокоить одышка, боль в груди, усиление кашля. Это тревожные симптомы, говорящие о поражении легких и требующие проведения дополнительного обследования: компьютерной томографии легких, измерения насыщения крови кислородом (сатурации).
Легкие после COVID-19
Попадая в организм человека через слизистые оболочки дыхательных путей SARS-CoV-2 вызывает мощнейшую воспалительную реакцию. Активируются иммунные клетки, вырабатывается колоссальное количество воспалительных веществ (воспалительных цитокинов). Интенсивность этой реакции скорее всего обусловлена генетически. Именно интенсивностью воспалительной реакции и определяется тяжесть поражения легочной ткани по данным исследований. В легочной ткани поражение при COVID-19 обусловлено как поражением самих альвеол (в которых происходит газообмен и кровь насыщается кислородом из воздуха) нашими собственными иммунными клетками так и поражением легочных сосудов, оплетающих альвеолы. Степень поражения легких можно определить при помощи КТ (компьютерной томографии).
Таблица 1. Поражение лёгких при COVID-19
Процент поражения легочной ткани
Поражена часть лёгкого. Небольшое затруднение дыхания.
ТОП препаратов кальция
Кальций является одним из электролитов в организме. Это минерал, который несет электрический заряд при растворении в крови. Роль кальция в организме сложно переоценить, т. к. он является строительным материалом для костных структур, поддерживает здоровье клеточных мембран и принимает участие в передаче нервных импульсов. Также кальций обладает детоксикационным, противовоспалительным и противоаллергенным действием.
Лучшие препараты кальция представлены в рейтинге ниже. ТОП составлен в зависимости от эффективности и безопасности лекарственных средств, а также на основе отзывов. Не менее важный критерий – соответствие цена-качество. Самостоятельно подобрать лекарство непросто. Для начала следует проконсультироваться с врачом и при необходимости пройти обследование, чтобы уточнить диагноз.
Классификация препаратов кальция
Дефицит кальция часто развивается ползуче, а затем долго остается незамеченным. Это состояние может оказать негативное влияние на здоровье костей. Таким образом, увеличивается риск развития остеопороза и переломов костей.
Эксперты рекомендуют принимать добавки кальция только при доказанном дефиците данного минерала и витамина D или, а также при существующем остеопорозе. Главное – правильно подобрать препарат и дозировку.
Причины дефицита кальция в организме
Чтобы правильно выполнять свои разнообразные задачи, кальций должен присутствовать в организме в достаточном количестве. Но что такое достаточное количество? Суточные потребности разнятся в зависимости возрастных групп. В отличие от многих других питательных веществ, потребность в кальции не зависит от половой принадлежности. Мужчины и женщины нуждаются в минерале в одинаковой степени.
Таблица – Суточная потребность в кальции в зависимости от возраста
Кальций ионизированный (Ca++) (венозная кровь) в Москве
Ионизированный или свободный кальций — кальций, не связанный с белками и циркулирующий в крови.
Приём и исследование биоматериала
Комплексы с этим исследованием
Когда нужно сдавать анализ Кальций ионизированный (Ca++)?
Подробное описание исследования
Кальций – важнейший макроэлемент, который принимает участие в формировании костей и зубов, проведении электрического импульса по нервным волокнам, сокращении мышц, в том числе и миокарда. Также кальций является необходимым участником процесса свертывании крови, отвечает за нормальную перистальтику кишечника, предотвращение запоров и аллергических реакций, регулирует выработку кальцитонина – одного из важнейших гормонов паращитовидной железы и отвечает за нормальный сон.
На долю ионизированного кальция приходится около половины общего кальция в организме. Его концентрация меняется в течение суток, достигая своего максимума в 2-4 часа ночи, а минимума — в районе 8 часов вечера.
Уровень свободного кальция регулируется паратгормоном, кальцитонином и витамином D.
Что ещё назначают с этим исследованием?
Использованная литература
1.Алан Г.Б «Клиническое руководство Тица по лабораторным тестам»
2.Тиц Н.М. «Клиническое руководство по лабораторным тестам»
Подготовка к исследованию
1. Кровь сдают утром натощак (после последнего приема пищи должно пройти как минимум 8 часов).
2. Вечером накануне поужинайте легкой нежирной пищей. За 2 часа до сдачи крови на анализ нельзя курить, пить кофе и чай, а также фруктовые соки. Допустимо употребление небольшого количества негазированной воды.
3. В течение 24 часов до анализа крови нельзя употреблять лекарственные препараты (по согласованию с лечащим врачом). Также откажитесь от алкоголя за 3 суток до исследования.
4. За 1 час до исследования избегайте психоэмоционального напряжения, физического напряжения, такого, как быстрый подъем по лестнице, бег. Желательно прийти в отделение лаборатории заблаговременно и в течение 10-15 минут до сдачи крови спокойно посидеть.
5. Не сдавайте кровь сразу после физиотерапевтических процедур, массажа, инструментальных обследований, таких как УЗИ и рентген. Это может повлиять на показатели крови и исказить результаты исследования.
6. Если вы контролируете лабораторные показатели в динамике, постарайтесь сдавать каждый анализ в одно и то же время при одинаковых условиях.
Противопоказания и ограничения
Интерпретация результата
Снижение показателя наблюдается при:
• Первичном гипопаратиреоидизме
• Нехватке витамина D и магния
• Остром панкреатите
• Почечной недостаточности
• Обширных травмах и ожогах
• Остеопорозе
• Злоупотреблении алкоголем
• Повышенном содержании натрия в крови
• Использовании ряда лекарственных препаратов (гепарин, противосудорожные средства и др.)
Повышение показателя наблюдается при:
• Первичном гиперпаратиреоидизме
• Передозировке витамина D
• Гормонпродуцирующих опухолях, синтезирующих паратгормон
• Злокачественных новообразованиях
• Использовании препаратов-андрогенов
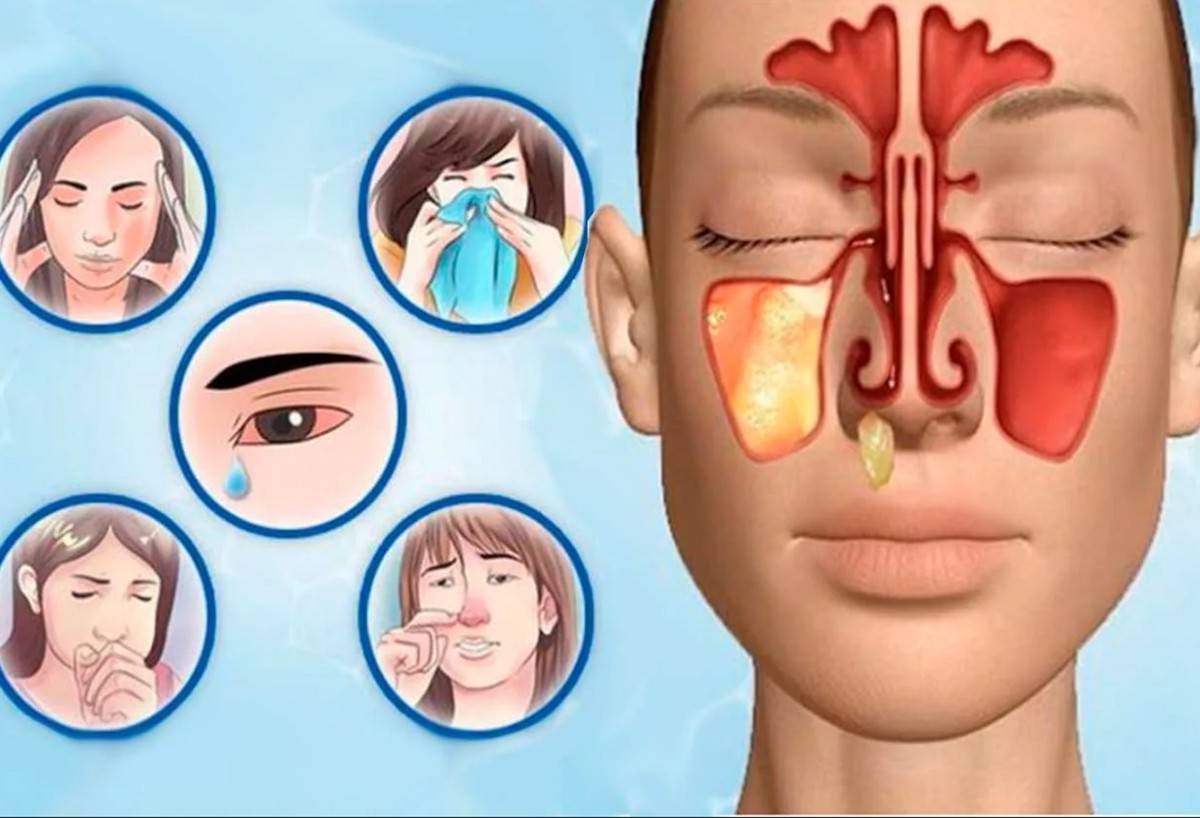
Гайморит: симптомы, особенности лечения и правила профилактики
Гайморит – это воспалительный процесс в области гайморовой пазухи, расположенной в толще черепной кости над верхней челюстью, слева и справа. Этот процесс является одной из разновидностей синуситов (это общее название для воспалительных процессов в области придаточных пазух – лобной, гайморовой, решетчатой или клиновидной). Обычно воспалительный процесс затрагивает слизистые оболочки, выстилающие пазухи изнутри, реже затрагиваются более глубокие слои тканей, вплоть до костных структур. Обычно процесс возникает как осложнение вирусных или бактериальных инфекций в области носоглотки и верхних дыхательных путей.
Исходя из причины развития, механизмов формирования и симптомов, гайморит бывает нескольких типов. Выделение каждого из них важно для определения тактики лечения, прогноза и разработки мер профилактики.
Острый – развивается быстро, как осложнение ОРВИ, насморков, простудных заболеваний, воспаления в области корней зубов на верхней челюсти. Возбудители проникают через каналы, соединяющие пазухи с полостью носа с гайморовыми пазухами, размножаются в полости. Тело начинает активно вырабатывать иммунные клетки и слизь, чтобы обезвредить патогенные организмы. Если слизь закупорит проток пазухи, возникает давление на стенки, усиление воспалительного процесса. По мере очищения пазухи от содержимого воспалительный процесс постепенно затухает.
Хронический – воспалительный процесс, который длится более 4 недель, имеет вялое или волнообразное течение, с периодами обострений. Обычно возникает из-за не долеченной острой формы, наличия аденоидов, тонзиллитов, отитов.
Гнойный – обычно становится осложнением острой формы либо обострения хронического процесса, если процесс не лечится, предпринимаются попытки самолечения или пациент переносит инфекцию на ногах. Патогенные бактерии накапливаются в пазухах, в смеси с лейкоцитами образуют гнойное содержимое. Самое опасное осложнение при этой форме – прорыв гноя в полость черепа, поражение костных тканей, мозга.
Двусторонний – одна из тяжелых форм, поражение локализовано сразу в обеих пазухах – левой и правой. Нередко возникает как осложнение инфекций в полости рта и носоглотки, обычно грибковой или бактериальной. Обычно имеет острое течение, редко переходит в хроническую форму.
Аллергическое поражение возникает у пациентов, страдающих от чрезмерно активной реакции иммунной системы на различные вещества. Особенно часто эта форма синусита бывает при поллинозе, круглогодичном рините, реакции на плесень, пылевых клещей.
Катаральный – преимущественно бывает у детей. Он развивается при проникновении в полость пазух патогенных организмов, что формирует отек и раздражение слизистых. Считается самой легкой формой болезни, проходящей при активном лечении без осложнений и последствий.
Полипозная форма формируется при образовании полипозных разрастаний слизистых из-за чрезмерно быстрого деления клеток. Рост полипов могут провоцировать инфекции, травмы, велика роль наследственности.
Одонтогенный – формируется как результат серьезных проблем зубов, особенно 4-6 зуба на верхней челюсти, корни которых расположены в непосредственной близости от пазухи. Если возникают проблемы в области корней этих зубов, воспаление и нагноение может переходить на пазуху, она заполняется секретом и воспаляется.
Причины
Придаточные пазухи, включая гайморовы, созданы как естественный барьер на пути инфекций, фильтр для различных опасных веществ в воздухе. Они помогают согревать воздух, увлажнять его и очищать от примесей перед попаданием в гортань, и ниже по респираторному тракту. Основная причина воспаления и появления признаков гайморита – это проникновение бактерий, грибков или вирусов, аллергенов. Реже инфекция попадает с током крови из других, отдаленных очагов.
Нарушать работу пазух могут патологии иммунной системы, частые ОРВИ, респираторная форма аллергии, носительство патогенных бактерий в носоглотке (стафило-, стрепто- или менингококк).
Среди ключевых причин, которые могут привести к развитию гайморита, можно выделить:
Осложнения
Не все люди знают, как начинается гайморит, поэтому многие принимают симптомы за тяжелую простуду и лечатся самостоятельно. Это может привести к определенным осложнениям, отдаленным последствиям. Среди ключевых осложнений можно выделить поражения бронхов и распространение инфекции на легкие, развитие отитов (поражение среднего уха), переход болезни в хроническую форму.
Тяжелый и запущенный, своевременно не вылеченный гайморит может привести к воспалению внутренних органов – сердца, глаз, почек, поражению суставов и мозга, его оболочек. Если образуются гнойные полости в гайморовых пазухах, возможен прорыв гноя в кровь (возникает сепсис), проникновение его в соседние пазухи с развитием пансинусита, воспаление мозговых оболочек с явлениями менингита. Всех этих осложнений можно избежать при полноценном лечении гайморита под руководством лор-врача.
Симптомы и диагностика
Конечно, при развитии гайморита нужно немедленно обращаться к врачу, но как понять, что гайморит начался? Начальные признаки неспецифичные – это повышение температуры от незначительной до высокой, сильная слабость, заложенность носа или обильные густые выделения, болезненность в проекции пазух или в области лица.
Боль при гайморите может быть различной – от тупой, давящей до сильной, мучительной. Она локализуется в подглазничной области, может отдавать в область переносицы, лобную зону или верхние зубы. При надавливании на область пазух или наклонах головы вперед она усиливается, распространяясь по подглазничной области. Могут краснеть и отекать веки.
Врачи отмечают некоторые особенности того, как проявляется болезнь в определенных возрастных группах. Так, у взрослых самым ключевым признаком могут быть болевые ощущения, головная боль, нарушение восприятия запахов. Может меняться голос, он становится гнусавым, нос сильно заложен, выделяется полупрозрачная или желто-зеленая слизь. Высокая лихорадка типична для острой формы, при хроническом или аллергическом гайморите болезнь может протекать без температуры.
На фоне поражения пазух возможно слезотечение, неприятный привкус во рту, слабость, постоянное утомление, нарушения аппетита, расстройства сна, ознобы и приступы кашля.
Заразен ли гайморит? Само по себе воспаление – это результат влияния патогенных факторов, и это не заразно. Бактерии или вирусы, которые спровоцировали заболевание, могут передаваться от человека к человеку, но не обязательно вызовут поражение пазух.
Диагноз гайморита ставит лор-врач после проведения ряда тестов и осмотра пациента. Важно подробно рассказать, как началось заболевание, какие жалобы были ранее и имеются в данный момент. Врач осмотрит полость носа и глотку, прощупает проекцию пазух, определяя болезненность.
Дополнительно могут понадобиться КТ или МРТ придаточных пазух, рентгенограмма, УЗИ исследование, эндоскопия носоглотки, при необходимости – биопсия полипозных образований. Назначаются анализы крови, посевы отделяемой из носа слизи для определения флоры, чтобы подобрать необходимые препараты.
Как лечить у взрослого
Терапия болезни должна быть комплексной. Она направлена на борьбу с инфекцией, устранение воспаления, налаживание оттока слизи из пазух и улучшение носового дыхания. В неосложненных случаях возможно лечение гайморита дома под постоянным контролем оториноларинголога. В тяжелых случаях и при необходимости хирургического лечения пациент госпитализируется в стационар.
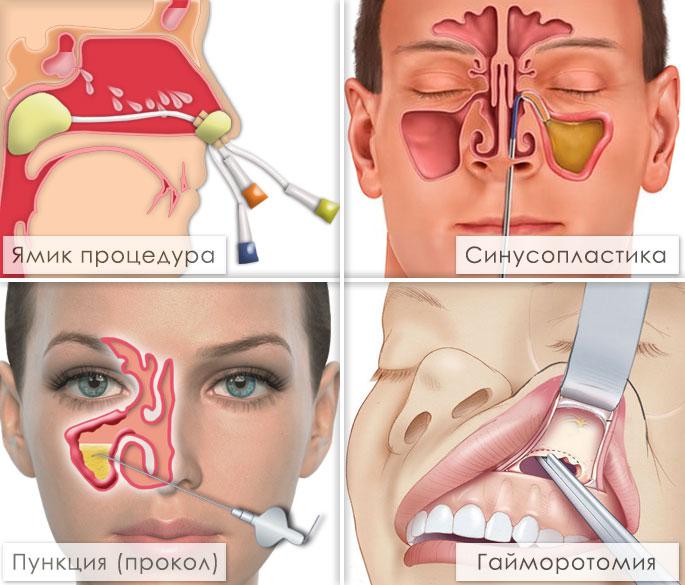
Возможно консервативное лечение с назначением антибактериальных препаратов, противовоспалительных средств, антигистаминных препаратов и различных капель, спреев для носа. Также применяют пункционное лечение или хирургические вмешательства. Выбор зависит от возраста пациента, вида патологии, тяжести состояния и возможных осложнений.
Многим пациентам назначают пункции (с местным обезболиванием) – они помогают удалить гнойное содержимое, помочь в оценке характера воспаления, плюс приносят существенное облегчение. После удаления содержимого пазухи промывают физраствором или фурациллином, вводят растворы антибиотиков и противовоспалительные препараты. Минус подобной тактики – не всегда достаточно одного прокола, поэтому требуется курс процедур в течение нескольких недель. Метод достаточно неприятный, имеет ряд противопоказаний и осложнений, процедура болезненна как во время прокола, так и после него.
Кальций горит каким цветом
14.1. Общая характеристика элементов IA и IIA групп
В случае магния, кальция и стронция из-за малой растворимости образующихся гидроксидов реакция сопровождается образованием осадка:
M 2 

Щелочные металлы реагируют с большинством неметаллов:
2M + H2 = 2MH (при нагревании),
4M + O2 = 2M2O (M – Li),
2M + Cl2 = 2MCl (при обычных условиях),
2M + S = M2S (при нагревании).
Из щелочных металлов, сгорая в кислороде, обычный оксид образует только литий. Остальные щелочные металлы образуют пероксиды (M2O2) или надпероксиды (MO2 – соединения, содержащие надпероксид-ион с формальным зарядом –1 е).
Как и щелочные металлы, металлы элементов IIA группы реагируют со многими неметаллами, но при более жестких условиях:
M + H2 = MH2 (при нагревании; кроме бериллия),
2M + O2 = 2MO (при обычных условиях; Be и Mg – при нагревании),
M + Cl2 = MCl2 (при обычных условиях),
M + S = MS (при нагревании).
В отличие от щелочных металлов с кислородом они образуют обычные оксиды.
С кислотами спокойно реагирует только магний и бериллий, остальные простые вещества очень бурно, часто со взрывом.
Бериллий реагирует с концентрированными растворами щелочей:
Be + 2OH 

В соответствии с положением в ряду напряжений с растворами солей реагируют только бериллий и магний, остальные металлы в этом случае реагируют с водой.
Являясь сильными восстановителями, щелочные и щелочноземельные металлы восстанавливают многие менее активные металлы из их соединений, например, при нагревании протекают реакции:
4Na + MnO2 = 2Na2O + Mn;
2Ca + SnO2 = 2CaO + Sn.
Общий для всех щелочных металлов и металлов IIA группы промышленный способ получения – электролиз расплавов солей.
Кроме бериллия оксиды всех рассматриваемых элементов – основные оксиды, а гидроксиды – сильные основания (у бериллия эти соединения амфотерные, гидроксид магния – слабое основание).
Усиление основных свойств гидроксидов с увеличением порядкового номера элемента в группе легко прослеживается в ряду гидроксидов элементов IIA группы. Be(OH)2 – амфотерный гидроксид, Mg(OH)2 – слабое основание, Ca(OH)2, Sr(OH)2 и Ba(OH)2 сильные основания, но с увеличением порядкового номера растет их растворимость, и Ba(OH)2 уже можно отнести к щелочам.

2.По каким причинам водород помещают в IA группу, а по каким – в VIIA группу?
3.Составьте уравнения реакций следующих веществ с избытком кислорода: Li, Na, K, LiH, NaH, Li3N, Na2C2.
4.Кристаллы некоторого вещества состоят из однозарядных ионов. В состав каждого иона входит по 18 электронов. Составьте а) простейшую формулу вещества; б) сокращенные электронные формулы ионов; в) уравнение одной из реакций получения этого вещества; г) два уравнения реакций с участием этого вещества.
Натрий и калий – важнейшие щелочные элементы.
Простые вещества, образуемые этими элементами, – мягкие легкоплавкие серебристые металлы, легко режутся ножом, быстро окисляются на воздухе. Хранят их под слоем керосина. Температура плавления натрия 98 °С, а калия 64 °С.
Оксиды этих элементов типичные основные оксиды. Они очень гигроскопичны: поглощая воду, превращаются в гидроксиды.
Гидроксиды натрия и калия – щелочи. Это твердые бесцветные кристаллические вещества, плавящиеся без разложения. Как и оксиды, они очень гигроскопичны: поглощая воду, превращаются в концентрированные растворы. Как твердые гидроксиды, так и их концентрированные растворы – очень опасные вещества: при попадании на кожу вызывают труднозаживающие язвы, вдыхание их пыли приводит к поражению дыхательных путей. Гидроксид натрия (тривиальные названия – едкий натр, каустическая сода) относится к важнейшим продуктам химической промышленности – с его помощью создается щелочная среда во многих химических производствах. Гидроксид калия (тривиальное название – «едкое кали») используют для производства других соединений калия.
Большинство средних солей натрия и калия термически устойчивые вещества и разлагаются только при очень высоких температурах. При умеренном нагревании разлагаются только соли галогенсодержащих оксокислот, нитраты и некоторые другие соединения:
NaClO4 = NaCl + 2O2 ;
8NaClO3 = 6NaClO4 + 2NaCl;
2NaNO3 = 2NaNO2 + O2 ;
Na2[Zn(OH)4] = Na2ZnO2 + 2H2O .
Кислые соли менее устойчивы, при нагревании все они разлагаются:
2NaHS = Na2S + H2S ;
2NaHSO4 = Na2S2O7 + H2O ;
2NaHCO3 = Na2CO3 + H2O + CO2 ;
NaH2PO4 = NaPO3 + H2O ;
Na2HPO4 = Na4P2O7 + H2O .
Основных солей эти элементы не образуют.
Из солей наибольшее значение имеет хлорид натрия – поваренная соль. Это не только необходимая составная часть пищи, но и сырье для химической промышленности. Из него получают гидроксид натрия, питьевую соду (NaHCO3), соду (Na2CO3) и многие другие соединения натрия. Соли калия – необходимые минеральные удобрения.
Почти все соли натрия и калия растворимы, поэтому доступных качественных реакций на ионы этих элементов не. (Качественными реакциями называют химические реакции, позволяющие обнаружить в соединении атомы или ионы какого-либо химического элемента, доказав при этом, что обнаружен именно эти атомы или ионы, а не какие-нибудь другие, похожие на них по химическим свойствам. Также называют реакции, позволяющие обнаружить какое-либо вещество в смеси) Определить наличие в соединении ионов натрия или калия можно по окрашиванию бесцветного пламени при внесении в него исследуемого образца: в случае натрия пламя окрашивается в желтый цвет, а в случае калия – в фиолетовый.

Простые вещества магний и кальций – металлы. Кальций быстро окисляется на воздухе, а магний в этих условиях значительно устойчивее – он окисляется лишь с поверхности. Кальций хранят под слоем керосина. Температуры плавления магния и кальция – 650 и 851 °С соответственно. Магний и кальций значительно более твердые вещества, чем щелочные металлы. Невысокая плотность магния (1,74 г/см 3 ) при значительной прочности дает возможность использовать его сплавы в авиационной промышленности.
И магний, и кальций – сильные восстановители (особенно при нагревании). Их часто используют для восстановления других, менее активных, металлов из их оксидов (магний – в лаборатории, а кальций – в промышленности).
Магний и кальций – одни из немногих металлов реагирующих с азотом. При нагревании они образует с ним нитриды Mg3N2 и Ca3N2. Поэтому, сгорая на воздухе, магний и кальций превращаются в смесь оксидов с нитридами.
Кальций легко реагирует с водой, а магний – только при кипячении. В обоих случаях выделяется водород и образуются малорастворимые гидроксиды.
Оксиды магния и кальция – ионные вещества; по химическому поведению они – основные оксиды. Оксид магния с водой не реагирует, а оксид кальция (тривиальное название – «негашеная известь») реагирует бурно с выделением теплоты. Образующийся гидроксид кальция в промышленности называют «гашеной известью».
Гидроксид магния нерастворим в воде, тем не менее он является основанием. Гидроксид кальция заметно растворим в воде; его насыщенный раствор называют «известковой водой», это щелочной раствор (изменяет окраску индикаторов). Гидроксид кальция в сухом, а особенно во влажном состоянии поглощает углекислый газ из окружающего воздуха и превращается в карбонат кальция. Это свойство гашеной извести много веков использовалось в строительстве: гашеная известь как основной компонент входила в состав строительных известковых растворов, в настоящее время почти полностью замененных цементными. Оба гидроксида при умеренном нагревании, не плавясь, разлагаются.
Соли магния и особенно кальция входят в состав многих породообразующих минералов. Из этих горных пород наиболее известны мел, мрамор и известняк, основным веществом которых является карбонат кальция. Карбонаты кальция и магния при нагревании разлагаются на соответствующие оксиды и углекислый газ. С водой, содержащей растворенный диоксид углерода, эти карбонаты реагируют, образуя растворы гидрокарбонатов, например:
MCO3 + CO2 + H2O = M 2 

При нагревании, и даже при попытке выделить гидрокарбонаты из раствора, удаляя воду при комнатной температуре, они разлагаются по обратной реакции:
M 2 

+ CO2
+ H2O.
Гидратированный сульфат кальция CaSO4·2H2O представляет собой бесцветное кристаллическое вещество малорастворимое в воде. При нагревании оно частично обезвоживается, переходя в кристаллогидрат состава 2CaSO4·H2O. Тривиальное название двуводного гидрата – гипс, а полуводного – алебастр. При смешивании алебастра с водой он гидратируется, при этом образуется плотная твердая масса гипса. Это свойство алебастра используется в медицине (гипсовые повязки) и строительстве (армированные гипсовые перегородки, заделка дефектов). Скульпторы используют алебастр для изготовления гипсовых моделей и форм.
Карбид (ацетиленид) кальция CaC2. Структурная формула (Ca 2 


CaO + 3C = CaC2 + CO
Это ионное вещество не является солью и полностью гидролизуется водой с образованием ацетилена, который долгое время и получали таким способом:
CaC2 + 2H2O = C2H2 + Ca(OH)2.
Гидратированный ион магния [Mg(H2O)6] 2 
Кальций в соединении может быть обнаружен по окрашиванию пламени. Цвет пламени – оранжево-красный. Качественная реакция на ионы Ca 2 


M 2 

.
2.Составьте уравнения всех реакций, приведенных параграфе описательно.
3.Составьте уравнения реакций, характеризующих химические свойства а) кальция, б) оксида кальция, в) гидроксида магния, г) карбоната кальция, д) хлорида магния.
Природная вода в той, или иной степени содержит ионы растворимых солей. Если в пресной воде суммарная концентрация ионов Mg 2 




При нагревании жесткой воды из нее выделяются карбонаты магния и кальция, а при кипячении – еще и сульфаты. Образующийся плотный осадок часто называют «накипью». Именно он появляется на внутренних поверхностях чайников. В промышленности этот осадок образуется на стенках котлов, снижая их теплопроводность, и трубопроводов, уменьшая их внутренний диаметр.
При стирке в жесткой воде с использованием мыла его расход сильно возрастает, а качество стирки снижается, так как из раствора мыла (натриевых солей некоторых органических кислот) выделяются нерастворимые кальциевые и магниевые соли. При использовании синтетических стиральных порошков этот эффект не наблюдается.
Различают временную (карбонатную) жесткость, устраняемую кипячением, и постоянную (некарбонатную), сохраняющуюся после кипячения воды.
Устранение жесткости заключается в удалении из нее ионов Mg 2 

Временная жесткость устраняется кипячением.
Для устранения общей жесткости в воду добавляют различные реагенты:
1. Гашеную известь Ca(OH)2.
Ca 2 


+ H2O
Mg 2 



+ CaCO3
+ 2H2O
Mg 2 

2. Соду Na2CO3.
M 2 

3. Фосфат натрия Na2PO4.
3M 2 
= M3(PO4)2
Фосфаты кальция и магния менее растворимы, чем карбонаты. Поэтому применение фосфата натрия приводит к более полному устранению жесткости.
Современный способ устранения жесткости основан на применении ионообменных смол (ионитов). Иониты представляют собой полимерные кислоты RHn (катиониты) и полимерные основания R(OH)n (аниониты).
При пропускании растворов солей через трубки (ионообменники), заполненные зернами ионитов, протекают реакции, называемые реакциями ионного обмена: катиониты как бы обменивают свои атомы водорода на катионы (отсюда и их название), а аниониты – гидроксильные группы на анионы:
RHn + (n/2)M 2 

R(OH)n + nA 

Последовательно пропуская жесткую воду через ионообменник, заполненный катионитом, и ионообменник, заполненный анионитом, жесткость можно устранить полностью.
Таким способом можно очистить не только жесткую, но и морскую воду, что иногда и делается для ее опреснения. В промышленности иониты используют для получения чистой (деионизированной) воды вместо дистиллированной.



Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору