какую роль играет кожа в процессе терморегуляции
Кожа как показатель здоровья человека
Защитная функция.
Наиболее важная роль в реализации защитных механизмов кожи принадлежит эпидермису. Барьерные свойства кожи, как органа механической защиты, обеспечиваются значительным электросопротивлением, прочностью коллагеновых и эластических волокон, упругой подкожной жировой клетчаткой. Компактный роговой слой и водно-липидная мантия предохраняют кожу от высыхания, многих химических и физических повреждающих воздействий, микробной флоры. Этому способствуют отторжение ороговевшего эпителия и выделения сальных и потовых желез. Кроме того, кожа обладает стерилизующими свойствами из-за кислой реакции водно-липидной мантии, а содержащиеся в ней низкомолекулярные жирные кислоты угнетающе действуют на рост патогенной флоры («собственный стерилизатор»).
Защита организма от повреждающего действия ультрафиолетовых лучей солнца осуществляется за счет утолщения рогового слоя и увеличения пигментация. Меланин поглощает видимый свет и ультрафиолетовые лучи во всем диапазоне.
Рецепторная функция.
Рецепторные функции кожи обеспечиваются множеством разнообразных чувствительных нервных окончаний и сенсорных телец, рассредоточенных по всему кожному покрову неравномерно. Существует тактильная (чувство осязания и давления), болевая и температурная (чувство холода и тепла) кожная чувствительность. Кожа непрерывно реагирует на разнообразные раздражения, поступающие из окружающей среды, из ЦНС и внутренних органов. Кожа является как бы экраном, на котором проецируются функциональные и органические изменения деятельности внутренних органов, ЦНС, эндокринной и иммунной систем. Нередко даже при небольшом расстройстве деятельности организма и его отдельных функций и систем в коже возникают изменения, позволяющие предположить ту или иную патологию.
Соблюдение правил гигиены кожи – это, в первую очередь, способ уберечь свое здоровье от воздействия внешних факторов окружающей среды. Очень многие заболевания проникают в наш организм через кожные покровы, и в наших силах предотвратить большинство из них.
Какую роль играет кожа в процессе терморегуляции
Регуляция теплообмена, а следовательно, и температуры тела человека осуществляется центром терморегуляции, который расположен в медиальной преоптической области переднего отдела гипоталамуса и в заднем отделе гипоталамуса. Разрушение этих отделов гипоталамуса или нарушение их нервных связей посредством перерезки на уровне среднего мозга в экспериментах на животных приводит к нарушению контроля за температурой тела у гомойотермных организмов. Кроме того, местное нагревание передней гипоталамической области вызывает усиление потоотделения и учащение дыхания у экспериментальных животных, охлаждение — возникновение дрожи и «свертывание в клубок». Регистрация активности отдельных нейронов гипоталамуса с помощью микроэлектродов показала ее изменение как в ответ на локальные колебания температуры в самом гипоталамусе, так и при воздействии раздражителей на терморецепторы кожи, внутренних органов и сосудов. Вышеперечисленные факты доказывают, что центр терморегуляции расположен в гипоталамусе.
В терморегуляторном центре гипоталамуса обнаружены различные по функциям группы нервных клеток:
1) термочувствительные нейроны преоптической области;
2) клетки, «задающие» уровень поддерживаемой в организме температуры тела («установочная точка» терморегуляции) в переднем гипоталамусе;
3) вставочные нейроны (интернейроны) гипоталамуса;
4) эффекторные нейроны, управляющие процессами теплопродукции и теплоотдачи, в заднем гипоталамусе (рис. 13.5).
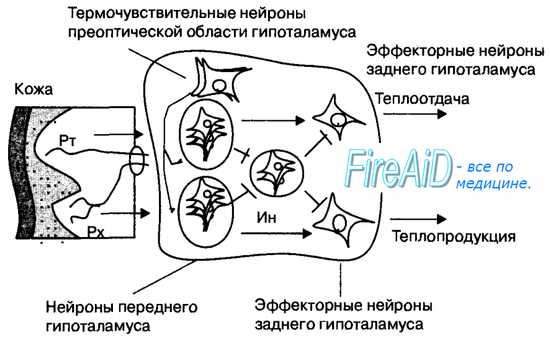
Термочувствительные нервные клетки преоптической области гипоталамуса непосредственно «измеряют» температуру артериальной крови, протекающей через мозг, и обладают высокой чувствительностью к температурным изменениям (способны различать разницу температуры крови в 0,011 °С). Отношение холодо- и теплочувствительных нейронов в гипоталамусе составляет 1:6, поэтому центральные терморецепторы преимущественно активируются при повышении температуры «ядра» тела человека. На основе анализа и интеграции информации о значении температуры крови и периферических тканей, в преоптической области гипоталамуса непрерывно определяется среднее (интегральное) значение температуры тела. Эти данные передаются через вставочные нейроны в группу нейронов переднего отдела гипоталамуса, задающих в организме определенный уровень температуры тела — «установочную точку» терморегуляции. На основе анализа и сравнений значений средней температуры тела и заданной величины температуры, подлежащей регулированию, механизмы «установочной точки» через эффекторные нейроны заднего гипоталамуса воздействуют на процессы теплоотдачи или теплопродукции, чтобы привести в соответствие фактическую и заданную температуру. Таким образом, за счет функции центра терморегуляции устанавливается равновесие между теплопродукцией и теплоотдачей, позволяющее поддерживать температуру тела в оптимальных для жизнедеятельности организма пределах (рис. 13.6).
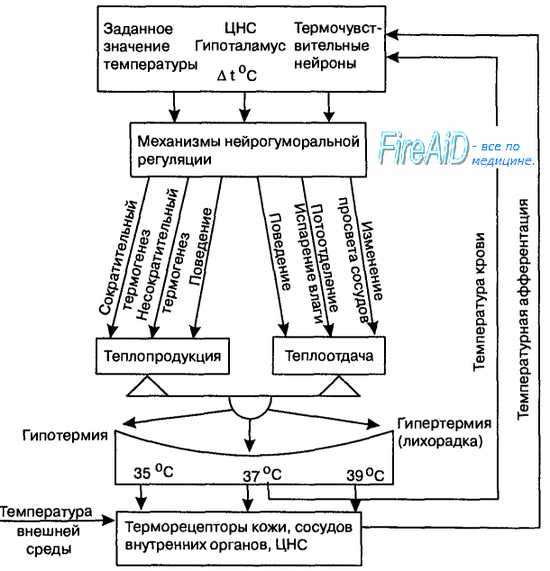
В механизме формирования «установочной точки» имеет значение уровень спонтанной активности вставочных нейронов гипоталамуса. Например, если уровень спонтанной активности интернейрона является высоким, то для усиления термогенеза требуется более высокая активность кожных Холодовых рецепторов, а значение пороговой температуры для регулируемой теплопродукции является более низким. И наоборот, если вставочный нейрон проявляет низкую спонтанную активность, то даже незначительная афферентация от кожных Холодовых рецепторов может оказаться достаточной для запуска дополнительного теплообразования в организме. Уровень спонтанной активности вставочных нейронов зависит от соотношения концентрации ионов натрия и кальция в гипоталамусе и некоторых других нетемпературных факторов.
Научная электронная библиотека
1.5 Особенности терморегуляции человека в условиях пониженных температур
В среде с низкой, некомфортной температурой незначительное снижение теплопотерь тела человека происходит за счет уменьшения градиента температуры между поверхностью тела и среды в результате охлаждения рецепторов кожи, спазмирования под влиянием этого кровеносных сосудов и увеличения термического сопротивления тканей организма. С течением времени постепенно происходит адаптация организма человека к пониженным температурам [28].
Низкие температуры окружающей среды оказывают влияние и на функционирование внутренних органов. При значительном охлаждении растет число тромбоцитов и эритроцитов в крови, увеличивается содержание холестерина, вязкость крови, что нарушает работу кровеносной системы и повышает возможность тромбообразования. Холод способствует возникновению различных сердечно-сосудистых патологий, приводит к вегетососудистой дистонии, обострению язвенной болезни, радикулита и ревматизма, обуславливает возникновение заболеваний органов дыхания: бронхита, пневмонии, тонзиллита [28, 41].
Внешнее проявление локального и общего охлаждения человека наблюдается как изменение его двигательной активности и реакции, нарушение общей координации и способности выполнять точные операции. Более глубокое воздействие холода на организм инициирует тормозные процессы в коре головного мозга, что может стать причиной возникновения различных форм травматизма. В результате, кроме потери здоровья человека, возрастают потери рабочего времени, связанные с временной утратой работоспособности.
При охлаждении человека для сохранения его работоспособности необходимо знать пределы переносимости холода организмом. На основании исследований теплообмена человека с окружающей средой [41] разработаны показатели допустимого теплового состояния человека (таблица 1.4).
Из таблицы видно, что увеличение физической активности способствует лучшей переносимости охлаждающего воздействия, несмотря на снижение средневзвешенной температуры кожи.
Таким образом, тепловое состояние человека определяется климатическими факторами, индивидуальными особенностями человека и теплозащитной одеждой. Диапазон возможной физиологической терморегуляции человека крайне ограничен, и защита его возможна лишь средствами специальной одежды. Обеспечение необходимого микроклимата в пододёжном слое и безопасного теплового состояния человека реализуется благодаря проектированию и созданию качественной и безопасной теплозащитной одежды.
Какую роль играет кожа в процессе терморегуляции
Анатомия и физиология кожи
Кожа – наш самый большой орган, составляющий 15% от общей массы тела. Она выполняет множество функций, прежде всего защищает организм от воздействия внешних факторов физической, химической и биологической природы, от потери воды, участвует в терморегуляции. Последние научные данные подтверждают, что кожа не только обладает собственной иммунной системой, но и сама является периферическим иммунном органом.
Структура кожи
Кожа состоит из 3 слоев: эпидермиса, дермы и подкожной жировой клетчатки (ПЖК) (рис. 1). Эпидермис – самый тонкий из них, представляет собой многослойный ороговевающий эпителий. Дерма – средний слой кожи. Главным образом состоит из фибрилл структурного белка коллагена. ПЖК содержит жировые клетки – адипоциты. Толщина этих слоев может значительно варьировать в зависимости от анатомического места расположения.
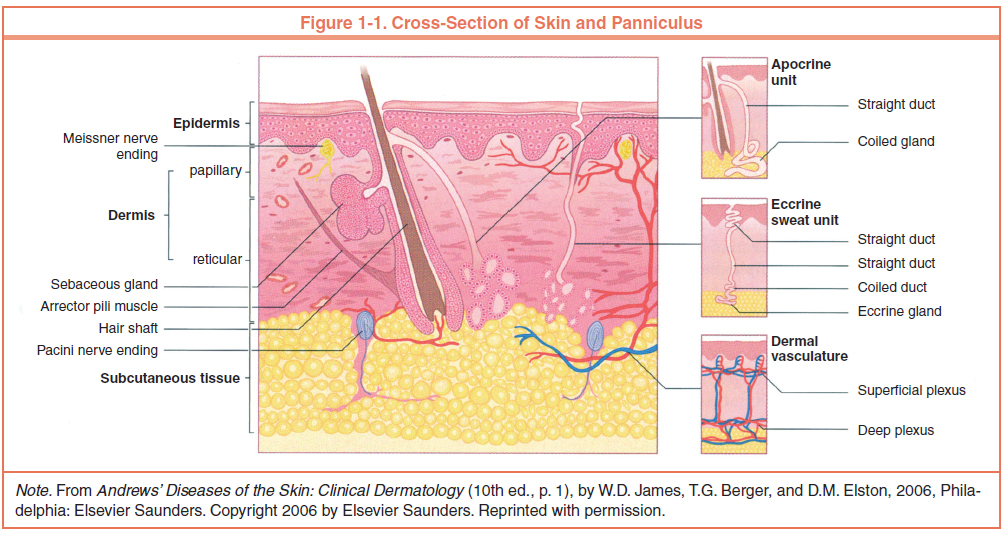
Эпидермис
Кератинизация. По мере дифференцировки кератиноцитов и продвижения от базального слоя до рогового происходит их кератинизация (ороговевание) – процесс, начинающийся с фазы синтеза кератина кератиноцитами и заканчивающийся их клеточной деградацией. Кератин служит строительным блоком для промежуточных филаментов. Пучки из этих филаментов, достигая цитоплазматический мембраны, формируют десмосомы, необходимые для образования прочных контактов между соседними клетками. Далее, по мере процесса эпителиальной дифференцировки, клетки эпидермиса вступают в фазу деградации. Ядра и цитоплазматические органеллы разрушаются и исчезают, обмен веществ прекращается, и наступаетапоптозклетки, когда она полностью кератинизируется (превращается в роговую чешуйку).
Базальный слой эпидермиса состоит из одного ряда митотически активных кератиноцитов, которые делятся в среднем каждые 24 часа и дают начало новым клеткам новым клеткам вышележащих эпидермальных слоев. Они активируются только в особых случаях, например при возникновении раны. Далее новая клетка, кератиноцит, выталкивается в шиповатый слой, в котором она проводит до 2 недель, постепенно приближаясь к гранулярному слою. Движение клетки до рогового слоя занимает еще 14 дней. Таким образом, время жизни кератиноцита составляет около 28 дней.
Надо заметить, что не все клетки базального слоя делятся с такой скоростью, как кератиноциты. Эпидермальные стволовые клетки в нормальных условиях образуют долгоживущую популяцию с медленным циклом пролиферации.
Шиповатый слой эпидермиса состоит из 5-10 слоев кератиноцитов, различающихся формой, структурой и внутриклеточным содержимым, что определяется положением клетки. Так, ближе к базальному слою, клетки имеют полиэдрическую форму и круглое ядро, но по мере приближения клеток к гранулярному слою они становятся крупнее, приобретают более плоскую форму, в них появляются ламеллярные гранулы, в избытке содержащие различные гидролитические ферменты. Клетки интенсивно синтезируют кератиновые нити, которые, собираясь в промежуточные филаменты, остаются не связанными со стороны ядра, но участвуют в образовании множественных десмосом со стороны мембраны, формируя связи с соседними клетками. Присутствие большого количества десмосом придает этому слою колючий вид, за что он и получил название «шиповатый».
Зернистый слой эпидермиса составляют еще живые кератиноциты, отличающиеся своей уплощенной формой и большим количеством кератогиалиновых гранул. Последние отвечают за синтез и модификацию белков, участвующих в кератинизации. Гранулярный слой является самым кератогенным слоем эпидермиса. Кроме кератогиалиновых гранул кератиноциты этого слоя содержат в большом количестве лизосомальные гранулы. Их ферменты расщепляют клеточные органеллы в процессе перехода кератиноцита в фазу терминальной дифференцировки и последующего апоптоза. Толщина гранулярного слоя может варьировать, ее величина, пропорциональная толщине вышележащего рогового слоя, максимальна в коже ладоней и подошв стоп.
Блестящий слой эпидермиса (назван так за особый блеск при просмотре препаратов кожи на световом микроскопе) тонкий, состоит из плоских кератиноцитов, в которых полностью разрушены ядра и органеллы. Клетки наполнены элейдином – промежуточной формой кератина. Хорошо развит лишь на некоторых участках тела – на ладонях и подошвах.
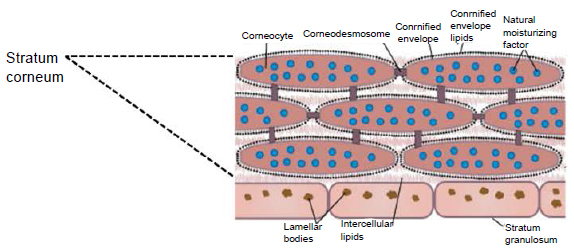
Роговой слой эпидермиса представлен корнеоцитами (мертвыми, терминально-дифференцированными кератиноцитами) с высоким содержанием белка. Клетки окружены водонепроницаемым липидным матриксом, компоненты которого содержат соединения, необходимые для отшелушивания рогового слоя (рис. 3). Физические и биохимические свойства клеток в роговом слое различаются в зависимости от положения клетки внутри слоя, направляя процесс отшелушивания наружу. Например, клетки в средних слоях рогового слоя обладают более сильными водосвязывающими свойствами за счет высокой концентрации свободных аминокислот в их цитоплазме.
Дерма
Дерма представляет собой сложноорганизованную рыхлую соединительную ткань, состоящую из отдельных волокон, клеток, сети сосудов и нервных окончаний, а также эпидермальных выростов, окружающих волосяные фолликулы и сальные железы. Клеточные элементы дермы представлены фибробластами, макрофагами и тучными клетками. Лимфоциты, лейкоциты и другие клетки способны мигрировать в дерму в ответ на различные стимулы.
Дерма, составляя основной объем кожи, выполняет преимущественно трофическую и опорную функции, обеспечивая коже такие механические свойства, как пластичность, эластичность и прочность, необходимые ей для защиты внутренних органов тела от механических повреждений. Также дерма удерживает воду, участвует в терморегуляции и содержит механорецепторы. И, наконец, ее взаимодействие с эпидермисом поддерживает нормальное функционирование этих слоев кожи.
В дерме нет такого направленного и структурированного процесса клеточной дифференцировки, как в эпидермисе, тем не менее в ней также прослеживается четкая структурная организация элементов в зависимости от глубины их залегания. И клетки, и внеклеточный матрикс дермы также подвергаются постоянному обновлению и ремоделированию.
Коллаген – один из главных компонентов ВКМ дермы. Синтезируется фибробластами. Процесс его биосинтеза сложный и многоступенчатый, в результате которого фибробласт секретирует в экстрацеллюлярное пространство проколлаген, состоящий из трех полипептидных α-цепей, свернутых в одну тройную спираль. Затем мономеры проколлагена ферментивным путем собираются в протяженные фибриллярные структуры различного типа. Всего в коже не менее 15 типов коллагена, в дерме больше всего I, III и V типов этого белка: 88, 10 и 2% соответственно. Коллаген IV типа локализуется в зоне базальной мембраны, а коллаген VII типа, секретируемый кератиноцитами, играет роль адаптерного белка для закрепления фибрилл ВКМ на базальной мембране (рис. 4). Волокна структурных коллагенов I, III и V типов служат каркасом, к которому присоединяются другие белки ВКМ, в частности коллагены XII и XIV типов. Считается, что эти минорные коллагены, а также небольшие протеогликаны (декорин, фибромодулин и люмикан) регулируют формирование структурных коллагеновых волокон, их диаметр и плотность образуемой сети. Взаимодействие олигомерных и полимерных комплексов коллагена с другими белками, полисахаридами ВКМ, разнообразными факторами роста и цитокинами приводит к образованию особой сети, обладающей определенной биологической активностью, стабильностью и биофизическими характеристиками, важными для нормального функционирования кожи. В папиллярном слое дермы волокна коллагена располагаются рыхло и более свободно, тогда как ее ретикулярный слой содержит более крупные тяжи коллагеновых волокон.
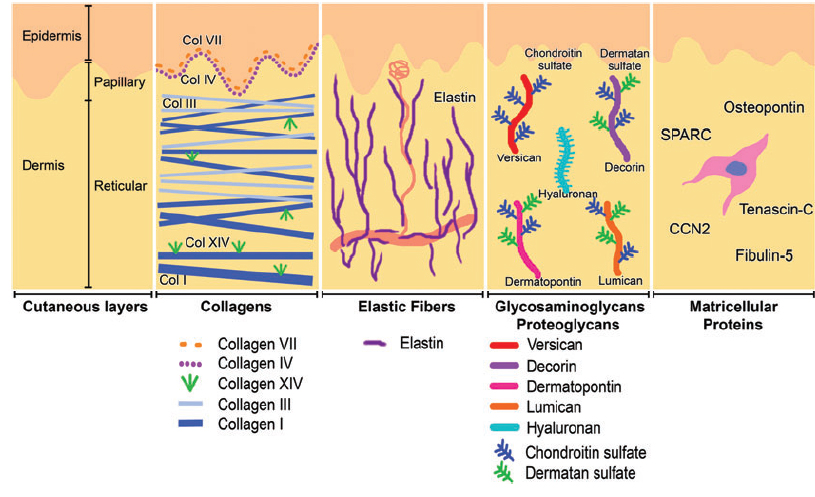
Коллаген постоянно обновляется, деградируя под действием протеолитических ферментов коллагеназ и замещаясь вновь синтезированными волокнами. Этот белок составляет 70% сухого веса кожи. Именно коллагеновые волокна «держат удар» при механическом воздействии на нее.
Эластин формирует еще одну сеть волокон в дерме, наделяя кожу такими качествами, как упругость и эластичность. По сравнению с коллагеном эластиновые волокна менее жесткие, они скручиваются вокруг коллагеновых волокон. Именно с эластиновыми волокнами связываются такие белки, как фибулины и фибриллины, с которыми, в свою очередь, связывается латентный TGF-β-связывающий белок (LTBP). Диссоциация этого комплекса приводит к высвобождению и к активации TGF-β, самого мощного из всех факторов роста. Он контролирует экспрессию, отложение и распределение коллагенов и других матриксных белков кожи. Таким образом, интактная сеть из волокон эластина служит депо для TGF-β.
ГК с легкостью образует вторичные водородные связи и внутри одной молекулы, и между соседними молекулами. В первом случае они обеспечивают формирование относительно жестких спиральных структур. Во втором – происходит ассоциация с другими молекулами ГК и неспецифическое взаимодействие с клеточными мембранами, что приводит к образованию сети из полимеров полисахаридов с включенными в нее фибробластами. На длинную молекулу ГК, как на нить, «усаживаются» более короткие молекулы протеогликанов (версикана, люмикана, декорина и др.), формируя агрегаты огромных размеров. Протяженные во всех направлениях, они создают каркас, внося вклад в стабилизацию белковой сети ВКМ и фиксируя фибробласты в определенном окружении матрикса. В совокупности все эти свойства ГК наделяют матрикс определенными химическими характеристиками – вязкостью, плотностью «ячеек» и стабильностью. Однако сеть ВКМ является динамической структурой, зависящей от состояния организма. Например, в условиях воспаления агрегаты ГК с протеогликанами диссоциируют, а образование новых агрегатов между вновь синтезированными молекулами ГК (обновляющимися каждые 3 дня) и протеогликанами блокируется. Это приводит к изменению пространственной структуры матрикса: увеличивается размер его ячеек, меняется распределение всех волокон, структура становится более рыхлой, клетки меняют свою форму и функциональную активность. Все это сказывается на состоянии кожи, приводя к снижению ее тонуса.
Помимо регуляции водного баланса и стабилизации ВКМ, ГК выполняет важную регуляторную роль в поддержании эпидермального и дермального гомеостаза. ГК активно регулирует динамические процессы в эпидермисе, включая пролиферацию и дифференцировку кератиноцитов, окислительный стресс и воспалительный ответ, поддержание эпидермального барьера и заживление раны. В дерме ГК также регулирует активность фибробластов и синтез коллагена. Ремоделируя матрикс, ГК управляет функционированием клеток в матриксе, влияя на их доступность для различных факторов роста и изменяя их функциональную активности. От действия ГК зависит миграция клеток и иммунный ответ в ткани. Таким образом, изменения в распределении, организации, молекулярном весе и метаболизме ГК имеют значимые физиологические последствия.
Фибробласты представляют собой основной тип клеточных элементов дермы. Именно эти клетки отвечают за продукцию ГК, коллагена, эластина, фибронектина и многих других белков межклеточного матрикса, необходимых для формирования соединительной ткани. Фибробласты в различных слоях дермы различаются и морфологически, и функционально. От глубины их залегания в дерме зависит не только количество синтезируемого ими коллагена, но и соотношение типов этого коллагена, например I и III типов, а также синтез коллагеназы: фибробласты более глубоких слоев дермы производят меньшее ее количество. Вообще, фибробласты – очень пластичные клетки, способные менять свои функции и физиологический ответ и даже дифференцироваться в другой тип клеток в зависимости от полученного стимула. В роли последнего могут выступать и сигнальные молекулы, синтезированные соседними клетками, и перестройка окружающего ВКМ.
Подкожно-жировая клетчатка
Нарушение терморегуляции организма
Общие сведения
Расстройство терморегуляции это нарушение постоянства температуры тела, вызванные дисфункцией ЦНС. Температурный гомеостаз считается одной из основных функций гипоталамуса, который содержит специализированные термочувствительные нейроны.
От гипоталамуса начинаются вегетативные пути, которые при необходимости могут обеспечивать увеличение теплопродукции, вызывая мышечную дрожь или рассеяние излишнего тепла.
При поражении гипоталамуса, а также следующих от него к стволу мозга или спинному мозгу путей возникают расстройства терморегуляции в виде гипертермии или гипотермии.
Теплоотдача организмом во внешнюю среду зависит от температуры окружающей среды, от количества влаги (пота), выделяемой организмом вследствие затрат тепла на испарение, от тяжести выполняемой работы и физического состояния человека.
При высокой температуре воздуха и облучении кровеносные сосуды поверхности тела расширяются, при этом происходит перемещение крови: главного аккумулятора тепла в организме, к периферии (поверхности тела). Вследствие такого перераспределения крови теплоотдача с поверхности тела значительно увеличивается.
Нарушения терморегуляции организма могут возникать при:
повреждении центрального или периферического звена системы терморегуляции;
кровоизлияниях и опухолях в области гипоталамуса;
при травмах, сопровождающихся повреждением соответствующих проводящих путей.
Нарушение терморегуляции сопутствует многим системным заболеваниям, обычно проявляясь повышением температуры тела или лихорадкой. Повышение температуры тела является настолько надежным индикатором заболевания, что наиболее часто используемой в клинике процедурой стала термометрия.
Изменения температуры можно выявить даже при отсутствии явного фебрилитета. Они проявляются в виде покраснения, побледнения, потоотделения, дрожи, ненормальных ощущений тепла или холода, а также могут состоять из неустойчивых колебаний температуры тела в пределах нормы у больных с постельным режимом.
При физической работе временно нарушается баланс между теплопродукцией и теплоотдачей с последующим быстрым восстановлением нормальной температуры в состоянии покоя за счет длительной активации механизмов теплоотдачи.
Фактически, при длительной физической нагрузке расширение сосудов кожи в ответ на повышение температуры сердцевины организма прекращается для того, чтобы сохранить эту температуру.
Нарушение терморегуляции при лихорадке
При лихорадке адаптационная способность снижается, так как по достижении стабильной температуры тела теплопродукция становится равной теплоотдаче, однако и та, и другая находятся на уровне выше исходного. Кровоток в периферических сосудах кожи играет более важную роль в регуляции теплопродукции и теплоотдачи, чем потоотделение.
При лихорадке температура тела, определяемая терморецепторами, низкая, поэтому организм реагирует на нее как на охлаждение.
Дрожь приводит к увеличению теплопродукции, а сужение сосудов кожи — к уменьшению теплоотдачи. Эти процессы позволяют объяснить возникающие в начале лихорадки ощущения холода или озноба. И наоборот, при удалении причины лихорадки температура снижается до нормальной, и больной ощущает жар. Компенсаторными реакциями в данном случае являются:
расширение сосудов кожи;
При высокой температуре окружающей среды развиваются четыре клинических синдрома:
тепловая травма при напряжении;
Каждое из этих состояний можно отдифференцировать на основании различных клинических проявлений, однако между ними есть много общего и эти состояния можно рассматривать как разновидности синдромов одного и того же происхождения.
Симптомокомплекс теплового поражения развивается при высокой температуре (более 32°С) и при высокой относительной влажности воздуха (более 60%). Наиболее уязвимы люди пожилого возраста, лица, страдающие психическими заболеваниями, алкоголизмом, принимающие антипсихотические, мочегонные, антихолинергические препараты, а также люди, находящиеся в помещениях с плохой вентиляцией.
