холицистоз печени что это
Холестаз: симптомы и лечение холестатического синдрома
Холестаз – клинико-лабораторный синдром, при котором нарушена выработка желчи или полностью либо частично блокирован ее отток в двенадцатиперстную кишку.
Состояние может быть вызвано различными заболеваниями. Оно характеризуется накоплением в крови выводимых с желчью веществ, что сопровождается кожным зудом, слабостью, желтухой и другими проявлениями.
Диагностика патологии основана преимущественно на данных анализов, а также инструментальных методов исследования.
Лечение холестатического синдрома включает прием медикаментов, диету и в ряде случаев хирургическое вмешательство на органах печени и желчевыводящих путей.
Распространенность и особенности холестаза
По данным статистики, этой патологией страдает 1 человек на 10 тысяч населения планеты в год. При этом около 50-70% людей с заболеваниями печени и желчных путей (даже пролеченных ранее) может столкнуться в той или иной степени с холестазом в разные периоды жизни.
Большая часть заболевших мужского пола, в возрасте старше 40 лет. Среди беременных женщин состояние выявляется от 0,2 до 27% среди обследованных, в зависимости от региона и дополнительных заболеваний и состояний.
Причины и виды холестатического синдрома
Существует две основные формы патологии – внепеченочная и внутрипеченочная. Первая развивается в случае полной или частичной закупорки желчных протоков, чаще всего камнями при желчнокаменной болезни и холедохолитиазе, а также при опухоли органов гепатобилиарной системы, дисфункции сфинктера Одди, описторхоза, врожденных аномалий желчевыводящих путей.
Внутрипеченочный холестаз – следствие заболеваний гепатоцеллюлярной системы, таких как гепатиты вирусного, алкогольного и медикаментозного происхождения, жировая болезнь печени (довольно частая патология современного человека, поражающая до 20% людей и более, в зависимости от возраста и массы тела) и ее аутоиммунные поражения, дефекты внутрипеченочных протоков.
Среди частых причин патологии также врожденные метаболические нарушения (галактоземия, муковисцидоз и другие), саркоидоз, изменения гормонального фона, например, при беременности.
Проявления застоя желчи
Холестаз у беременных женщин и детей
Отдельного внимания заслуживают такие формы патологии, как холестаз во время вынашивания плода и в детском возрасте. В этих случаях механизм развития нарушений и симптомы имеют свои особенности.
Проявления холестаза у беременных наблюдаются в третьем триместре. Кожный зуд может быть ярко выраженным или практически не доставлять дискомфорта. Расчесы чаще отмечаются на руках, голенях, предплечьях. Желтуха встречается лишь у одной из десяти женщин и, как правило, проходит самостоятельно через две недели после родов. Однако при выраженной желтухе и раннем начале (до 25-27-й недели беременности) может повышать риск осложнений в родах.
Детский холестаз может наблюдаться как с первых месяцев жизни, так и появиться в более старшем возрасте. В младенчестве чаще встречаются внутрипеченочный холестатический синдром, вызванный врожденными метаболическими нарушениями, идиопатический неонатальный гепатит и пороки развития желчных протоков. Причинами холестаза могут быть также инфекции, токсические поражения органов, цирроз печени, сердечно-сосудистая недостаточность, опухоли поджелудочной железы, паразитарные поражения, склерозирующий холангит.
Опасность холестаза в том, что он развивается у детей в скрытой форме. Симптоматика зависит от возраста, в котором проявилось заболевание, и особенностей организма.
Диагностика патологии
Диагностику и лечение синдрома холестаза проводит врач-гастроэнтеролог. Некоторые пациенты ошибочно консультируются с дерматологом, акцентируя внимание только на кожном зуде и не принимая во внимание прочие симптомы.
Заподозрить патологию врачу позволяют беседа с больным, внешний осмотр кожи и слизистых пациента. Пальпация и перкуссия часто позволяют выявить увеличение печени в размерах, болезненные области. Нередко холестатический синдром протекает почти бессимптомно, и на его наличие указывают только лабораторные анализы. Они заключаются в определении уровня билирубина, холестерина, щелочной фосфатазы, ферментов и желчных кислот в крови, желчных пигментов в моче.
Для общего анализа крови при холестазе характерны анемия, лейкоцитоз, завышенные значения СОЭ. В биохимическом анализе крови выявляются гипербилирубинемия (за счет прямого (конъюгированного) билирубина), гиперлипидемия, повышение активности ферментов, таких как аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), щелочная фосфатаза (ЩФ), гаммаглутамилтранспептидаза (ГГТП). Обнаружение антимитохондриальных, антинуклеарных антител и антител к гладкомышечным клеткам позволяет заподозрить аутоиммунное поражение печени как возможную причину холестаза.
Инструментальная диагностика холестаза предполагает ультразвуковое и рентгеновское исследования органов брюшной полости, гастро- и дуоденоскопию, магнитно-резонансную или эндоскопическую ретроградную холангиопанкреатографию, чрескожную чреспеченочную холангиографию. Диагноз может быть установлен на любом этапе, даже просто после выполнения лабораторных анализов и УЗИ, не все вышеперечисленные исследования обязательно потребуются для диагностики.
Если результаты проведенных обследований сомнительны, то прибегают к биопсии печени (которая также может быть назначена на любом этапе диагностического поиска).
Лечение холестаза
Первая мера при выявлении холестаза или подозрении на него – коррекция питания. Особенностью такой диеты является замена животных жиров на растительные. Рекомендуется употреблять больше овощей и фруктов, выбирать нежирные сорта мяса и виды молочных продуктов. Полезны также каши на основе злаковых культур. Нужно ограничить жареные, копченые и острые продукты. Следует полностью отказаться от спиртного, крепкого кофе и чая.
Лечение беременных осложняется рисками для плода при применении лекарств, потому для уменьшения симптоматики прибегают в первую очередь к простым и безопасным средствам – маски из овсяных хлопьев, отвар ромашки, использованию детского крема.
Холодная вода и сон в прохладном помещении облегчают кожный зуд. Однако при его усилении врачом могут быть назначены препараты желчных кислот, разрешенные к применению у беременных (в частности – урсодезоксихолевая кислота). Эти препараты определены американской Food and Drug Administration (FDA) на основании проведенных клинических исследований. Препараты, по которым накоплено достаточно данных о применении их у беременных, отнесены данной организацией к соответствующей группе (категории действия на плод).
Для успешного лечения холестаза у детей важно своевременно установить причину данного синдрома. Часто одними лекарствами патологию у этой группы больных не вылечить, тогда проводят хирургическую операцию.
Актуальные вопросы терапии хронического некалькулезного холецистита
Хронический холецистит — воспалительное заболевание желчного пузыря, сочетающееся с функциональными нарушениями и изменениями физико-химических свойств желчи.
Хронический холецистит — воспалительное заболевание желчного пузыря, сочетающееся с функциональными нарушениями (дискинезиями желчного пузыря и сфинктерного аппарата желчевыводящих путей) и изменениями физико-химических свойств желчи (дисхолией).
По данным различных авторов, больные хроническим холециститом составляют 17–19%, в индустриально развитых странах — до 20%.
Классификация
Согласно МКБ-10 выделяют:
Клиника
В клинике преобладает болевой синдром, который возникает в области правого подреберья, реже — в подложечной области. Боль иррадиирует в правую лопатку, ключицу, плечевой сустав, имеет ноющий характер, продолжается в течение многих часов, дней, иногда недель. Нередко на этом фоне возникает острая схваткообразная боль, обусловленная обострением воспаления в желчном пузыре. Возникновение боли и ее усиление чаще связано с нарушением диеты, физическим напряжением, охлаждением, интеркуррентной инфекцией. Обострению болевого приступа обычно сопутствуют повышение температуры тела, тошнота, рвота, отрыжка, понос или чередование поносов и запоров, вздутие живота, чувство горечи во рту.
Рвота — необязательный симптом хронического бескаменного холецистита и наряду с другими диспепсическими расстройствами (тошнота, отрыжка горечью или постоянный горький вкус во рту) может быть связана не только с основным заболеванием, но и с сопутствующей патологией — гастритом, панкреатитом, перидуоденитом, гепатитом. Часто в рвотных массах обнаруживают примесь желчи, при этом они окрашиваются в зеленый или желто-зеленый цвет.
Наблюдаются вялость, раздражительность, нарушение сна. Преходящая желтушная окраска склер и кожных покровов может наблюдаться в связи с затруднением оттока желчи из-за скопления слизи, эпителия или паразитов (в частности, лямблий) в холедохе.
При пальпации живота у больных хроническим холециститом определяются следующие симптомы.
Симптом Кера — в области проекции желчного пузыря, расположенной у места пересечения наружного края правой прямой мышцы живота с краем ложных ребер, появляется болезненность при глубокой пальпации во время вдоха.
Симптом Грекова–Ортнера–Рашбы — болезненность при поколачивании ребром кисти по правой реберной дуге.
Симптом Мерфи — осторожное, мягкое введение руки в зону желчного пузыря, и при глубоком вдохе пальпирующая рука вызывает резкую болезненность.
Симптом Мюсси — болезненность при надавливании на диафрагмальный нерв между ножками грудинно-ключично-сосцевидной мышцы справа.
Инструментальные и клинико-биохимические исследования
При хроническом холецистите в фазе обострения повышается СОЭ, возрастает количество лейкоцитов со сдвигом формулы влево, эозинофилия.
К рентгенологическим методам исследования относят холеграфию, которую проводят после перорального или внутривенного введения контрастного вещества. На снимках выявляются симптомы поражения желчного пузыря: удлинение, извитость, неравномерность заполнения (фрагментированность) пузырного протока, его перегибы.
В последние годы стали использовать комплексную методику, в которую, кроме холеграфии, включают холецистохолангиографию, ультразвуковое и радионуклидное сканирование, компьютерную томографию, лапароскопию. В ряде случаев по особым показаниям проводят лапароскопическую холецистографию. Применение этого метода позволяет просмотреть различные отделы желчного пузыря, отметить степень его наполнения, наличие спаек и сращений, деформаций, состояние стенки.
К неинвазивным методам исследования желчевыводящих путей относят ультразвуковое исследование (УЗИ).
УЗИ не имеет противопоказаний и может применяться в тех случаях, когда рентгенологическое исследование не может быть проведено: в острую фазу заболевания, при повышенной чувствительности к контрастным веществам, беременности, печеночной недостаточности, обструкции магистральных желчных путей или пузырного протока. УЗИ позволяет не только установить отсутствие конкрементов, но и оценить сократительную способность и состояние стенки желчного пузыря (утолщение, склерозирование).
Лечение
Режим
В период выраженного обострения больных нужно госпитализировать. При сильном болевом синдроме, особенно возникшем впервые или осложнившемся механической желтухой, угрозе развития деструктивного холецистита больных следует направлять в хирургическое отделение. При легком течении заболевания лечение проводят амбулаторно.
В период обострения больному рекомендуется постельный режим в течение 7–10 дней. Очень важно состояние психоэмоционального комфорта, особенно при гипертонической дискинезии желчевыводящих путей. При гипокинетической дискинезии постельный режим не рекомендуется.
Питание
В фазе обострения в первые 1–2 дня назначается питье теплой жидкости (некрепкий сладкий чай, соки из фруктов и ягод, разведенные водой, отвар шиповника, минеральная вода без газа) небольшими порциями до 6 стаканов в день, несколько сухариков. По мере улучшения состояния назначается в ограниченном количестве протертая пища: слизистые супы (овсяный, рисовый, манный), каши (манная, овсяная, рисовая), кисели, желе, муссы. Далее включается нежирный творог, нежирная отварная рыба, протертое мясо, белые сухари. Пища принимается 5–6 раз в день.
Многие специалисты рекомендуют в периоде обострения хронического холецистита 1–2 разгрузочных дня. Например:
После купирования обострения назначается диета № 5. Она содержит нормальное количество белков (90–100 г); жиров (80–100 г), около 50% жиров составляют растительные масла; углеводов (400 г), энергетическая ценность 2500–2900 ккал.
Питание дробное (небольшими порциями) и частое (5–6 раз в сутки), что способствует лучшему оттоку желчи.
При хронических холециститах полезны растительные жиры, масла. Они богаты полиненасыщенными жирными кислотами, фосфолипидами, витамином Е. Полиненасыщенные жирные кислоты (ПНЖК) (арахидоновая, линолевая) входят в состав клеточных мембран, способствуют нормализации обмена холестерина, участвуют в синтезе простагландинов, которые разжижают желчь, повышают сократительную способность желчного пузыря. Растительные жиры особенно важны при застое желчи.
Установлено антилитогенное свойство диеты, богатой растительной клетчаткой (яблоки, морковь, арбуз, дыня, помидоры). Целесообразно добавлять к пище пшеничные отруби — до 30 г в сутки. Их обдают кипятком, запаривают; затем жидкость сливают, разбухшие отруби добавляют в блюда по 1–2 столовых ложки 3 раза в день. Курс лечения — 4–6 недель. Овощи, фрукты, отруби способствуют отхождению желчи, уменьшают содержание в ней холестерина, снижают вероятность образования камней.
При гипертонусе желчного пузыря для уменьшения тонуса гладкой мускулатуры назначается диета, богатая магнием (пшеничная и гречневая каши, пшеничные отруби, пшено, хлеб, овощи).
Больным хроническим холециститом не рекомендуются продукты, оказывающие раздражающее действие на печень: мясные бульоны, животные жиры (кроме сливочного масла), яичные желтки, острые приправы (уксус, перец, горчица, хрен), жареные и тушеные блюда, изделия из сдобного теста. Запрещаются алкогольные напитки и пиво.
Купирование болевого синдрома в периоде обострения
При интенсивных болях в правом подреберье, тошноте и повторной рвоте назначают периферические М-холинолитики: 1 мл 0,1% раствора Атропина сульфата или 1 мл 0,2% раствора Платифиллина п/к. Они оказывают и противорвотное действие, уменьшают секрецию поджелудочной железы, кислото- и ферментообразование в желудке.
После купирования интенсивных болей препараты могут быть назначены внутрь: Метацин в дозе 0,004–0,006 г, Платифиллин — по 0,005 г на прием. При наличии противопоказаний можно рекомендовать селективный М-холинолитик Гастроцепин внутрь по 50 мг 2–3 раза в день.
Для купирования боли применяются также миотропные спазмолитики: 2 мл 2% раствора Папаверина гидрохлорида, 2 мл 2% раствора Но-шпы п/к или в/м 2–3 раза в день, 2 мл 0,25% раствора Феникаберана в/м. В начале приступа желчной колики боль может купироваться приемом 0,005 г Нитроглицерина под язык.
При наличии у больного гипотонической дискинезии (монотонные тупые, ноющие боли, ощущение тяжести в правом подреберье) холинолитики и спазмолитики не показаны.
В этих случаях можно рекомендовать холекинетики (повышают тонус желчного пузыря, способствуют его опорожнению, уменьшают боль в правом подреберье): растительное масло по 1 столовой ложке 3 раза в день перед едой, ксилит или сорбит по 15–20 г на 1/2 стакана теплой воды 2–3 раза в день, 25% раствор магния сульфата по 1 столовой ложке 2–3 раза в день перед едой.
С этой же целью применяется синтетический гормональный препарат — холецистокинин октапептид (интраназально по 50–100 мкг), он дает и обезболивающий эффект.
При выраженном болевом синдроме у больного с гипотонической дискинезией целесообразно использовать ненаркотические анальгетики, а в дальнейшем — холекинетики.
Регулирующим влиянием на тонус желчевыводящих путей и противорвотным действием обладают метоклопрамид (Церукал) и домперидон (Мотилиум), который можно применять внутрь или в/м по 10 мг 2–3 раза в день.
Антибактериальная терапия (АБТ) в период обострения
АБТ назначается тогда, когда есть основания предполагать бактериальную природу заболевания (лихорадка, лейкоцитоз и др.).
Naumnan (1967) назвал свойства «идеального антибиотика» для лечения инфекции желчного пузыря и желчных путей:
Антибактериальные препараты, проникающие в желчь в очень высоких концентрациях
По данным Я. С. Циммермана, наибольшей концентрации в желчи достигают ампициллин и рифампицин. Это антибиотики широкого спектра действия, они оказывают влияние на большинство возбудителей холецистита.
Ампициллин — относится к полусинтетическим пенициллинам, подавляет активность ряда грамотрицательных (кишечная палочка, энтерококки, протей) и грамположительных бактерий (стафилококки и стрептококки). Хорошо проникает в желчные пути даже при холестазе, назначается внутрь по 0,5 г 4 раза в день или в/м по 0,5–1,0 г каждые 6 ч.
Оксациллин — полусинтетический пенициллин, оказывает бактерицидное действие преимущественно на грамположительную флору (стафилококк, стрептококк), но неэффективен в отношении большинства грамотрицательных бактерий. В отличие от пенициллина действует на пенициллиназообразующие стафилококки. Хорошо накапливается в желчи и назначается внутрь по 0,5 г 4–6 раз в день до еды или по 0,5 г 4–6 раз в день внутримышечно.
Оксамп (ампициллин + оксациллин) — препарат бактерицидного действия широкого спектра, подавляет активность пенициллиназообразующих стафилококков. Создает в желчи высокую концентрацию. Назначается по 0,5 г 4 раза в день внутрь или в/м.
Рифампицин — полусинтетический бактерицидный антибиотик широкого спектра действия. Рифампицин не разрушается пенициллиназой, но в отличие от ампициллина не проникает в желчные пути при застойных явлениях в них. Препарат принимается внутрь по 0,15 3 раза в день.
Эритромицин — антибиотик из группы макролидов, активен в отношении грамположительных бактерий, слабо влияет на грамотрицательные микроорганизмы, создает высокие концентрации в желчи. Назначается по 0,25 г 4 раза в день.
Линкомицин — бактериостатический препарат, влияющий на грамположительную флору, в том числе на пенициллиназообразующие стафилококки, и неактивный в отношении грамотрицательных микроорганизмов. Назначается внутрь по 0,5 г 3 раза в день за 1–2 ч до еды или внутримышечно по 2 мл 30% раствора 2–3 раза в день.
Препараты, проникающие в желчь в достаточно высоких концентрациях
Пенициллин (бензилпенициллин-натрий) — бактерицидный препарат, активный в отношении грамположительной флоры и некоторых грамотрицательных кокков, на большинство грамотрицательных микроорганизмов не действует. Не активен в отношении пенициллиназообразующих стафилококков. Назначается в/м по 500 000–1 000 000 ЕД 4 раза в сутки.
Феноксиметилпенициллин — назначается внутрь по 0,25 г 6 раз в сутки до еды.
Тетрациклины — обладают бактериостатическим действием как на грамположительную, так и на грамотрицательную флору. Назначаются внутрь по 0,25 г 4 раза в день.
Высокоэффективны полусинтетические производные тетрациклина. Метациклин принимают в капсулах по 0,3 г 2 раза в день. Доксициклин назначается внутрь в 1-й день по 0,1 г 2 раза в день, затем по 0,1 г 1 раз в день.
Антибиотики группы цефалоспоринов
Применяются цефалоспорины I поколения — цефалоридин (Цепорин), цефалотин (Кефлин), цефазолин (Кефзол); II поколения — цефалексин (Цепорекс), цефуроксим (Кетоцеф), цефамандол (Мандол); III поколения — цефотаксим (Клафоран), цефтриаксон (Лонгацеф), цефтазидим (Фортум).
Препараты I поколения угнетают большинство стафилококков, стрептококков, многие штаммы кишечной палочки, протея.
Цефалоспорины II поколения обладают более широким спектром действия на грамотрицательные бактерии, угнетают резистентные к препаратам I поколения кишечные палочки, различные энтеробактерии.
Еще более широким спектром действия обладают цефалоспорины III поколения, они подавляют, кроме перечисленных бактерий, сальмонеллы, шигеллы.
Кефзол — вводится в/м или в/в по 0,5–1 г каждые 8 ч. Цепорин — вводится в/м по 0,5–1 г каждые 8 ч. Клафоран — вводится в/м или в/в по 2 г 2 раза в день.
Препараты фторхинолонов
Обладают бактерицидными свойствами, препараты широкого спектра действия, достаточно хорошо проникающие в желчь. Назначаются при тяжелой инфекции желчевыводящих путей.
Абактал (пефлоксацин) — назначается внутрь по 0,4 г 2 раза в день во время еды или в/в капельно — 5 мл (0,4 г) в 250 мл 5% раствора глюкозы.
Таривид (офлоксацин) — назначается по 0,2 г 2 раза в день.
Ципролет (ципрофлоксацин) — назначается по 0,5 г 2 раза в день.
Производные нитрофурана
Подавляют как грамположительные, так и грамотрицательные микроорганизмы. Концентрация Фурадонина в желчи в 200 раз превосходит его содержание в сыворотке крови; Фурадонин подавляет также патогенную флору в желудочно-кишечном тракте, действует на лямблии. Фурадонин и Фуразолидон назначают по 0,1–0,15 г 3–4 раза в день после еды.
Хлорофиллипт
Это препарат, содержащий смесь хлорофиллов, находящихся в листьях эвкалипта, подавляет грамположительные и грамотрицательные микроорганизмы, в том числе и пенициллиназообразующие стафилококки. Назначается по 20–25 капель 1% спиртового раствора 3 раза в день.
При обострении хронического холецистита лечение антибактериальными средствами проводится в течение 7–10 дней.
Антибактериальные средства целесообразно сочетать с желчегонными препаратами, оказывающими бактерицидное и противовоспалительное действие (Циквалон по 0,1 г 3–4 раза в день перед едой; Никодин по 0,5 г 3–4 раза в день перед едой).
При обнаружении в желчи паразитов проводится антипаразитарная терапия. При наличии описторхоза, фасциолеза, клонорхоза наряду с эритромицином или Фуразолидоном назначают Хлоксил (по 2 г в виде порошка в 1/2 стакана молока через каждые 10 мин 3–5 раз в течение 2 дней подряд; проводят 2 курса с интервалами 4–6 месяцев).
При обнаружении стронгилоидоза, трихоцефалеза, анкилостомидоза проводится лечение Вермоксом — по 1 таблетке 2–3 раза в день в течение 3 дней, повторный курс назначается через 2–4 недели, применяется также Комбантрин по 0,25 г 1 раз в день в течение 3 дней.
При обнаружении лямблий в желчи проводится антилямблиозная терапия одним из следующих препаратов: Фуразолидон по 0,15 г 3–4 раза в день в течение 5–7 дней; Фазижин по 2 г на прием однократно; Трихопол (метронидазол) по 0,25 г 3 раза в день после еды в течение 5–7 дней; Макмирор по 0,4 г 2 раза в день в течение 7 дней.
Применение желчегонных средств
Классификация желчегонных средств (Н. П. Скакун, А. Я. Губергриц, 1972):
Холестатические заболевания печени: алгоритмы диагностики и лечения
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
За последнее десятилетие достигнут существенный прогресс в понимании молекулярных основ образования желчи и патофизиологии холестаза. В этом обзоре кратко обобщены современные концепции образования желчи и возникновения холестаза. Определены цели медикаментозной терапии холестаза, которые помогают понять существующие методы лечения и способствуют разработке новых лекарственных препаратов от холестатических заболеваний печени (ХЗП). Лечение ХЗП проиллюстрировано на примере наиболее часто встречающегося хронического ХЗП — первичного билиарного холангита.
Ключевые слова: желчь, холестаз, холестатические заболевания печени, первичный билиарный холангит, урсодезоксихолевая кислота.
Для цитирования: Полунина Т.Е. Холестатические заболевания печени: алгоритмы диагностики и лечения. РМЖ. 2021;6:81-87.
Cholestatic liver diseases: diagnostic and treatment algorithms
A.I. Yevdokimov Moscow State University of Medicine and Dentistry, Moscow
Over the past decade, significant progress has been made in understanding the molecular basis of bilification and the cholestasis pathophysiology. The article presents the goals of cholestasis therapy, which help to understand existing treatment methods and contribute to the development of new drugs for cholestatic liver diseases (CLD). This article also briefly summarizes the current concepts of bilification and cholestasis occurrence. Treatment of CLD is illustrated by the example of the most common chronic cholestatic liver disease — primary biliary cholangitis.
Keywords: bile, cholestasis, cholestatic liver diseases, primary biliary cholangitis, ursodeoxycholic acid.
For citation: Polunina T.E. Cholestatic liver diseases: diagnostic and treatment algorithms. RMJ. 2021;6:81–87 (in Russ.).
Введение
Холестатические заболевания печени (ХЗП) начинают развиваться на фоне поражения билиарных протоков, вызванного нарушением оттока желчи [1–3]. Повреждение клеток желчных протоков (холангиоцитов) приводит к задержке желчных кислот (ЖК), билирубина и других холефилов в печени и крови и дефициту ЖК в кишечнике. Клинические признаки ХЗП проявляются в широком диапазоне: от отдельных нарушений биохимических показателей функции печени до острой печеночной недостаточности или злокачественных образований в гепатобилиарной системе (например, холангиокарциномы). Длительно сохраняющийся холестаз (в течение нескольких месяцев или лет) может привести к развитию цирроза печени [4]. К наиболее распространенным и изученным ХЗП относят первичный билиарный холангит и первичный склерозирующий холангит [2].
Холестатические заболевания печени включают прогрессирующие холангиопатии, которые могут переходить в терминальную стадию заболевания печени. В США с 1988 по 2018 г. на ХЗП приходилось 14,2% всех трансплантаций печени [2]. Высокая заболеваемость и смертность превратились в большую проблему из-за отсутствия эффективных методов лечения. Более того, от 10% до 40% пациентов после трансплантации печени переживают рецидив основного заболевания [5].
Общие патогенные механизмы ХЗП
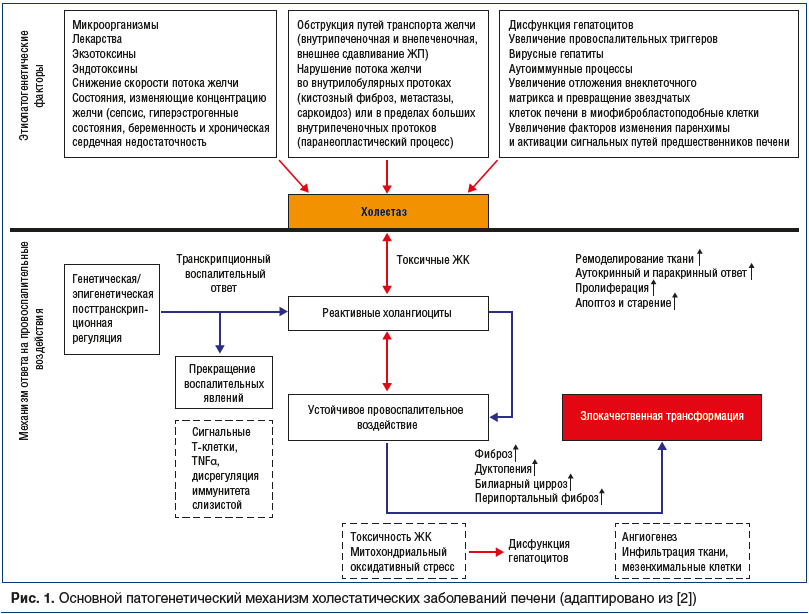
Нарушение оттока желчи может быть обусловлено несколькими факторами (рис. 1), основные из них — антигенные стимулы, экзотоксины, эндотоксины, ксенобиотики и микроорганизмы. Эти внешние факторы вызывают воспалительную реакцию холангиоцитов, которая перерастает в холестатическое состояние [6]. Обструкция транспорта желчи — еще один предрасполагающий фактор. Внутрипеченочная и внепеченочная обструкция может иметь место из-за внешнего доброкачественного сдавления (кистозные заболевания), эффекта злокачественной опухоли (холангиокарциномы), а также вследствие образования или миграции желчных конкрементов по билиарному тракту. Условия, которые замедляют отток желчи, способствуют холестатическому состоянию с повышенной концентрацией ЖК. Сепсис, гиперэстрогенные состояния (беременность), хроническая сердечная недостаточность и дисфункция генов — транспортеров ЖК могут изменять основные характеристики желчи, активируя более цитотоксический компонент ЖК.
Первичная защитная реакция холангиоцитов позволяет купировать повреждение. Однако устойчивое нарушение провоспалительных генетических и/или эпигенетических регуляторных механизмов может вызвать постоянное дисфункциональное расстройство, что в конечном итоге приведет к фиброгенному состоянию с билиарным и перипортальным фиброзом, потерей гомеостаза тканей и аутокринным и паракринным ремоделированием. Пролиферация может вызвать изменение клеточного цикла, старение, апоптоз, дуктопению, мезенхимальную инфильтрацию, а иногда и злокачественную трансформацию.
В настоящее время выделяют несколько концепций возникновения холестаза.
Дуктулярная (канальцевая) реакция — первая основная концепция холестаза. Внутрипеченочные и внепеченочные желчные протоки разного размера выстланы холангиоцитами, которые регулируют и изменяют объем и состав желчи. Они различаются по размеру, скорости метаболизма, а также способности к пролиферации и пластичности. Дуктулярная реакция является частью реакции клеток печени на повреждения при ХЗП [7]. Ответная реакция холангиоцитов на воспаление может привести к уменьшению повреждения, а в случае устойчивого воспалительного воздействия приводит к фиброзу желчных протоков [8].
Цитотоксичность ЖК и митохондриальная дисфункция — вторая фундаментальная основа патогенеза ХЗП, описанная в нескольких исследованиях при внепеченочном холестазе [9].
Влияние иммуногенетических и эпигенетических факторов на иммуновоспалительный ответ — это третий фундаментальный аспект патогенеза ХЗП. У пациентов с ХЗП имеется множество генетических изменений, которые объясняют различные элементы каждого ХЗП. Однако некоторые из этих генов могут быть непосредственно вовлечены в прогрессирование холестатического фенотипа. Следовательно, они могут стать потенциальной мишенью для новых терапевтических средств либо их активаторы транскрипции косвенно могут служить модулирующими мишенями. Эта модуляция представляет собой тип эпигенетического контроля экспрессии генов как патогенного механизма холестаза [2].
Клинический спектр ХЗП [2]:
Идиопатические: первичный билиарный холангит, первичный склерозирующий холангит, аутоиммунный холангит, IgG4-ассоциированный холангит, идиопатическая дуктопения, билиарная атрезия.
Вторичный склерозирующий холангит: холедохолитиаз, лекарственный (токсический) холангит, портально-гипертензивная билиопатия, ВИЧ-ассоциированный холангит, абдоминальная травма, дефицит АВСВ4, ятрогенные билиарные стриктуры, васкулярный/ишемический холангит, серповидно-клеточная болезнь, рецидивирующий пиогенный холангит.
Генетические: муковисцидоз, синдром Кароли, синдром Алажилля, аутосомно-доминантная поликистозная болезнь почек, аутосомно-рецессивная поликистозная болезнь почек, аутосомно-доминантный поликистоз печени, холестаз при беременности.
Дисфункциональные перестройки матрикса и фиброгенез — четвертая концепция патогенеза ХЗП. Фиброгенез — это сложный динамический процесс, связанный с взаимодействием иммуновоспалительных механизмов, изменением секреции тканевых металлопротеиназ, цитокиновых сетей и нарушением инфильтрации мезенхимальных клеток с окончательной потерей поддерживающего гомеостаза тканей. Фиброгенные процессы затрагивают поврежденные и неповрежденные желчные протоки, а также перипортальную синусоидальную систему, что приводит к прогрессирующему холестазу [10].
Диагностика
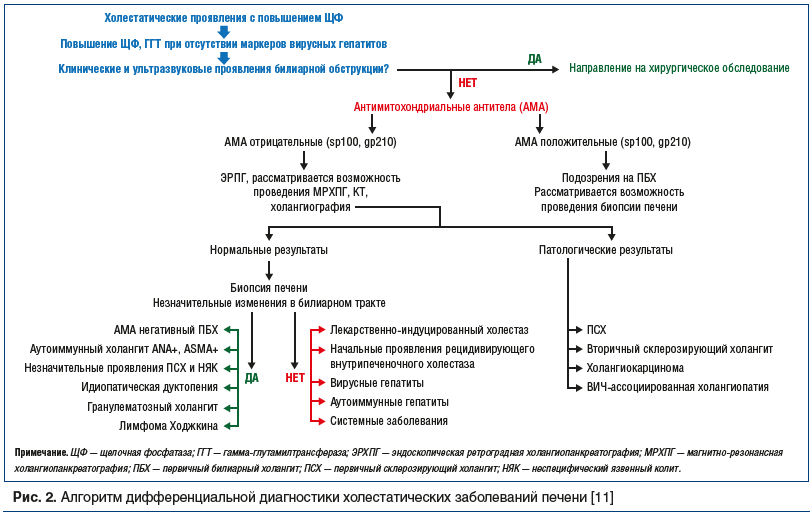
Различить виды холестаза по клиническим симптомам и биохимическим показателям не всегда удается. Чрезвычайно важным является разграничение вне- и внутрипеченочного холестаза с использованием диагностического алгоритма (рис. 2) [11].
Клиническая картина ХЗП различна. У многих пациентов холестаз протекает бессимптомно и диагностируется при оценке стойких холестатических лабораторных аномалий. У пациентов с симптомами могут наблюдаться дискомфорт в правом верхнем квадранте, зуд, усталость и потеря веса.
Первичный билиарный холангит (ПБХ) является аутоиммунным заболеванием и представляет собой наиболее распространенное хроническое ХЗП. Его прежнее название — «первичный билиарный цирроз». Однако от этого термина отказались в пользу «первичного билиарного холангита», поскольку у большинства пациентов нет цирроза. ПБХ возникает под воздействием сочетания генетических факторов и факторов окружающей среды, которые запускают опосредованное Т-лимфоцитами разрушение внутрипеченочных желчных протоков. Большинство (90%) заболевших — женщины, и обычно это заболевание диагностируется в возрасте от 40 до 60 лет. Сопутствующие аутоиммунные заболевания часто встречаются у пациентов с ПБХ, включая синдром Шегрена, заболевания щитовидной железы, ограниченную кожную склеродермию и ревматоидный артрит [12].
Приблизительно 60% пациентов с ПБХ не имеют симптомов на момент постановки диагноза. Обычно диагноз ставится на основании отклонений от нормы биохимических тестов печени. Утомляемость и зуд являются наиболее частыми симптомами у пациентов с ПБХ. Физикальное обследование может выявить гепатомегалию, гиперпигментацию кожи, желтуху, ксантомы или стигматы цирроза и портальной гипертензии на более поздних стадиях. Характерные лабораторные отклонения включают повышение щелочной фосфатазы (ЩФ) с нормальным или умеренным повышением аминотрансфераз в сыворотке крови. Повышение уровня билирубина в сыворотке обычно происходит при прогрессировании заболевания и является плохим прогностическим признаком.
При ПБХ часто встречаются нарушения липидов. Небольшое повышение липопротеинов низкой плотности (ЛПНП) с более выраженным повышением липопротеинов высокой плотности (ЛПВП) часто встречается на ранних стадиях ПБХ, тогда как более заметное повышение ЛПНП и более низкие уровни ЛПВП отмечаются на более поздних стадиях заболевания. ПБХ также может быть связан с метаболическим заболеванием костей, стеатореей и дефицитом жирорастворимых витаминов.
Антимитохондриальные антитела (АМА) — это специфические антитела, которые считаются серологическим признаком ПБХ и присутствуют у 95% пациентов с этим заболеванием. Следовательно, положительный результат теста на АМА в контексте повышения холестатической пробы печени достаточен для установления диагноза ПБХ.
Первичный склерозирующий холангит (ПСХ) — это хроническое ХЗП, характеризующееся воспалением и фиброзом внутри- и внепеченочных желчных протоков. Холангит может быть диагностирован на более поздней стадии болезни, вторичной по отношению к обструкции из-за стриктур. Повышение уровня ЩФ в сыворотке крови является наиболее частым лабораторным отклонением у пациентов с ПСХ. Примерно 50% пациентов с ПСХ могут иметь нормальные показатели ЩФ. Следовательно, нормальные значения ЩФ не исключают диагноз ПСХ. Уровень аминотрансфераз в сыворотке может быть в 2–3 раза выше верхней границы нормы. В отличие от ПБХ, аутоантитела в сыворотке неспецифичны и обычно не используются для постановки диагноза ПСХ. Диагноз ПСХ, связанного с патологией большого протока, устанавливается на основании холангиограммы, и отсутствие патологии при УЗИ брюшной полости не исключает ПСХ. Следовательно, при подозрении на ПСХ предпочтительным диагностическим тестом является магнитно-резонансная холангиопанкреатография. По сравнению с эндоскопической ретроградной холангиопанкреатографией это неинвазивный и точный метод обнаружения ПСХ. Пациенты с ПСХ в малом протоке имеют нормальные холангиограммы и требуют биопсии печени для установления диагноза ПСХ.
Вторичный склерозирующий холангит (ВСХ) — это хроническое ХЗП, которое приводит к прогрессирующему фиброзу печени, нерегулярному уплотнению и расширению желчных протоков. Холангиографическая картина ВСХ аналогична таковой при ПСХ. К наиболее частым обструктивным причинам ВСХ относятся: хирургические травмы, вызванные холецистэктомией, внутрипротоковые камни, рецидивирующий панкреатит и стриктуры желчных путей. Застой в желчевыводящих путях, вызванный обструкцией, предрасполагает к рецидиву холангита и образованию пигментных камней и воспалительных стриктур, которые затем усугубляют холестаз. Ранние изменения, наступившие после обструкции желчных путей, могут регрессировать при ее лечении. Однако со временем такие изменения могут развиться в необратимый обширный перипортальный и перидуктулярный фиброз и вторичный билиарный цирроз.
По клинической картине и лабораторному профилю ВСХ и ПСХ очень похожи. Рецидивирующий бактериальный холангит очень часто встречается на поздних стадиях ВСХ.
В редких случаях биопсия печени требуется для установления диагноза ПБХ, когда проба на АМА отрицательна или когда требуется более точная дифференциальная диагностика с аутоиммунным гепатитом, лекарственным холестазом, рецидивирующим внутрипеченочным холестазом, вирусными гепатитами, системными заболеваниями.
Перспективы проведения биопсии печени зависят от поражений мелких желчных протоков при: ПСХ, идиопатической дуктопении, гранулематозном холангите, лимфоме Ходжкина.
Лечение ХЗП
Распространенным следствием всех форм холестаза является задержка ЖК в гепатоцитах. Повышенный уровень ЖК приводит к апоптозу или некрозу гепатоцитов и в конечном итоге к хроническому ХЗП [13]. При некоторых холестатических расстройствах также происходит проникновение ЖК в перибилиарное пространство, что вызывает воспаление воротной вены и фиброз за счет индукции хемокинов и цитокинов.
В связи с этим выделяют следующие фармакологические мишени для лечения внутрипеченочного холестаза (рис. 3) [13]:
стимуляция ортоградной секреции желчных путей и ретроградной секреции ЖК и других токсичных холефилов в системный кровоток для выведения почками;
стимуляция метаболизма гидрофобных ЖК и других токсичных соединений до более гидрофильных, но менее токсичных метаболитов;
защита пораженных холангиоцитов от токсического действия желчи; ингибирование апоптоза, вызванного повышенным уровнем цитотоксических ЖК;
ингибиция фиброза, вызванного утечкой ЖК в перибилиарное пространство.
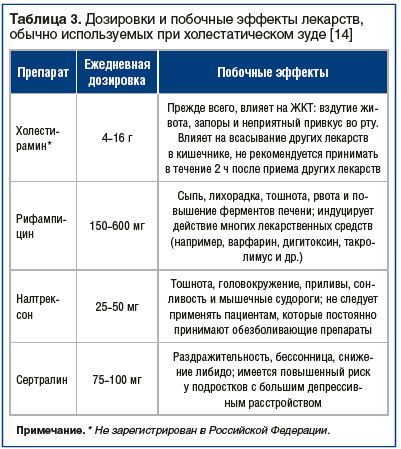
Медикаментозная терапия ХЗП представлена в табл. 1. В табл. 2 и 3 представлены основные симптомы, возникающие при ХЗП, и лекарственные препараты для их купирования.
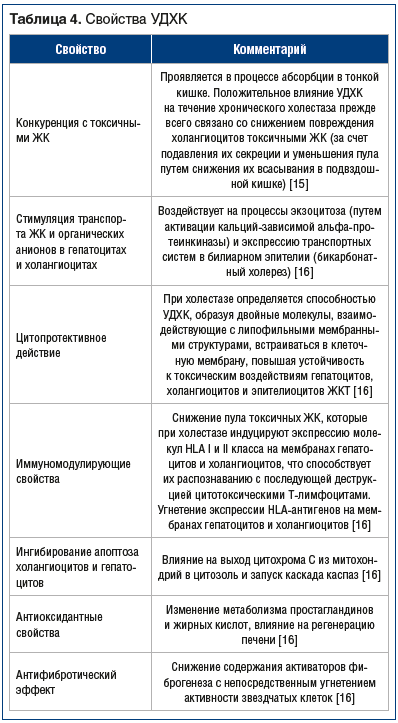
Единственным общепринятым препаратом для медикаментозного лечения большинства хронических ХЗП является урсодезоксихолевая кислота (УДХК) [12, 15–19]. Способность лечить холестаз считается одним из важнейших и наиболее ценным свойством этого лекарственного средства. В табл. 4 представлены основные свойства УДХК, которые, по мнению автора, наиболее полно раскрыты в статьях [15, 16].
Наиболее убедительно доказано положительное действие УДХК при таком холестатическом заболевании, как ПБХ. В комбинированном анализе французских, канадских и североамериканских когорт больных при 2–4-летнем наблюдении отмечено снижение смертности и необходимости трансплантации печени в группах с умеренным и тяжелым течением заболевания. «Барселонское» исследование 192 пациентов, получавших УДХК сроком от 1,5 года до 14 лет, показало, что выживаемость у пациентов, ответивших на терапию УДХК (ответ оценивался по уровню снижения ЩФ), была выше предсказанной по прогностической модели Мейо и соответствовала популяционной [16].
Доза УДХК 13–15 мг/кг/сут при большинстве холестатических заболеваний имеет преимущество по биохимическому ответу и стоимости в сравнении с низкими и высокими дозами. Исключением является муковисцидоз, где рекомендуются дозы 20–30 мг/кг/сут [16]. При ПСХ рекомендуемые дозы не определены.
Имеются данные о положительном влиянии УДХК на лекарственный холестаз, в том числе обусловленный одним из наиболее часто вызывающих гепатотоксичность препаратов — амоксициллином/клавуланатом [16].
Европейская ассоциация по изучению болезней печени (European Association for the Study of the Liver, 2009) [20] и Российская гастроэнтерологическая ассоциация [1] рекомендуют обязательное назначение УДХК в качестве базисной терапии при ряде ХЗП: первичном билиарном циррозе, ПСХ, муковисцидозе, прогрессирующем семейном холестазе 3 типа (Progressive Familial Intrahepatic Cholestasis 3), внутрипеченочном холестазе беременных, а также обсуждают ее назначение при лекарственном холестазе и доброкачественном семейном холестазе.
Концепция структурированной пожизненной терапии ПБХ опирается на 3 основных элемента: 1) стратификацию риска и соответствие ему терапии; 2) определение стадии и наблюдение в соответствии с ней; 3) активное ведение. Помощь всегда строится с учетом индивидуальных особенностей больного и возможностей здравоохранения данной страны, но ее эффективность обеспечивают эти 3 опорных элемента [21].
На сегодня оригинальный препарат УДХК — Урсо (Япония) в России не зарегистрирован. В этой ситуации при выборе дженерических препаратов, широко представленных на отечественном фармацевтическом рынке, следует руководствоваться, прежде всего, соотношением цены и качества. Появившийся в последние годы отечественный препарат УДХК Урдокса ® производства АО «ФП «Оболенское» не уступает ранее зарегистрированным в нашей стране дженерическим формам [16]. Этот отечественный лекарственный препарат обладает характеристиками, позволяющими считать его препаратом выбора на любом этапе медицинской помощи больным с широким спектром нозологий, в том числе при хронических ХЗП. Урдокса ® производится из европейской субстанции (Италия, Industria Chimica Emiliana) на российском предприятии по международному стандарту GMP (Good Manufacturing Practice — Надлежащая производственная практика). Высокий профиль безопасности позволяет применять препарат у детей старше 3 лет [22].
Препарат успешно прошел все предусмотренные законодательством регистрационные процедуры, что позволяет говорить о его биоэквивалентности референтным препаратам, содержащим УДХК [23, 24].
Подтверждением фармацевтической эквивалентности препаратов УДХК является не только одинаковое количество активного вещества и вспомогательных веществ в 1 капсуле препарата, но и наличие идентичных инфракрасных спектров, полученных при инфракрасной спектроскопии готовых лекарственных форм сравниваемых препаратов УДХК [25–27].
Надежность динамики стандартных биохимических показателей функции печени на фоне терапии — простого и информативного диагностического инструмента подтверждена последними 10 годами его широкого использования. Ответ на УДХК-терапию поддается оценке по модели дискретных бинарных переменных или балльных оценочных систем на основе расчета непрерывных переменных [21]. Так, согласно Парижским критериям хорошим биохимическим ответом через 12 мес. терапии УДХК считается уровень сывороточного билирубина ≤17 мкмоль/л (1 мг/дл), уровень ЩФ ≤3 верхней границы нормы и уровень аспартат-аминотрансферазы ≤2 верхней границы нормы.
Заключение
Таким образом, холестаз является очень частым явлением и может встречаться в различных клинических условиях. Понимание особенностей этиопатогенеза холестаза и правильное применение этих особенностей в дифференциальной диагностике и лечении ХЗП способствуют формированию эффективного практического подхода в терапии холестаза общей этиологии. В настоящее время УДХК является препаратом выбора для лечения ХЗП, поскольку она обеспечивает облегчение симптомов, улучшает биохимические и гистологические показатели функции печени, а также, что наиболее важно, увеличивает выживаемость пациентов с ХЗП [16]. Положительные эффекты УДХК были документально подтверждены рандомизированными контролируемыми исследованиями. Терапия с применением препаратов УДХК является определяющей при ряде холестатических расстройств, таких как ПБХ, ПСХ, внутрипеченочный холестаз беременных, заболевания печени при муковисцидозе, прогрессирующий семейный внутрипеченочный холестаз и некоторые формы лекарственного холестаза.
Редакция благодарит АО «Алиум» за оказанную помощь в технической редактуре настоящей публикации.
Только для зарегистрированных пользователей