Гонококки хламидии чем лечить
Гонорея и хламидиоз – близнецы-братья
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Центральный научно-исследовательский кожно-венерологический нститут
Среди множества инфекций, передаваемых половым путем, гонорея и хламидиоз занимают особое место. Гонорея – одно из самых знаменитых заболеваний человека – олицетворяет собой нечто очень древнее, испокон веков ему присущее, то есть болезнь с «историей». Первые упоминания о ней обнаруживаются в древних трактатах, даже в Библии есть рекомендации по предупреждению этого заболевания. Сам термин «гонорея», что означает «истечение семени» (тогда ошибочно считали, что выделения при этом заболевании представляют собой именно семенную жидкость, а не гной), был введен Галеном во II веке н.э. Итак, к концу XX века о этой инфекции должно быть известно практически все. А хламидиоз – это нечто вполне современное. Возбудитель был открыт лишь в начале XX века как инфекция, вызывающая поражение глаз. А о способности хламидий передаваться половым путем и вызывать соответствующие воспалительные урогенитальные заболевания стало известно лишь через несколько десятков лет. Все, что касается клинических проявлений, диагностики и лечения хламидийной инфекции, – предмет самого пристального изучения ученых и клиницистов сегодня.
Из–за таких серьезных исторических различий может создаться впечатление, что между этими инфекциями мало общего. На самом деле это далеко не так. Различия, конечно, велики, но и аналогий вполне достаточно, чтобы рассматривать их параллельно. Эти инфекции имеют сходные эпидемиологические особенности, пути передачи, похожи между собой нозологические формы, которые они вызывают у людей, и соответственно их клинические проявления. Всего этого вполне достаточно, чтобы объединить их описание в одной статье, что мы и попытаемся сделать.
Итак, что из себя представляют возбудители гонореи и хламидиоза?
Пожалуй, различия между этими двумя инфекциями нигде столь наглядно не проявляются, как в характеристике самих возбудителей. Единственное, что можно считать безусловно общим, так это принадлежность и Neisseria gonorrhoeae и Chlamydia trachomatis к бактериям, – к грамотрицательным бактериям. На этом сходство и кончается, все остальное – сплошные различия.
Возбудитель гонореи – Neisseria gonorrhoeae – микроорганизм с вполне характерной морфологией. Это бобовидной формы диплококк, который, как правило, можно легко идентифицировать при окраске по Граму или просто любыми анилиновыми красителями (метиленовым синим, бриллиантовым зеленым и пр.) с использованием обычной световой микроскопии при 400–600-кратном увеличении.
Хламидии, а точнее Chlamydia trachomatis – единственные из четырех видов хламидий, способные передаваться половым путем, – из-за своих мелких размеров, соизмеримых с размерами вирусов, при обычной светооптической микроскопии обнаружить невозможно. В лучшем случае при такой микроскопии можно обнаружить так называемые хламидийные включения – внутриклеточные вакуоли, содержащие хламидийные тельца. Говоря о морфологии хламидий, подразумевают не что-то вполне определенное, как в случае с гонококком, а нечто постоянно развивающееся и существующее в двух совершенно различных формах, обладающих абсолютно разными свойствами и даже размерами, которые могут отличаться в 3 раза. То, что при своем развитии демонстрируют хламидии, – уникальное явление в биологии, и это позволило в классификации микроорганизмов выделить их в особое семейство. В процессе жизнедеятельности хламидий происходит постоянный переход одной формы их существования, элементарного тельца (ЭТ), в другую – ретикулярное тельце (РТ). Этот процесс получил название жизненного цикла хламидий и по времени занимает около 72 ч. Причем к самостоятельной жизнедеятельности хламидии совершенно неспособны, поскольку у них начисто отсутствует энергетическая система. В этом смысле они полностью зависят от клетки–хозяина. Такое явление получило название «облигатный внутриклеточный паразитизм» и для бактерий совершенно не характерно, зато является отличительным признаком вирусов. Любопытно, что инфекционными для человека являются именно ЭТ, зато в них не происходит никаких заметных жизненных процессов и размножаться они не могут. Именно эти тельца напоминают по своим свойствам (мелкие размеры, неспособность к самостоятельному размножению, нечувствительность к действию антибиотиков) вирусы. Попадая внутрь чувствительной к ним клетки, ЭТ хламидий начинают преобразовываться в РТ, которые уже обладают всеми признаками обычной бактерии, т.е. способны делиться, чувствительны к антибиотикам и пр. Только облигатный внутриклеточный паразитизм выдает их принадлежность к особой разновидности бактерий. Кстати, РТ не обладают инфекционными свойствами и заразить ими невозможно. Такие особенности хламидий определяют очень многие проблемы, встающие перед клинической практикой, начиная от диагностики и кончая лечением.
Несмотря на такие явные различия гонококков и хламидий, с точки зрения клиницистов общего у этих двух инфекций гораздо больше, чем можно было ожидать, и прежде всего пути передачи.
Пути передачи гоноккокков и хламидий
Оба возбудителя передаются от больного человека здоровому практически исключительно половым путем. Из этого правила, разумеется, возможны исключения (естественно его подтверждающие). Хотя описаны случаи так называемого бытового заражения, но их достоверность, как правило, вызывает сомнения. Безусловно встречаются случаи заражения плода при прохождении родовых путей матери, пораженных гонококком или хламидиями. При этом возбудитель может попасть на конъюнктиву глаза или в дыхательные пути.
Клинические проявления гонококковой и хламидийной нфекции
Следует отметить, что оба микроорганизма – и гонококки, и хламидии – обладают тропностью к цилиндрическому эпителию, выстилающему слизистую уретры, прямой кишки, глотки и конъюнктивы глаза у мужчин и женщин, а также цервикального канала у женщин. При попадании любого из этих возбудителей на такой эпителий может возникать соответствующая характерная симптоматика. Правда, имеется и ряд отличий в клинических проявлениях гонококковой и хламидийной инфекции, которые позволяют предположить наличие у пациента именно того, а не другого возбудителя еще до получения результатов лабораторной диагностики (таб. 1).
Разумеется, приведенными признаками не исчерпываются все возможные клинические различия. Мы перечислили лишь основные и наиболее явные.
На практике бывает сложно отличить хламидийную инфекцию от гонококковой еще и потому, что примерно у 1/3 больных встречается комбинация этих двух возбудителей. При общности путей передачи, групп риска и тропности к одному и тому же эпителию такое сочетание скорее следует признать закономерным, чем исключительным.
Некоторые эпидемиологические аспекты гонококковой и хламидийной инфекций
Если между этими двумя микроорганизмами и есть различия с точки зрения эпидемиологии, то они носят скорее статистический и социальный, чем принципиальный характер.
В развитых странах хламидийную инфекцию считают самой частой из передаваемых половым путем, и встречается она преимущественно среди людей, принадлежащих к классу не ниже среднего, а вот гонорея встречается крайне редко, да и распространена она среди низов общества. Что касается России, то, согласно официальным статистическим данным, самой распространенной инфекцией, передаваемой половым путем, является сифилис. А частота гонореи и урогенитального хламидиоза у нас примерно одинакова и гораздо меньше, чем сифилиса. Такие существенные расхождения с мировыми данными позволяют предположить, что мы не обладаем полной информацией относительно истинной распространенности хламидийной (как, впрочем, и гонококковой) инфекции в России. Однако в последние несколько лет имеется явная тенденция к ежегодному росту регистрируемых случаев хламидиоза одновременно со значительным сокращением числа случаев гонореи.
Диагностика гонококковой и хламидийной инфекции
В отличие от эпидемиологии принципы диагностики гонореи и хламидиоза различаются существенно, и определяется это в первую очередь биологическими особенностями возбудителей.
Благодаря крупным размерам и характерной морфологии, как правило, идентификация N.gonorrhoeae не представляет особых сложностей. Наиболее распространенным методом лабораторной диагностики гонореи является окраска по Граму мазков отделяемого из уретры или цервикального канала. В подавляющем большинстве случаев такого исследования для выявления гонореи бывает достаточно. Если же возникают какие–либо трудности, то можно прибегнуть к культуральной диагностике, т.е. посеву материала от больного на специальные питательные среды с последующей идентификацией выросшего на этой среде возбудителя.
С хламидиями все далеко не так просто. Малые их размеры не позволяют наблюдать эти микроорганизмы при обычной световой микроскопии, а облигатный внутриклеточный паразитизм не дает возможности выращивать хламидии на обычных искусственных питательных средах. Думается, что именно эти особенности хламидий не позволяли в течение длительного времени разработать достаточно точную и практически применимую методику выявления этого микроорганизма. Массовая диагностика хламидийной инфекции началась лишь с середины 80–х годов нашего века, когда в клиническую практику был внедрен метод прямой иммунофлюоресценции с использованием моноклональных антител к C.trachomatis. Этот метод впервые позволил идентифицировать не только хламидийные включения внутри клеток, но и находящиеся в межклеточном пространстве ЭТ хламидий, причем сделать это достаточно быстро, буквально в течение получаса. До сих пор этот метод остается одним из самых распространенных при диагностике хламидий. Культуральное исследование для выявления хламидий может быть проведено только с помощью культуры клеток, как это делается с целью идентификации вирусов. Это очень сложно и дорого, а самое главное, занимает очень много времени, до недели, что для практики не вполне приемлемо. Серологические методы диагностики при хламидиозе широкого применения не нашли, поскольку сам факт обнаружения антител к хламидиями еще не означает, что у больного возбудитель присутствует на момент обследования. Возможно, хламидиоз был излечен в прошлом. Зато недавнее появление нового молекулярного диагностического метода (полимеразная цепная реакция), произвело новый переворот в диагностике хламидиоза, позволив обнаружить этот микроорганизм у человека при наличии в пробе всего одной хламидии. Такая чувствительность диктует необходимость особо тщательного контроля за качеством реагентов, соблюдением всех тонкостей методики, где нет мелочей, и учета возможностей метода, в частности, влияния ингибиторов, способных препятствовать обнаружению инфекции даже при явной клинической картине.
Лечение гонококковой и хламидийной инфекций
Когда речь идет об инфекции, наибольший интерес у клиницистов и у больных всегда вызывают вопросы лечения. Вот здесь различия между N.gonorrhoeae и C.trachomatis проявляются так же ярко, как и при сравнении их морфологии. Именно биологические особенности обоих возбудителей определяют совершенно разную лечебную тактику и выбор антибактериальной терапии.
Препараты, которые обладают наивысшей активностью в отношении N.gonorrhoeae оказываются совершенно неэффективными для лечения хламидийной инфекции (табл. 2)
Конечно, в таблице перечислены не все препараты, известные своей активностью в отношении гонококков и хламидий, а лишь основные группы. Причем, если в случае гонореи список препаратов настолько обширен, что легче перечислить те, которые не обладают активностью в отношении этого возбудителя, то для лечения хламидийной инфекции используются только тетрациклины, макролиды (включая азалиды), и фторхинолоны. На самом деле список рекомендуемых для лечения гонореи препаратов заметно отличается от списка антибиотиков, обладающих какой–либо активностью в отношении этого микроорганизма. Согласно современным представлениям для лечения гонореи следует использовать только те антибиотики, которые эффективны не менее чем в 95% случаев при одномоментном применении. Список таких препаратов достаточно широк, но в подавляющем большинстве случаев для лечения гонореи препараты из группы цефалоспоринов и фторхинолонов, практически любой из которых отвечает вышеуказанному требованию. Для каждого антибиотика из представленных выше групп известны эффективные схемы лечения. Между тем проблемы при терапии гонореи и хламидиоза сохраняются. Если попытаться их классифицировать, представляются наиболее существенными следующие:
1) непереносимость антибиотика пациентом;
2) развитие устойчивости к антибиотику у микроорганизма;
3) неправильный выбор антибиотика в случае смешанной инфекции.
Во избежание возникновения этих проблем следует придерживаться определенных, достаточно простых правил.
Правило 1. Оно носит универсальный характер: перед назначением любого препарата, особенно антибиотиков и тем более парентерально, следует в обязательном порядке собирать аллергологический анамнез.
Правило 2. Чтобы быть уверенным в эффективности выбранного антибиотика, желательно определить чувствительность к нему микроорганизма, изолированного от больного. Справедливости ради следует заметить, что ни при гонорее, ни при хламидиозе такие исследования, как правило, не проводятся. В первом случае – из-за простоты решения проблемы путем назначения антибиотика из другой группы при неэффективности вначале выбранной терапии, а во втором – из-за больших технических сложностей при опредлении in vitro чувствительности к антибиотикам. Во избежание ошибок в выборе терапии следует руководствоваться региональными данными об устойчивости возбудителей к антибиотику для каждой конкретной местности. Так рост пенициллиназопродуцирующих штаммов гонококка в некоторых регионах мира уже привел практически к полному вытеснению пенициллинов из числа антибиотиков, рекомендуемых к применению при гонорее. То же самое можно сказать и в отношении тетрациклинов, к которым, как показали исследования, проведенные в России, устойчивы около 70% штаммов гонококка.
Правило 3. Если у больного диагностирована смешанная гонорейно-хламидийная инфекция, то рациональным представляется назначение препаратов, одинаково эффективных в отношении обеих инфекций. Трудно было бы объяснить назначение антибиотиков из двух разных групп, если имеется возможность назначить единственный антибиотик. Данные табл. 2 показывают, что фторхинолоны – единственная группа препаратов, обладающих достаточно высокой активностью как в отношении N.gonorrhoeae, так и в отношении C.trachomatis. Действительно, антибиотики из этой группы отвечают основному требованию, необходимому для назначения их при гонорее, т.е. способны излечивать эту инфекцию при одномоментном применении. Что касается хламидий, то, хотя фторхинолоны и не относятся к препаратам выбора при этой инфекции, но в качестве альтернативных представители этой группы (офлоксацин и ломефлоксацин) входят в список рекомендуемых при урогенитальном хламидиозе. Все это дает основание считать использование фторхинолонов при смешанной гонорейно–хламидийной инфекции оптимальным.
Что касается конкретных схем терапии гонореи и хламидиоза, то их можно найти в любом справочнике. Важно помнить, что при решении вопроса о длительности терапии хламидийной инфекции надо исходить из продолжительности жизненного цикла этого микроорганизма не менее 72 ч. Любая схема лечения должна учитывать тот факт, что, если хламидия находится на стадии ЭТ, то антибиотики могут оказаться неэффективными, поэтому следует продолжать терапию по крайней мере на протяжении двух жизненных циклов. Другой возможностью может быть назначение антибиотика с действием, пролонгированным настолько, чтобы поддерживать подавляющую концентрацию на протяжении этих двух жизненных циклов. Единственным таким антибиотиком является азитромицин. К сожалению, его активность в отношении гонококков оставляет желать лучшего.
В заключение хочется еще раз напомнить о сходстве и различиях гонореи и хламидиоза, поскольку желательно, чтобы выявление, лечение и профилактика этих двух распространенных инфекций представляли собой единый комплекс мероприятий, обеспечивающих избавление от этих «легких» инфекций, чреватых иногда весьма тяжелыми последствиями, такими как эпидидимит, простатит, сальпингоофорит и бесплодие.
Урогенитальный хламидиоз, урогенитальный трихомониаз
Клиника, диагностика, лечение Каковы особенности современного течения урогенитального хламидиоза и трихомониаза? Какова тактика ведения этих заболеваний? Хламидийная инфекция может вызывать воспаление органов малого таза Урогенита
Клиника, диагностика, лечение
Каковы особенности современного течения урогенитального хламидиоза и трихомониаза?
Какова тактика ведения этих заболеваний?
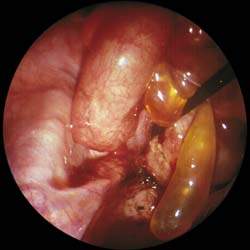 |
| Хламидийная инфекция может вызывать воспаление органов малого таза |
Урогенитальный хламидиоз является одной из серьезных медико-социальных проблем. Указанная инфекция получила широкое распространение в различных странах мира, причем число инфицированных постоянно растет.
Хламидии представляют собой бактерии с характерной для прокариотов структурой. Они имеют вид мелких грамотрицательных кокков. Это облигатные внутриклеточные паразиты с уникальным циклом развития, включающим две различные по морфологии и биологическим свойствам формы существования микроорганизмов, которые обозначаются как элементарные и инициальные (ретикулярные) тельца.
В последнее время появляется все больше данных о возможности существования латентных или персистирующих форм хламидий как при моделировании in vitro, так и в организме больного in vivo.
Клиника урогенитального хламидиоза
В настоящее время отечественные специалисты не пришли к единому мнению относительно классификации хламидиоза. Часть из них пользуются классификацией, аналогичной той, которая принята для гонореи, другие произвольной, в соответствии с локализацией очагов поражения или характером течения инфекции. Целесообразно при постановке диагноза использовать термин «урогенитальный хламидиоз», что позволяет идентифицировать хламидиоз среди заболеваний, передаваемых половым путем.
Клиническая картина заболеваний мочеполовых органов, обусловленных хламидиями, отличается от гонококковой инфекции главным образом меньшей остротой воспалительного процесса, большой частотой осложнений и устойчивостью по отношению к терапии. Для женщин хламидиоз представляет наибольшую опасность, т. к. он вызывает не только серьезную патологию нижнего отдела мочеполовой системы, но и нередко сопровождается развитием восходящей диссеминированной инфекции, возникновением тазовых воспалительных заболеваний, развитием бесплодия, инфицированием новорожденных. Чаще всего и прежде всего хламидиями инфицируется шейка матки, откуда, как из резервуара, процесс распространяется в мочеиспускательный канал, матку и фаллопиевы трубы, во внутренние органы. Инкубационный период при хламидиозе колеблется в пределах 15-30 дней.
Особенностью клинического течения воспалительного процесса при хламидиозе мочеполовых органов является асимптомное и малосимптомное течение, многоочаговость: уретриты, эпидидимиты, оофориты, простатит, вульвовагиниты, проктиты, кольпиты, цервициты, эндоцервициты, сальпингиты, параметриты, септические состояния. Острая форма хламидиоза с обильными выделениями, выраженной гиперемией слизистых оболочек, с дизурическими расстройствами и выраженными болевыми ощущениями встречается редко даже у мужчин, а у женщин лишь в исключительных случаях. Значительно чаще наблюдаются подострые и торпидные формы. У мужчин, больных хламидиозом, при осмотре обнаруживается умеренная гиперемия и отечность губок мочеиспускательного канала, иногда и крайней плоти полового члена, слизисто-гнойное отделяемое. У женщин хламидиоз проявляется усилением болей, могут отмечаться боли внизу живота и в крестце во время и после полового акта, болезненность при мочеиспускании. Заболевание чаще протекает без субъективных ощущений и с минимальными клиническими проявлениями или без них.
Симптоматика хламидийных заболеваний у детей более выражена и, в зависимости от давности воспалительного процесса, проявляется в виде вульвовагинита, уретрита, цервицита. Болеют чаще девочки, особенно в старшем возрасте, когда заражение происходит половым путем. Наряду с диффузной гиперемией вульвы и прилегающих участков кожного покрова отмечается отек наружных половых органов, мацерация их в результате обильных, жидких серо-зеленого цвета выделений. При поражении мочеиспускательного канала губки гиперемированы, отечны, покрыты отделяемым серого цвета, возможно учащенное и болезненное мочеиспускание.
Следовательно, клиническая картина воспалительного процесса в мочеполовых органах при хламидиозе идентична таковой при других заболеваниях, передаваемых половым путем, но процесс менее выражен, протекает почти без субъективных ощущений и редко заставляет больных обращаться к врачу. Поэтому заболевание, переходя в вялотекущую хроническую форму, может протекать годами, вызывая как у мужчин, так и у женщин различные осложнения. У мужчин при восходящей хламидийной инфекции развиваются воспалительные изменения в простате и придатке яичка, что может приводить к нарушению генеративной функции и к бесплодию (развитие простатитов и эпидидимитов). Бесплодие у мужчин может развиться не только в результате перенесенного эпидидимита хламидийной этиологии, но и из-за непосредственного воздействия паразита на сперматозоиды. У женщин хламидийная инфекция вызывает также нарушение репродуктивной функции. К серьезнейшим осложнениям генитального хламидиоза можно отнести окклюзионные процессы в маточных трубах, ведущие к трубному бесплодию.
У беременных, больных хламидиозом, чаще наблюдаются осложнения: срочные роды, преждевременные роды, неразвивающаяся беременность, спонтанный выкидыш. Принято считать, что новорожденный в 40-50% случаев приобретает хламидийную инфекцию во время родов вследствие инфицирования патологическим материалом при прохождении через родовые пути больной хламидиозом матери (хламидии выделяли у новорожденных детей из конъюнктивы, носоглотки, среднего уха, трахеи, легких, прямой кишки и влагалища), однако возможно также проникновение инфекции в околоплодные воды и внутриутробное заражение плода.
Методы лабораторной диагностики урогенитальных хламидиозов
Основные принципы диагностики хламидийной инфекции те же, что и при другой бактериальной патологии. Тестовые процедуры включают в себя следующее:
Методы серологической диагностики хламидиоза основаны на определении специфических антител в сыворотке крови, а также в секретах лиц, больных или имеющих хламидиоз в анамнезе. Интерпретацию результатов серологического обследования следует проводить в совокупности с анализом клинико-эпидемиологических данных, а также с учетом особенностей использованного серологического теста.
Для серодиагностики в настоящее время наиболее часто используют иммуноферментный анализ (ИФА на наличие антител). Общий принцип ИФА-дигностики следующий: антиген фиксируется на твердой поверхности, обрабатывается испытуемой сывороткой, а затем антивидовым иммуноглобулином, связанным с ферментом, визуализирующимся после добавления субстрата. Достоинством метода является возможность автоматического учета результатов и выявления классов антител — IgG, IgA, IgM. Учитывая низкую иммуногенность «урогенитальных штаммов» хламидий и возможность присутствия антител после ранее перенесенной хламидийной инфекции, необходимо исследовать несколько проб сыворотки в динамике заболевания с интервалом в 2–3 недели.
Общеупотребительным методом серодиагностики является реакция непрямой иммунофлюоресценции для выявления антител (НИФ). При проведении НИФ используются фиксированные очищенные антигены хламидий, нанесенные в виде точек на стекло. Нанесенная сыворотка больных реагирует с антигенами различных серотипов, после чего обрабатывается антивидовой люминесцирующей сывороткой. Тест чувствителен, во многих случаях дает информацию о серотипе хламидий; целесообразно его применение при эпидемиологических исследованиях.
Методы амплификации нуклеиновых кислот
Методы ДНК диагностики основаны на комплементарном взаимодействии нуклеиновых кислот, которое позволяет с высокой точностью идентифицировать последовательность нуклеотидов в генах искомого микроорганизма. Из многочисленных модификаций данного метода следует выделить полимеразную цепную реакцию (ПЦР) и лигазную цепную реакцию как получившие наибольшее распространение.
Лечение урогенитального хламидиоза
Терапия заболеваний органов мочеполового тракта, вызванных хламидиями, основана на применении лекарственных препаратов, активных в отношении этого микроорганизма. В то же время следует учитывать и биологические особенности хламидий. Они обладают не только высоким тропизмом к эпителиальным клеткам очагов поражения, но и персистируют в особых мембраноограниченных зонах эпителия, что является предпосылкой для переживания возбудителями периода лекарственной терапии. С этим могут быть связаны неудачи в лечении, а также возможность перехода заболевания в асимптомное и латентное состояние. Поэтому в ходе лечения используются не только этиотропные, но и патогенетические средства. Все лица, у которых обнаружены хламидии, независимо от выраженности клинической картины подлежат лечению, целесообразно также лечение их половых партнеров. Во всех случаях терапия этой инфекции, вне зависимости от применяемой методики, предполагает профилактику развития кандидоза, в том числе применение на протяжении всего курса терапии нистатина и леворина в суточной дозе 2 млн. ЕД или низорала по 0,2 г дважды в день или пимафуцина по 0,2 г дважды в день.
Этиотропным действием по отношению к хламидийной инфекции обладают препараты тетрациклинового ряда, антибиотики-макролиды, рифампицин, джозамицин, а также фторхинолоны. Для этиотропной терапии используются курсы лечения продолжительностью от 7 до 14 дней. При неосложненной инфекции у мужчин и женщин лечение следует назначать с применением антибиотика. При вялотекущих торпидных формах инфекции лечение, как правило, должно быть комплексным. При лечении таких больных в стационаре назначению антибиотика должны предшествовать иммунотерапия и местное лечение. В амбулаторных условиях в целях предотвращения распространения инфекции антибиотик назначается одновременно с иммунотерапией (полиоксидоний или циклоферон) с последующим проведением местного лечения. При лечении беременных женщин назначают эритромицин по 0,5 г внутрь после еды через каждые 6 ч в течение 7 дней.
Препаратами первого выбора являются азитромицин и доксициклин. Высокая эффективность доксициклина при хламидийной инфекции и его низкая стоимость сохраняет за ним приоритет при лечении урогенитального хламидиоза.
Доксициклин (вибрамицин, юнидокс солютаб). Больным неосложненными формами хламидиоза препарат назначается внутрь: первый прием 0,2 г, затем через каждые 12 часов по 0,1 г. Курс лечения 7-14 дней, всего на курс 1,5-3,0 г. Удачное сочетание химической формулы (моногидрат) и лекарственной формы (солютаб) делает препарат юнидокс солютаб наиболее безопасным, а лечение с его помощью отличается наиболее высокой комплаентностью среди всех известных доксициклинов.
Азитромицин (сумамед). При неосложненном хламидиозе назначается однократно 1,0 г препарата. При вялом течении рекомендуется следующая схема приема сумамеда: 1-й день 1,0 г однократно, 2-3-й дни по 0,5 г, 4-7-й дни по 0,25 г, всего 3,0 г.
Метациклин (рондомицин). При острых и неосложненных формах назначается внутрь после еды в дозе 600 мг (первый прием), затем по 300 мг через каждые 8 ч в течение 7 дней, на курс лечения 6,6 г. При остальных формах курс лечения удлиняется до 10 дней.
Клацид (кларитромицин). При неосложненных формах хламидиоза назначается по 250 мг дважды в день в течение 7 дней, при хронической — 12-14 дней по 400 мг один раз в сутки.
Пефлоксацин (абактал). При свежем неосложненном хламидиозе назначают внутрь по 600 мг один раз в сутки в течение 7 дней. При хроническом — в течение 10-12 дней.
Ломефлоксацин (максаквин). При свежей неосложненной форме хламидиоза рекомендуется по 600 мг один раз в сутки в течение 7 дней, при хроническом — в течение 10-11 дней.
Ципрофлоксацин (ципробай, сифлокс). При неосложненных и осложненных формах хламидиоза назначают внутрь в течение 10 дней, первый прием 500 мг, последующие через 12 часов по 250 мг; на курс 5,0 г.
Джозамицин (вильпрафен). При неосложненном хламидиозе назначают внутрь в течение 7 дней по 500 мг через каждые 12 ч; на курс 7,0 г.
Лечение детей проводят теми же препаратами, учитывая противопоказания, в дозах, определяемых в соответствии с возрастом; чаще используются местные процедуры: сидячие ванны из настоя цветов ромашки или шалфея (одна столовая ложка на один стакан кипятка), или раствора марганцовокислого калия два раза в день, или спринцевания теми же настоями и растворами, а также общеукрепляющее лечение.
У больных урогенитальным хламидиозом, особенно при длительном, рецидивирующем его течении, повторном или нерациональном использовании антимикробных препаратов, выявляются нарушения микробиоценоза кишечника, что в свою очередь негативно воздействует на течение физиологических процессов и реактивность организма.
Установление диагноза кишечного дисбактериоза основывается на результатах бактериологических исследований фекалий в совокупности с клиническими проявлениям, после чего проводится медикаментозная коррекция дисбактериоза.
Трихомониаз
Урогенитальный трихомониаз — широко распространенное инфекционное воспалительное заболевание, передаваемое половым путем, вызывается простейшим Trichomonas vaginalis.
Урогенитальная трихомонада впервые была описана в 1836 г. парижским врачом A. Donne, обнаружившим ее в выделениях из влагалища у женщин, больных гонореей и сифилисом. Он дал ей видовое название Trichomonas vaginale. Французский паразитолог С. Davaine (1854) выделил из испражнений больного холерой другого жгутиконосца, морфологически сходного с урогенитальной трихомонадой, которому он дал название Trichomonas intestinalis — кишечная трихомонада. Киевский врач С. Штейнберг в 1862 г. описал ротовую трихомонаду — Trichomonas elongata, которая выявлялась в белом мягком веществе, накапливающемся на зубах. Таким образом, у человека паразитируют три вида трихомонад: урогенитальная, ротовая и кишечная.
Урогенитальные трихомонады бывают трех форм: грушевидной, амебоидной и почкующейся; последняя встречается реже других. Основной считается грушевидная форма, а остальные представляют собой промежуточные стадии жизненного цикла трихомонады, вне человеческого организма малоустойчивы. Обязательным условием их жизнеспособности является наличие влаги, при высушивании они быстро погибают. Эти простейшие неустойчивы также ко многим другим факторам окружающий среды: повышение температуры более 40°С, прямые солнечные лучи, изменение осмотического давления, воздействие антисептических средств и т. п.
Урогенитальные трихомонады, в результате эволюции приспособившиеся к паразитизму, способны поражать слизистые оболочки мочеполового тракта, а также эпителий кожи половых органов, вызывая язвы и эрозии. По мелким складкам на уздечке головки члена и шейке матки патологический материал попадает в уретру и цервикальный канал, постепенно per continuitatum распространяется по поверхности слизистых оболочек, а затем через межклеточные пространства попадает в субэпителиальную соединительную ткань, вызывая воспалительную реакцию. Распространяясь по слизистой оболочке уретры, трихомонады поражают лакуны и железы, проникают в лимфатические щели и сосуды, переносятся в придаточные половые железы, вызывая в них воспалительные изменения.
Мочеполовой трихомониаз является многоочаговым заболеванием, при котором урогенитальные трихомонады могут локализоваться во всех мочеполовых органах.
Урогенитальные трихомонады, попавшие на слизистую оболочку уретры во время полового акта, держатся в первые 12-24 ч на поверхности ладьевидной ямки, выстланной плоским эпителием. Размножаясь, они стелются, как плющ, по поверхности, но не проникают в щели плоского эпителия. В ответ на внедрившуюся инфекцию появляется активная гиперемия, которая выражается в припухлости и покраснении губок наружного отверстия уретры, а субъективно больной ощущает зуд и легкое щекотание. По мере размножения и распространения урогенитальных трихомонад вдоль слизистой оболочки уретры они достигают мест, выстланных цилиндрическим эпителием, примерно через 24-36 ч. С вовлечением в воспалительный процесс цилиндрического эпителия происходит просачивание через стенки сосудов серозной жидкости, которая разрыхляет связь между эпителиальными клетками и соединительной тканью. Нарушается нормальное состояние сосудистых стенок, начинается обильная миграция лейкоцитов с инфильтрацией ими верхних слоев подэпителиальной ткани.
Под влиянием урогенитальных трихомонад эпителий уретры травмируется, дегенерирует; нарушается взаимная связь между клетками и их питание, эпителий слущивается вплоть до образования эрозий и язв. Последние возникают за счет воздействия протеолитических ферментов простейших на эпителиальные клетки и подэпителиальную ткань. Слизистая оболочка уретры припухает, утолщается, теряет свою эластичность, легко кровоточит.
Полости желез и выводных протоков наполняются лейкоцитами и размножающимися урогенитальными трихомонадами.
При отсутствии лечения через 3-4 недели воспалительные явления начинают стихать, выделения прекращаются или же наблюдаются только по утрам, после обильного употребления алкоголя или полового акта. Происходит метаплазия эпителиального покрова слизистой оболочки уретры: вместо дегенерированного слущивающегося цилиндрического эпителия образуется многослойный плоский.
Клиника
Клиническое течение трихомониаза не отличается от такового при воспалительных заболеваниях мочеполовых органов другой этиологии и часто напоминает гонорею.
О длительности инкубационного периода трихомониаза нет единого мнения. В доступной нам литературе приводятся разные данные: от 3 дней до 3-4 недель и даже 55 дней.
Большое практическое значение приобретает вопрос о классификации трихомониаза. С целью назначения правильного лечения в основу классификации, как и при гонорее, положена интенсивность реакции организма на внедрение урогенитальных трихомонад, отражением которой является клиническое проявление болезни. С этой точки зрения целесообразно различать следующие формы трихомониаза.
К свежим формам трихомониаза следует относить случаи с давностью заболевания до 2 месяцев с выраженными и умеренно выраженными воспалительными процессами мочеполовой сферы человека. К хроническим формам трихомониаза относят вялотекущие случаи заболевания (более 2 месяцев или если сроки начала заболевания неизвестны). К трихомонадоносительству следует отнести случаи, когда воспалительные реакции в организме отсутствуют, но при половой близости урогенитальные трихомонады передаются здоровым лицам, вызывая у них типичную клиническую картину заболевания.
Трихомониаз следует классифицировать и по локализации воспалительных явлений.
Основными очагами поражения при урогенитальном трихомониазе являются мочеиспускательный канал у мужчин, влагалище и уретра у женщин. У женщин в воспалительный процесс могут вовлекаться большие вестибулярные и парауретральные железы, шейка матки. Трихомонады обнаруживаются в полости матки, в сактосальпинксах, кистах яичников. Имеются сообщения о связи урогенитального трихомониаза с осложнениями беременности (преждевременные роды, ранний разрыв плодного пузыря и др.). Клиническая картина неосложненного урогенитального трихомониаза у женщин характеризуется наличием воспалительного процесса во влагалище и влагалищной части шейки матки. В дальнейшем может присоединиться вестибулит, парауретрит, эндоцервицит, эндометрит и др., что рассматривается как осложненное течение заболевания.
У мужчин трихомонады могут вызывать поражение предстательной железы, семенных пузырьков, придатков яичек, куперовых желез.
Может развиваться восходящая инфекция мочевыводящих путей и почек (цистит, пиелит, пиелонефрит). Осложнения при трихомонадных уретритах у мужчин встречаются чаще, чем при гонорее. Клиническая картина трихомонадных простатитов, везикулитов, эпидидимитов отличается от таковой гонорейной этиологии, протекающей, как правило, более бурно. При затяжном течении возможно образование одиночных или множественных стриктур уретры. У девочек урогенитальный трихомониаз протекает с поражением вульвы и влагалища.
Лабораторная диагностика
Диагноз урогенитального трихомониаза устанавливается при обязательном обнаружении Т.vaginalis путем лабораторного исследования. Для лабораторной диагностики трихомониаза применяются скопические методы и культуральное исследование. Из-за общности путей заражения урогенитальный трихомониаз нередко сочетается с другими заболеваниями, передаваемыми половым путем, в связи с чем больных следует подвергать соответствующему обследованию. В случае сопутствующих урогенитальных инфекций (ассоциаций) их лечение проводится одновременно.
Наиболее широко распространенным, но недостаточно чувствительным методом при лабораторной диагностике трихомониаза является микроскопическое изучение нативных или окрашенных препаратов. При исследовании нативного препарата патологический материал помещают в каплю теплого изотонического раствора хлорида натрия на предметном стекле, тщательно перемешивают, накрывают покровным стеклом и немедленно исследуют в микроскопе с объективом 40. Лучшие результаты дает просмотр нативного препарата в микроскопе с темнопольным конденсором, т. к. при этом обнаруживаются единичные и слабоподвижные особи в скоплениях клеточных элементов за счет хорошо видимого движения жгутиков. В нативном препарате для трихомонад характерна овальная или округлая форма, наличие жгутиков и толчкообразные движения простейших.
При исследовании нативных препаратов следует помнить о возможности нахождения в моче жгутиковых простейших семейства бодонидов. В отличие от трихомонад они обладают меньшим размером и имеют лишь два жгутика, что обусловливает их быстрое поступательное движение по прямой. К ошибкам в распознавании трихомонад может привести и наличие в препарате лейкоцитов в сочетании с большим числом хорошо подвижных палочек, прикрепляющихся к ним.
С целью обнаружения влагалищных трихомонад в окрашенных препаратах используют многочисленные методы окраски, в частности метиленовым синим, генцианом фиолетовым, по способам Грама, Романовского-Гимза, Лейшмана-Романовского и др. Широкое применение метиленового синего обусловлено тем, что его используют и для окраски мазков на гонококк. Изучение окрашенных мазков позволяет определить морфологию возбудителя, мазки не требуют немедленного исследования, что особенно важно при массовом обследовании на трихомониаз. Однако возможны диагностические ошибки, поскольку эпителиальные клетки могут быть приняты за трихомонады.
Культуральный метод диагностики трихомониаза является более достоверным и чувствительным по сравнению с микроскопическим исследованием. В большей степени его эффективность зависит от качества используемых питательных сред. В состав предложенных сред с высокими ростовыми свойствами входят мясо-пептонный бульон (МПБ), препараты печени, минеральные соли, сахара, сыворотка крови человека или животных, соляно-кислый цистеин и другие ингредиенты.
Лечение
Мочеполовой трихомониаз протекает часто как смешанная протозойно-бактериальная болезнь с вовлечением в воспалительный процесс многих органов мочеполового тракта. Ввиду этого при лечении данного заболевания целесообразно использовать комплексную терапию. Помимо протистоцидных препаратов применяют антибиотики, иммунотерапию, витаминотерапию, биогенные стимуляторы и др. Широко используется и местное лечение: промывание и инстилляции уретры, ванночки и протирания влагалища у женщин и т. п. Диспансерное наблюдение у женщин, перенесших трихомониаз, должно проводиться в течение не менее двух менструальных циклов. Если источник заболевания трихомониазом неизвестен, динамическое врачебное наблюдение за лицами, болевшими урогенитальным трихомониазом, производится в течение 6 месяцев с ежемесячными анализами крови на классические серологические реакции. Этот срок необходим для профилактики и своевременного выявления сифилиса ввиду того, что препараты, применяемые при лечении трихомониаза, обладают и трепонемоцидным действием.
Основными препаратами для лечения трихомониаза являются:
Метронидазол (трихопол, флагил, клион). Обладает выраженным действием в отношении урогенитальных трихомонад. Важной особенностью этого средства является его активность при приеме внутрь; препарат быстро всасывается и накапливается в крови в концентрациях, губительных для трихомонад. Метронидазол широко применяют для лечения острого и хронического трихомониаза у мужчин и женщин. Препарат выпускается в таблетках по 0,25 и 0,5 г и в форме влагалищных свечей и таблеток по 0,5 г.
Первая схема приема препарата: в 1-й день по 2 таблетки (0,5 г) три раза в день с интервалом 8 ч. Затем суточная доза уменьшается ежедневно на 1 таблетку с этим же интервалом. На курс общая доза — 3,75 г в течение 6 дней. По второй схеме назначают по 0,25 г два раза в день с интервалом 12 ч; эта схема предусматривает дополнительное введение по 1 вагинальной свече или таблетке, содержащей 0,5 г метронидазола. Препарат применяют в течение 10 дней внутрь и местно. При необходимости курс лечения повторяют через месяц.
Тинидазол (фасижин, триконидазол и др.). По структуре и действию близок к метронидазолу. Назначают внутрь в таблетках по 0,5 г. Схема приема тинидазола: 1) однократно в дозе 2 г (4 таблетки); 2) по 0,5 г каждые 15 мин в течение 1 ч. Противопоказания те же, что и для метронидазола: 1-й триместр беременности и период кормления грудью ребенка, нарушения кроветворения, активные заболевания ЦНС. Во время лечения нельзя принимать спиртные напитки. До и во время лечения необходимо производить анализы крови.
Клиндамицин — перорально по 300 мг два раза в день.
Солкотриховак — 0,5 мл внутримышечно, три инъекции с интервалом в 2 недели, затем через год 0,5 мл однократно.
При наличии показаний рекомендуется назначать патогенетическую и местную терапию.
К установлению критериев излеченности мочеполового трихомониаза npиступают через 7-10 дней после завершения лечения с помощью микроскопического и культурального методов исследования.
Местное лечение. При свежих неосложненных трихомонадных поражениях нет необходимости в местном лечении, т. к. для ликвидации воспалительных явлений достаточно общего. При торпидно протекающих свежих воспалительных процессах и хронических формах трихомониаза назначается местное лечение.
Местнодействующие препараты применяются одновременно с протистоцидными препаратами общего действия.
Метронидазол — вагинальные шарики (таблетки) по 0,5 г назначаются один раз в сутки интравагинально в течение 6 дней.
Орнидазол — вагинальные таблетки по 0,5 г вводятся во влагалище однократно в течение 3-6 дней.
Гиналгин — 1 таблетка интравагинально в течение 10 дней.
Клиндамицин — 2%-ный вагинальный крем применяется ежедневно в течение 4 дней подряд.
Клион Д (метронидазол) — вагинальные таблетки по 0,1 5 дней.
Атрикан (тенонитрозол) — по 250 мг два раза в день 4 дня.
Для местного лечения применяют также инстилляции уретры 0,25-0,5%-ным раствором нитрата серебра через день 2%-ным раствором протаргола или 1%-ным раствором колларгола.
Лечение беременных. Лечение осуществляется метронидазолом (исключая 1-й триместр беременности) в дозе 2,0 г перорально однократно.
Лечение детей. Метронидазол назначают детям в возрасте от 1 до 5 лет перорально по 1/3 таблетки, содержащей 250 мг, два-три раза в сутки; 6-10 лет — по 0,125 г два раза сутки; 11-15 лет — по 0,25 г два раза в сутки в течение 7 дней.
