Гидрохлорид по молекуле hcl что это
ХЛОРИСТЫЙ ВОДОРОД: характеристики, ПДК, методики
Характеристики вещества в каталоге загрязняющих веществ от группы компаний «Лаборатория».
Химическое название вещества по IUPA : гидрохлорид.
Структурная формула : HCl
Синонимы : водород хлорид; Hydrochloric acid; Hydrogen chloride. Соляная кислота, Водород хлорид
Код загрязняющего вещества : 316
Агр.состояние : жидкость/газ
Класс опасности : 316
ОБУВ (ориентировочный безопасный уровень воздействия): –
ЛОС : –
РПОХВ : АТ-000238
CAS : 7647-01-0
RTECS : MW4025000
EC : 231-595-7
ПДК м.р. (предельно допустимая концентрация в атмосферном воздухе максимальная разовая): 0,2 мг/м³
ПДК с.с. (предельно допустимая концентрация в атмосферном воздухе среднесуточная): 0,1 мг/м³
Лимитирующий показатель : рефл.-рез.
Класс опасности : 2
ПДК р.з. (предельно допустимая концентрация в воздухе рабочей зоны максимальная разовая): 5 мг/м³
Класс опасности : 2
Особенности действия на организм : 0
Применяется на производствах : химическая промышленность.
Диапазоны определения вещества «ХЛОРИСТЫЙ ВОДОРОД» в промышленных выборсах, воздухе рабочей зоны, атмосферном воздухе различаются и определяются методиками исследования. Список методик смотрите ниже.
Соляная Кислота
Химическое название
Химические свойства
Хлороводородная кислота, хлористый водород или хлористоводородная кислота – раствор НСl в воде. Согласно Википедии, вещество относят у группе неорганических сильных одноосновных к-т. Полное название соединения на латинском: Hydrochloricum acid.
Химические свойства Соляной Кислоты. С чем реагирует Соляная Кислота? Вещество вступает во взаимодействие с металлами, которые стоят в ряду электрохимических потенциалов перед водородом (железо, магний, цинк и другие). При этом образуются соли и выделяется газообразный H. С Соляной Кислотой не реагирует свинец, медь, золото, серебро и другие металлы правее водорода. Вещество вступает в реакцию с оксидами металлов, при этом образуя воду и растворимую соль. Гидроксид натрия под действием к-ты образует хлорид натрия и воду. Реакция нейтрализации характерна для данного соединения.
Разбавленная Соляная Кислота реагирует с солями металлов, которые образованы более слабыми к-ами. Например, пропионовая кислота слабее, чем соляная. Вещество не взаимодействует с более сильными кислотами. Карбонат кальция и карбонат натрия будут образовывать после реакции с HCl хлорид, угарный газ и воду.
Для химического соединения характерны реакции с сильными окислителями, с диоксидом марганца, перманганатом калия: 2KMnO4 + 16HCl = 5Cl2 + 2MnCl2 + 2KCl + 8H2O. Вещество реагирует с аммиаком, при этом образуется густой белый дым, который состоит из очень мелких кристаллов хлорида аммония. Минерал пиролюзит с Соляной Кислотой также вступает в реакцию, так как содержит диоксид марганца: MnO2+4HCl=Cl2+MnO2+2H2O (реакция окисления).
Существует качественная реакция на хлороводородную кислоту и ее соли. При взаимодействии вещества с нитратом серебра выпадает белый осадок хлорида серебра и образуется азотная к-та. Уравнение реакции взаимодействия метиламина с хлористым водородом выглядит следующим образом: HCl + CH3NH2 = (CH3NH3)Cl.
Вещество реагирует со слабым основанием анилином. После растворения анилина в воде к смеси прибавляют Соляную Кислоту. В результате основание растворяется и образует солянокислый анилин (хлорид фениламмония): (С6Н5NH3)Cl. Реакция взаимодействия карбида алюминия с хлористоводородной к-ой: Al4C3+12HCL=3CH4+4AlCl3. Уравнение реакции карбоната калия с к-той выглядит следующим образом: K2CO3 + 2HCl = 2KCl + H2O + CO2.
Получение соляной кислоты
Чтобы получить синтетическую Соляную Кислоту сжигают водород в хлоре, а затем полученный газообразный хлороводород растворяется в воде. Также распространено производство реактива из абгазов, которые образуются в виде побочных продуктов при хлорировании углеводородов (абгазная Соляная Кислота). При производстве данного химического соединения применяют ГОСТ 3118 77 – на реактивы и ГОСТ 857 95 – для технической синтетической хлористоводородной кислоты.
В лабораторных условиях можно применять давний способ, при котором поваренная соль подвергается действию концентрированной серной к-ты. Также средство можно получить с помощью реакции гидролиза хлорида алюминия или магния. Во время реакции могут образоваться оксихлориды переменного состава. Для определения концентрации вещества применяют стандарт титры, которые выпускаются в запаянных ампулах, чтобы в последствии можно было получить стандартный раствор известной концентрации и использовать его для определения качества другого титранта.
У вещества имеется достаточно широкая область применения:
Данное химическое соединение имеет высокий класс опасности – 2 (по ГОСТу 12Л.005). При работе с кислотой требуется спец. защита кожи и глаз. Достаточно едкое вещество при попадании на кожу или в дыхательные пути вызывает химические ожоги. Для ее нейтрализации применяют растворы щелочи, чаще всего – питьевую соду. Пары хлороводорода образуют с молекулами воды в воздухе едкий туман, который раздражает дыхательные пути и глаза. Если вещество вступает в реакцию с хлорной известью, перманганатом калия и прочими окислителями, то образуется токсичный газ — хлор. На территории РФ ограничен оборот Соляной Кислоты с концентрацией более 15%.
Фармакологическое действие
Повышает кислотность желудочного сока.
Фармакодинамика и фармакокинетика
Что такое кислотность желудочного сока? Это характеристика концентрации Соляной Кислоты в желудке. Кислотность выражается в рН. В норме в составе желудочного сока должна вырабатываться кислота и принимать активное участие в процессах пищеварения. Формула хлороводородной кислоты: HCl. Ее продуцируют париетальные клетки, расположенные в фундальных железах, с участием Н+/К+-АТФазы. Эти клетки выстилают дно и тело желудка. Кислотность желудочного сока сама по себе изменчива и зависит от числа париетальых клеток и интенсивности процессов нейтрализации вещества щелочными компонентами желудочного сока. Концентрация продуцируемой к-ты стабильна и равняется 160 ммоль/л. У здорового человека в норме должно вырабатываться не более 7 и не менее 5 ммоль вещества в час.
При недостаточной или избыточной выработке Соляной Кислоты возникают заболевания пищеварительного тракта, ухудшается способность усваивать некоторые витамины и микроэлементы, например, железо. Средство стимулирует выделение желудочного сока, снижает рН. Активирует пепсиноген, переводит его в активный фермент пепсин. Вещество благоприятно воздействует на кислотный рефлекс желудка, замедляет переход не до конца переваренной пищи в кишечник. Замедляются процессы брожения содержимого пищеварительного тракта, исчезает боль, изжога и отрыжка, лучше усваивается железо.
После приема внутрь средство частично метаболизируется слюной и желудочной слизью, содержимым 12-перстной кишки. Несвязанное вещество проникает в 12-перстную кишку, где полностью нейтрализуется ее щелочным содержимым.
Показания к применению
Вещество входит в состав синтетических моющих средств, концентрата для полоскания ротовой полости ухода за контактными линзами. Разбавленная Соляная Кислота назначается при заболеваниях желудка, сопровождающихся пониженной кислотностью, при гипохромной анемии в сочетании с препаратами железа.
Противопоказания
Лекарство нельзя применять при аллергии на синтетическое вещество, при болезнях пищеварительного тракта, ассоциированных с повышенной кислотностью, при остром гастрите.
Побочные действия
Концентрированная Соляная Кислота при попадании на кожу, в глаза и дыхательные пути может вызывать сильные ожоги. В составе различных лек. препаратов используют разбавленное вещество, при длительном применении больших дозировок может возникнуть ацидоз, ухудшение состояния эмали зубов.
Инструкция по применению (Способ и дозировка)
Хлороводородную кислоту применяют в соответствии с инструкцией.
Внутрь лекарство назначают, предварительно растворив в воде. Обычно используют 10-15 капель препарата на пол стакана жидкости. Лекарство принимают во время еды, 2-4 раза в день. Максимальная разовая дозировка составляет 2 мл (около 40 капель). Суточная доза – 6 мл (120 капель).
Передозировка
Случаи передозировки не описаны. При бесконтрольном приеме вещества внутрь в больших количествах возникают язвы и эрозии в пищеварительном тракте. Следует обратиться за помощью к врачу.
Взаимодействие
Вещество часто используют в комбинации с пепсином и прочими лек. препаратами. Химическое соединение в пищеварительном тракте вступает во взаимодействие с основаниями и некоторыми веществами (см. химические свойства).
Особые указания
При лечении препаратами Соляной Кислоты необходимо четко придерживаться рекомендаций в инструкции.
Свойства хлороводорода, способы получения
Хлороводород — что это такое, формула
Хлороводород — это бесцветный газ с резким неприятным запахом.
Формула: HCl
Строение его молекулы определяет название соединения. Атомы хлора и водорода соединены ковалентной полярной связью.
Физические и химические свойства
Раствор хлороводорода в воде называют соляной кислотой. Процесс растворения можно описать с помощью следующего уравнения реакции:
При растворении хлороводорода выделяется большое количество теплоты.
Соляную кислоту относят к сильным одноосновным кислотам. Соединение активно вступает в химические реакции со следующими веществами:
В результате такого взаимодействия формируются соли соляной кислоты — хлориды:
M g + 2 H C l → M g C l 2 + H 2 ↑
F e O + 2 H C l → F e C l 2 + H 2 O
В присутствии сильных окислителей или в процессе электролиза хлороводород способен проявлять свойства восстановителя, при этом окисляясь с выделением газообразного хлора:
M n O 2 + 4 H C l → M n C l 2 + C l 2 ↑ + 2 H 2 O
В условиях повышенной температуры происходит окисление хлороводорода кислородом в присутствии катализатора, роль которого играет хлорид меди ( I I ) C u C l 2 :
4 H C l + O 2 → 2 H 2 O + 2 C l 2 ↑
Концентрированная соляная кислота взаимодействует с медью, что сопровождается образованием комплекса одновалентной меди:
2 C u + 4 H C l → 2 H [ C u C l 2 ] + H 2 ↑
Смесь, в состав которой входят три объемные части концентрированной соляной кислоты и одна объемная часть концентрированной азотной кислоты, носит название «царская водка». Данная смесь способна растворять золото и платину.
«Царская водка» характеризуется высокой окислительной способностью, что объясняется наличием в составе смеси хлористого нитрозила N O C l и хлора, находящихся в равновесии с исходными веществами:
За счет большого содержания хлорид-ионов в растворе происходит связывание металла. В результате образуется хлоридный комплекс, что является причиной его растворения:
3 P t + 4 H N O 3 + 18 H C l → 3 H 2 [ P t C l 6 ] + 4 N O + 8 H 2 O
В процессе присоединения хлороводорода к серному ангидриду происходит образование хлорсульфоновой кислоты H S O 3 C l :
S O 3 + H C l → H S O 3 C l
Хлороводород вступает в реакции присоединения по кратным связям в органических соединениях (электрофильное присоединение):
Взаимодействие с основаниями
Соляная кислота взаимодействует практически со всеми основаниями. При этом протекают реакции ионного обмена, в результате которых получают соль и воду:
При смешении соляной кислоты с аммиаком протекает реакция присоединения. В результате взаимодействия образуется соль в виде хлорида аммония. Уравнение реакции будет выглядеть так:
H C l + N H 3 → N H 4 C l
Соляная кислота также вступает в реакцию с амфотерными гидроксидами, которые в данном случае проявляют основные свойства. Взаимодействие с гидроксидом цинка:
2 H C l + Z n ( O H ) 2 → Z n C l 2 + 2 H 2 O
Способы получения, область применения
Лабораторный способ получения хлористого водорода заключается в реакции концентрированной серной кислоты с твердым хлоридом натрия (поваренной солью) в условиях повышенной температуры:
N a C l + H 2 S O 4 → N a H S O 4 + H C l ↑
P C l 5 + H 2 O → P O C l 3 + 2 H C l
R C O C l + H 2 O → R C O O H + H C l
Устаревший промышленный способ получения хлористого водорода заключался в методике Леблана. В процессе реакции твердый хлорид натрия взаимодействует с концентрированной серной кислотой.
В современной промышленности хлороводород производят с помощью прямого синтеза из простых веществ:
В промышленных масштабах хлористый водород производят на специальных установках путем сжигания водорода в хлоре. Причем водород попадает в пламя в небольшом избытке. Тогда весь объем подаваемого хлора реагирует, и на выходе получается продукт более высокого качества.
Газообразный хлороводород практически не используется из-за его физических и химических характеристик. Широкое применение находит соляная кислота:
Техника безопасности
При попадании хлороводорода в дыхательные пути может наступить сильное удушье. А его водный раствор высокой концентрации вызывает химические ожоги. Поэтому работать с хлористым водородом и соляной кислотой следует только в маске (респираторе), защитных перчатках и очках.
При вдыхании газа необходимо немедленно вывести пострадавшего на воздух и при необходимости сделать искусственное дыхание. В случае проглатывания соляной кислоты требуется промывание желудка.
Если кислота попала на кожу, пораженный участок следует промыть водой и обработать слабым раствором соды, который нейтрализуют кислоту. В случае попадания на слизистые оболочки после промывания нужно закапать глаза, нос или горло раствором новокаина и дикаина с адреналином.
720 г / л (20 ° С)
561 г / л (60 ° С)
4416 частей на миллион (кролик, 30 мин)
4416 частей на миллион (морская свинка, 30 мин)
3000 частей на миллион (человек, 5 мин) [7]
В сложный хлористый водород имеет химическая формула ЧАС Cl и как таковой галогенид водорода. В комнатная температура, это бесцветный газ, который образует белые пары соляная кислота при контакте с атмосферным водяной пар. Газообразный хлористый водород и соляная кислота важны в технологии и промышленности. Соляная кислота, водный раствор хлористого водорода, также обычно дают формулу HCl.
Содержание
Реакции
При контакте, H2O и HCl объединяются с образованием гидроксоний катионы ЧАС3О + и хлористый анионы Cl − через обратимый химическая реакция:
Полученное решение называется соляная кислота и является сильная кислота. В кислотная диссоциация или константа ионизации, Kа, является большим, что означает, что HCl практически полностью диссоциирует или ионизируется в воде. Даже в отсутствие воды хлористый водород может действовать как кислота. Например, хлористый водород может растворяться в некоторых других растворителях, таких как метанол и протонировать молекулы или ионы, а также могут служить кислотойкатализатор для химических реакций, где безводный (безводные) условия желательны.
Из-за своей кислой природы хлористый водород коррозионное вещество, особенно в присутствии влаги.
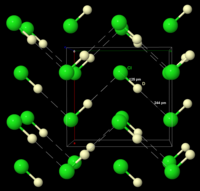
Структура и свойства
Замороженная HCl претерпевает фазовый переход при 98,4 К. Порошковая дифракция рентгеновских лучей замороженного материала показывает, что материал изменяется от ромбический структура к кубический один во время этого перехода. В обеих структурах атомы хлора находятся в гранецентрированный массив. Однако определить местонахождение атомов водорода не удалось. [9] Анализ спектроскопических и диэлектрических данных, а также определение структуры DCl (хлорида дейтерия) показывает, что HCl образует зигзагообразные цепочки в твердом теле, как и HF (см. рисунок справа). [10]
| Температура (° C) | 0 | 20 | 30 | 50 |
|---|---|---|---|---|
| Вода | 823 | 720 | 673 | 596 |
| Метанол | 513 | 470 | 430 | |
| Этиловый спирт | 454 | 410 | 381 | |
| Эфир | 356 | 249 | 195 |
В инфракрасный спектр газообразного хлористого водорода, показанный слева, состоит из ряда резких линий поглощения, сгруппированных около 2886 см −1 (длина волны
3,47 мкм). При комнатной температуре практически все молекулы находятся в основном колебательном состоянии. v = 0. С учетом ангармонизма колебательную энергию можно записать как.
E v я б = час ν е ⋅ ( v + 1 2 ) + час Икс е ν е ⋅ ( v + 1 2 ) 2 < displaystyle E _ < mathrm
E ( J ) р о т = час ⋅ B ⋅ J ( J + 1 ) < Displaystyle Е (J) _ < mathrm
Значение вращательной постоянной B намного меньше колебательного νо, так что для вращения молекулы требуется гораздо меньшее количество энергии; для типичной молекулы это находится в микроволновом диапазоне. Однако колебательная энергия молекулы HCl помещает свое поглощение в инфракрасную область, что позволяет легко собирать спектр, показывающий колебательные переходы этой молекулы, используя инфракрасный спектрометр с газовой ячейкой. Последний может быть даже изготовлен из кварца, так как поглощение HCl находится в окне прозрачности для этого материала.
Обильный хлор состоит из двух изотопов: 35 Cl и 37 Cl в соотношении приблизительно 3: 1. Хотя пружинные постоянные почти идентичны, разнородные уменьшенные массы из H 35 Cl и H 37 Cl вызывает измеримые различия во вращательной энергии, поэтому при внимательном рассмотрении каждой линии поглощения наблюдаются дублеты, взвешенные в том же соотношении 3: 1.
Производство
Большая часть хлористого водорода, производимого в промышленных масштабах, используется для соляная кислота производство. [12]
Прямой синтез
Очень чистый хлористый водород получают путем объединения хлор и водород:
Поскольку реакция экзотермический, установка называется HCl печь или горелка HCl. Образующийся газообразный хлористый водород поглощен в деионизированная вода, в результате чего получается химически чистая соляная кислота. Эта реакция может дать очень чистый продукт, например для использования в пищевой промышленности.
Органический синтез
R − H + Cl2 → R − Cl + HCl R − Cl + HF → R − F + HCl
Образующийся хлористый водород либо используется повторно, либо поглощается водой, в результате чего получается соляная кислота технического или промышленного класса.
Лабораторные методы
Небольшие количества хлористого водорода для лабораторного использования могут образовываться в Генератор HCl путем дегидратации соляной кислоты либо серная кислота или безводный хлорид кальция. В качестве альтернативы HCl можно получить реакцией серной кислоты с хлоридом натрия: [13]
Эта реакция происходит при комнатной температуре. При условии, что в генераторе остается NaCl и он нагревается выше 200 ° C, реакция протекает дальше:
Для работы таких генераторов реагенты должны быть сухими.
Хлористый водород также может быть получен гидролиз некоторых реактивных хлоридных соединений, таких как хлориды фосфора, тионилхлорид (SOCl2), и ацилхлориды. Например, холодную воду можно постепенно капать на пентахлорид фосфора (PCl5) для получения HCl:
Приложения
Большая часть хлористого водорода используется в производстве соляной кислоты. Это также важный реагент в других промышленных химических превращениях, например:
В полупроводниковой промышленности он используется как для травления полупроводниковых кристаллов, так и для очистки кремний через трихлорсилан (SiHCl3).
История
Алхимики из Средний возраст узнал, что соляная кислота (тогда известная как дух соли или же Acidum Salis) выделяется парообразный хлористый водород, который получил название морской кислотный воздух. В 17 веке Иоганн Рудольф Глаубер использованная соль (хлорид натрия) и серная кислота для подготовки сульфат натрия, выделяя газообразный хлористый водород (см. производство выше). В 1772 г. Карл Вильгельм Шееле также сообщил об этой реакции и иногда приписывают ее открытие. Джозеф Пристли приготовил хлористый водород в 1772 г., а в 1810 г. Хэмфри Дэви установлено, что он состоит из водород и хлор. [14]
Вовремя Индустриальная революция, спрос на щелочной такие вещества как кальцинированной соды увеличился, и Николя Леблан разработал новый промышленный процесс производства кальцинированной соды. в Процесс Леблана, соль была преобразована в кальцинированную соду с использованием серной кислоты, известняка и угля, с получением хлористого водорода в качестве побочного продукта. Первоначально этот газ выпускался в воздух, но Щелочной акт 1863 г. запретил такой выпуск, поэтому производители кальцинированной соды абсорбировали отработанный газ HCl в воде, производя соляную кислоту в промышленных масштабах. Позже Процесс Харгривза был разработан, который похож на процесс Леблана, за исключением диоксид серы, вода и воздух используются вместо серной кислоты в реакции, которая в целом является экзотермической. В начале 20 века процесс Леблана был фактически заменен Сольвеевский процесс, который не давал HCl. Однако производство хлористого водорода продолжалось как стадия производства соляной кислоты.
Историческое использование хлористого водорода в 20 веке включает гидрохлорирование алкины в производстве хлорированных мономеры хлоропрен и винилхлорид, которые впоследствии полимеризованный сделать полихлоропрен (Неопрен) и поливинил хлорид (ПВХ) соответственно. При производстве винилхлорида, ацетилен (C2ЧАС2) гидрохлорируют путем добавления HCl через тройная связь C2ЧАС2 молекула, превращая тройку в двойная связь, давая винилхлорид.
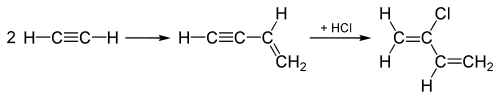
«Ацетиленовый процесс», использовавшийся до 1960-х годов для производства хлоропрен, начинается с объединения двух ацетилен молекул, а затем добавляет HCl к соединенному промежуточному продукту через тройная связь чтобы преобразовать его в хлоропрен, как показано здесь:
Этот «ацетиленовый процесс» был заменен процессом, который добавляет Cl2 к одной из двойных связей в 1,3-бутадиен вместо этого и последующее удаление вместо этого производит HCl, а также хлоропрен.
Безопасность
Соединенные штаты. Управление по охране труда и Национальный институт охраны труда и здоровья установили пределы профессионального воздействия хлористого водорода на уровне 5 частей на миллион (7 мг / м 3 ), [15] и собрал обширную информацию о проблемах безопасности на рабочем месте с использованием хлористого водорода. [16]
Смотрите также
Рекомендации
внешняя ссылка
Гидрид лития, LiH
ионный гидрид металла
Гидрид бериллия
Слева (газовая фаза): BeH2
ковалентный гидрид металла
Справа: (BeH2)п (твердая фаза)
полимерный гидрид металла
Боран и диборан
Слева: BH3 (особые условия), ковалентный металлоид гидрид
Справа: B2ЧАС6 (стандартные условия), димерный металлоид-гидрид
Метан, CH4
ковалентный гидрид неметалла
Аммиак, NH3
ковалентный гидрид неметалла
Вода, H2О
ковалентный гидрид неметалла
Фтороводород, HF
ковалентный гидрид неметалла