Герминальные мутации это что
Герминальные мутации ATM и BRCA1/2 позволяют различать риск летального и индолентного рака простаты и ассоциированы со смертью в раннем возрасте
Актуальность
Герминальные мутации BRCA1/2 и ATM были ассоциированы с риском рака предстательной железы (РПЖ).
Цель исследования
Дизайн, условия и участники исследования
Ретроспективное исследвование «случай-случай» с участием 313 пациентов, погибших от РПЖ, и 486 пациентов с локализованным РПЖ низкого риска европейского, африканского и китайского происхождения. Герминальная ДНК каждого из этих 799 пациентов была секвенирована на эти три гена.
Определение результатов и статистический анализ
Частота носительства мутации и их влияние на летальный РПЖ были проанализированы с использованием точного теста Фишера и регрессионного анализа Кокса соответственно.
Результаты и ограничения
Комбинированная частота носительства мутаций BRCA1/2 и ATM была значительно выше у пациентов с летальным РПЖ (6.07%), чем у пациентов с локализованным РПЖ (1.44%), p = 0.0007. Частота также значимо различалась у пациентов с летальным РПЖ как функция возраста на момент смерти (10.00%, 9.08%, 8.33%, 4.94% и 2.97% у пациентов, умерших в возрасте ≤ 60 лет, 61–65 лет, 66–70 лет, 71–75 лет и старше 75 лет соответственно, p = 0.046) и срока до смерти после установления диагноза (12.26%, 4.76% и 0.98% у пациентов, умерших за ≤ 5 лет, 6–10 лет и > 10 лет после установления диагноза РПЖ соответственно, p = 0.0006). Анализ выживаемости во всей когорте показал, что носительство мутации оставалось независимым предиктором летального РПЖ после контроля по расе и возрасту, простат-специфическому антигену и сумме Глисона на момент установления диагноза (отношение рисков = 2.13, 95%-ный доверительный интервал: 1.24–3.66, p = 0.004). Ограничением этого исследования является то, что другие гены репарации ДНК не были проанализированы.
Заключение
Статус мутаций BRCA1/2 и ATM отличает риски летального и индолентного РПЖ и ассоциирован с более ранним возрастом на момент смерти и меньшим сроком выживаемости.
Ключевые слова: летальный рак простаты, герминальный, мутация, гены репарации ДНК.
Germline Mutations in ATM and BRCA1/2 Distinguish Risk for Lethal and Indolent Prostate Cancer and are Associated with Early Age at Death
By: Rong Na, S. Lilly Zheng, Misop Han, Hongjie Yu, Deke Jiang, Sameep Shah, Charles M. Ewing, Liti Zhang, Kristian Novakovic, Jacqueline Petkewicz, Kamalakar Gulukota, Donald L. Helseth Jr, Margo Quinn, Elizabeth Humphries, Kathleen E. Wiley, Sarah D. Isaacs, Yishuo Wu, Xu Liu, Ning Zhang, Chi-Hsiung Wang, Janardan Khandekar, Peter J. Hulick, Daniel H. Shevrin, Kathleen A. Cooney, Zhoujun Shen, Alan W. Partin, H. Ballentine Carter, Michael A. Carducci, Mario A. Eisenberger, Sam R. Denmeade, Michael McGuire, Patrick C. Walsh, Brian T. Helfand, Charles B. Brendler, Qiang Ding, Jianfeng Xu, William B. Isaacs
European Urology, Volume 71 Issue 5, May 2017, Pages 740–747
Keywords: Lethal prostate cancer, Germline, Mutation, DNA repair genes
Молекулярные маркеры
Наследственные формы рака
Классическим примером гена-супрессора, осуществляющего негативную регуляцию клеточного цикла, является ген RB1. Наследственные формы рака молочной железы составляют около 5%. Мутации двух генов, BRCA1 и BRCA2, участвующих в репарации двухцепочечных разрывов, имеют практически равноценный вклад. Кроме рака молочной железы, герминальные мутации BRCA1 повышают риск возникновения рака яичников, а мутации BRCA2 предрасполагают к раку молочной железы у мужчин и раку поджелудочной железы. В то же время соматические мутации этих генов довольно редки при указанных новообразованиях. Спектр мутаций показывает, что их основная масса приводит к потери функции гена и представлена небольшими делециями и инсерциями, в том числе и в регуляторных областях генов. Две мутации BRCA1, 185delAG и 5382insC, составляют 20%, а мутации 617delT и 997del5 гена BRCA2 составляют почти 33%. Все мутации BRCA2, определяющие высокий риск развития рака яичников, локализуются в 3,3 т.п.н. экзона 11.
Наследственная форма неполипозного рака толстой кишки развивается в результате мутаций в генах MSH2 и MLH1, участвующих в образовании репарационных комплексов. Наиболее характерным признаком заболевания является нестабильность микросателлитных последовательностей. У женщин, имеющих герминальную мутацию в одном из этих генов, чаще всего возникают рак яичников и эндометрия. Среди мутаций MSH2 наиболее часто обнаруживается замена A→T в донорном сайте сплайсинга, приводящая к делеции 5 экзона. Для MLH1 преимущественного типа мутаций не показано, но установлено, что основным механизмом инактивации гена в опухолях является метилирование его промоторного района.
Предрасположенность к возникновению ретинобластомы обусловлена герминальной мутацией в одном из аллелей гена RB1, передающейся потомству по аутосомно-доминантному типу наследования с варьированием экспрессивности и неполной (90%) пенетрантностью. Опухоль развивается при инактивации неповрежденного аллеля гена, происходящей с высокой вероятностью в клетках сетчатки у детей в раннем возрасте или даже внутриутробно. Так как мишенью возникновения второй мутации могут быть и другие соматические клетки, то у пациентов, несущих герминальную мутацию в RB1, существует большой риск развития таких опухолей, как остеосаркома, лимфолейкоз, МРЛ, РМЖ, опухоли половых органов, поэтому за больными с наследственной формой заболевания необходимо наблюдение. Соматические мутации гена вызывают только ретинобластому, хотя нарушения функции RB1 обнаруживают во многих других опухолях, но уже как вторичные, являющиеся признаком дестабилизации генома опухолевой клетки.
Наследственные формы меланомы, синдрома диспластического невуса и атипичных родинок в ряде случаев вызываются герминальными мутациями гена-супрессора CDKN2A/p16. В семьях, несущих мутацию CDKN2A, кроме меланомы обнаруживаются опухоли поджелудочной железы, ОГШ. В то же время функциональная и структурная инактивация гена, обеспечивающего негативную регуляцию клеточного цикла путем ингибирования циклин-зависимых киназ, обнаруживается в различных типах опухолей, но преимущественно в мезотелиомах, спорадических меланомах и глиобластомах. Почти треть соматических мутаций гена представлена делециями, в то время как среди герминальных мутаций делеции и инсерции составляют не более 5%.
Нефробластома – генетически гетерогенное заболевание, но около трети случаев – результат инактивации гена-супрессора WT1.
Гемизиготные делеции хромосомного района 11p13 вызывают синдром WAGR, при котором кроме опухоли Вильмса обнаруживаются аномалии развития мочеполового тракта, аниридия и задержка физического и умственного развития.
Точковые мутации в 7-10 экзонах, кодирующих мотив цинковых пальцев, определяются у больных с синдромом Дениса-Драша, для которого характерна прогрессирующая нефропатия, псевдогермафродитизм, нефро— и гонадобластомы. Соматические точковые и структурные мутации гена выявлены в мезотелиомах, десмопластических мелко-кругло-клеточных опухолях и при острых лейкозах.
К хранителям клеточного цикла относятся оба гена NF1 и NF2, вызывающие нейрофиброматоз I и II типов, но выполняющие в геноме различную функцию. Первый обеспечивает негативную регуляцию онкогена Ras, второй стабилизирует клеточные контакты. Мутации и структурные перестройки первого гена вызывают шванномы периферической нервной системы, а второго – шванномы ЦНС и менингиомы. Изменений этих генов не обнаружено в опухолях другого происхождения.
Синдромы множественной эндокринной неоплазии I и II типов (МЭН 1, МЭН 2) возникают в результате мутаций в гене-супрессоре MEN1 и протоонкогене RET соответственно. В случае синдрома МЭН 1 могут развиваться карциноидные опухоли, ангиофибромы лица, липомы, коллагеномы, гастриномы и инсулиномы.
Герминальные миссенс-мутации RET выявлены у пациентов с синдромом МЭН 2A (медуллярный рак щитовидной железы, феохромоцитома, гиперплазия паращитовидных желез, ганглионейромы слизистой ротовой полости) и семейной формой медуллярного РЩЖ, причем мутации в основном затрагивают пять цистеиновых кодонов в 10 и 11 экзонах и на них приходится 97% и 85% всех мутаций в этих экзонах соответственно.
Спорадические мутации в тирозинкиназном домене гена более характерны для синдрома МЭН 2В, отличающегося от типа 2А более агрессивным течением и отсутствием гиперплазии паращитовидных желез и ганглионейром, а точковая мутация в экзоне 16 (T918C) была идентифицирована в 93% случаев.
Синдром фон Хиппель-Линдау наследуется аутосомно-доминантно с частотой 1 на 36 тыс. Среди злокачественных новообразований, являющихся диагностическим признаком и позволяющих выделить 4 типа заболевания, наиболее часто встречаются гемангиобластомы ЦНС, карциномы почки, феохромоцитомы и опухоли поджелудочной железы. При заболевании обнаруживаются мутации в гене VHL, клонированном в коротком плече хромосомы 3p25.5. Мутации представлены большими делециями, мутациями сдвига рамки считывания и миссенс-мутациями, повреждающими преимущественно 1 и 3 экзоны. Соматические мутации, повреждающие 1 и 2 экзоны гена, выявлены только в светлоклеточном раке почки. Почти в 20% опухолей обнаружено аномальное метилирование промоторной области гена.
Семейный аденоматозный полипоз желудочно-кишечного тракта – аутосомно-доминантное заболевание, вызываемое мутациями в гене APC. Вариантом заболевания является синдром Гарднера, при котором преимущественно поражается толстый кишечник. При заболевании достаточно часто выявляются гепатоцеллюлярный рак, опухоли щитовидной железы, медуллобластомы, фибромы и другие опухоли. Основным типом мутаций являются делеции и нонсенс-мутации, приводящие к преждевременной терминации синтеза белка. Герминальные мутации преимущественно повреждают первую половину гена, причем обнаружено два «горячих» кодона – 1061 и 1309. Мутации последнего кодона приводят к раннему появлению полипов и быстрой малигнизации. Соматические мутации в основном локализуются в районе кодонов 1286-1513, с преимущественным повреждением кодонов 1309 и 1450.
Синдром Горлина или базально-клеточных невусов – редкое аутосомно-доминантное заболевание (частота 1:57000), возникает в результате мутаций в гене-супрессоре PTC1, представленных в 86% делециями и инсерциями, равномерно распределенными по длине гена. Проявляется множественными аномалиями развития, невусами и различными новообразованиями, наиболее частыми среди которых являются базально-клеточные рак кожи, медуллобластомы, астроцитомы, фибромы и аденокарциномы яичников. Во всех опухолях у синдромальных пациентов и в спорадических базально-клеточных карциномах обнаруживается потеря гетерозиготности по маркерам района хромосомы 9q22.3.
Целая группа синдромов – Ковдена, Банаяна-Зонана, Банаяна-Райли-Рувалкаба и часть случаев ювенильного полипоза характеризуется сходными фенотипическими аномалиями и предрасположенностью к злокачественным новообразованиям. Причиной всех заболеваний является патология гена-супрессора PTEN. У больных наиболее часто встречаются рак молочной железы, предстательной железы, яичников, эндометрия, щитовидной железы. Мутации равномерно повреждают весь ген и представляют полный спектр. Только при синдроме Ковдена установлено, что 43% мутаций повреждают 5 экзон, а в экзонах 1, 4 и 9 мутаций не описано. Соматические делеции и мутации PTEN обнаружены в глиобластомах, раках простаты, молочной железы и неходжкинских лимфомах.
Герминальные миссенс-мутации гена-супрессора p53, участвующего в задержке клеточного цикла необходимой для репарации ДНК, приводят к довольно редкому синдрому Ли-Фраумени, при котором типичными являются опухоли мозга, саркомы костей и мягких тканей, лейкозы и РМЖ. Выявлена кластеризация мутаций в районе 14 кодонов (245-258). В то же время различные повреждения гена выявляют практически во всех типах опухолей. Частота миссенс-мутаций гена составляет 74%, сдвига рамки считывания – 11%, нонсенс-мутаций – 7%, мутаций сайта сплайсинга – 4%. Определено 7 «горячих» точек, повреждаемых мутациями: кодоны 130-142, 151-164, 171-181, 193-200, 213-223, 234-258 и 270-286, причем все они локализованы в эволюционно консервативном ДНК-связывающем домене, кодируемом экзонами 5-8. Мутации кодонов 157 и 179 наиболее часто выявляются при раке легкого, кодона 175 – при раке толстой кишки, кодона 248 – при плоскоклеточном раке головы и шеи, кодона 249 – при гепатоцеллюлярном раке и кодона 278 – при опухолях кожи.
Атаксия-телангиоэктазия – аутосомно-рецессивное заболевание, сопровождающееся ломкостью хромосом, причем ионизирующее излучение повышает нестабильность кариотипа. При заболевании наиболее часто обнаруживаются Т-клеточные лейкозы, В-лимфомы, медуллобластомы и глиомы. Причиной являются гомозиготные мутации или делеции гена ATM, регулирующего клеточный цикл, причем делеции составляют основную массу патологии. У гетерозиготных носителей герминальных мутаций часто возникают карциномы молочной железы. Основным типом являются мутации, приводящие к преждевременной терминации синтеза белка.
Недавно клонирован еще один ген, участвующий в репарации двухцепочечных разрывов ДНК. Герминальные мутации гена NBS1 приводят к синдрому Ниджмиген – очень редкому аутосомно-рецессивному заболеванию, основными признаками которого являются аномалии фенотипа, иммунодефицит, предрасположенность к возникновению опухолей (лимфома, лимфолейкоз, нейробластома) и нестабильность хромосом, чувствительных к ионизирующему излучению. Наиболее характерными мутациями гена являются делеции и инсерции, преимущественно повреждающие 6 и 7 экзоны, а мутация 675del5 выявлена у 90% пациентов.
Клонирование генов, вовлеченных в развитие наследственных онкологических заболеваний, практически полностью изменило тактику медико-генетического консультирования, определение конкретной мутации конкретного гена в семье позволяет эффективно проводить пренатальную диагностику.
Соматические мутации в опухоли
Мутация — любое изменение в молекуле ДНК либо структуре хромосом. Изменения, которые происходят в гаметах — половых клетках, называют герминальными, в любых других клетках организма — соматическими. Герминальные мутации передаются от родителей по наследству в виде генетических заболеваний. Соматические изменения не наследуются, а возникают в результате внешних воздействий (курения, радиоактивного излучения и других).
Доказано, что злокачественные опухоли в 90–95 % случаев возникают в результате соматических мутаций (спорадический рак). Наследственный рак, развивающийся в результате герминальных изменений, составляет 5–10 % от всех случаев заболевания.
Клеточные механизмы возникновения рака: протоонкогены и онкосупрессоры
Соматические мутации увеличивают шанс превращения здоровых клеток в раковые за счет активации онкогенов — генов, стимулирующих образование злокачественных опухолей. Онкогены образуются из обычных генов — протоонкогенов.
Деление клеток опухоли и разрастание опухолевой ткани тормозят антионкогены — гены-супрессоры. Протоонкогены и гены-супрессоры образуют систему стимуляции и подавления злокачественного процесса.
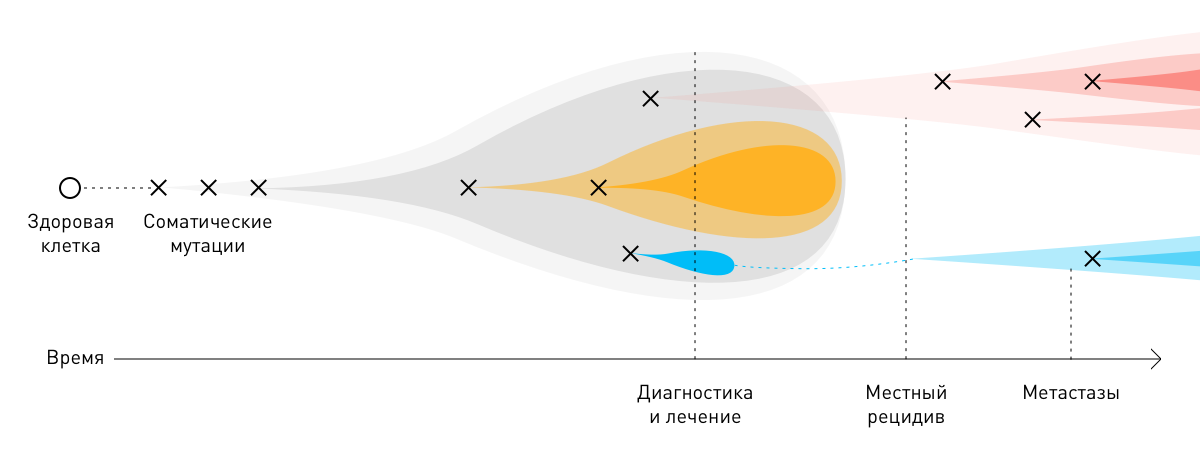
В подавляющем большинстве случаев раковые опухоли возникают из одной клетки в результате двух последовательных мутаций: первичной (герминальной) и вторичной (соматической). Для развития новообразования достаточно 3–6 таких повреждений. Вызванные ими изменения постепенно накапливаются в ДНК, вызывают неконтролируемое размножение пораженных клеток и образование атипичных тканей.
Драйверные соматические мутации и их использование для лечения злокачественных опухолей
В этиологии опухолей изменения в клетках вызывают ошибки копирования ДНК при делении — соматические драйверные мутации. В одних органах и тканях стволовые клетки делятся чаще, чем в других. В них злокачественные новообразования образуются чаще, чем в других структурах организма. По данным международного агентства по исследованию рака IARC, риск заболеть раком, а также выживаемость раковых клеток на 70–80 % зависят от интенсивности деления стволовых клеток и увеличиваются с возрастом.
Генетические маркеры опухолей (изменения в структуре белков в результате соматических драйверных мутаций) можно использовать как мишень и прицельно блокировать с помощью фармакологических препаратов. На этом принципе основан один из наиболее результативных современных методов лечения рака — таргетная терапия. Она позволяет:
Выявление драйверных соматических мутаций для диагностики злокачественных опухолей
Чем больше генетических маркеров известно, тем более адекватно подбирается лечение. Для выявления соматических мутаций при диагностике злокачественных опухолей используют следующие методики:
Целесообразность использования того или иного метода в каждом конкретном случае определяет врач.
Соматические мутации опухолей: влияние на диагностику и лечение
В процессе роста злокачественные новообразования приспосабливаются к факторам онкологического лечения — лучевой, химио- и иммунотерапии. Молекулы онкологических клеток, выжившие после того или иного лечебного этапа, нередко мутируют. Соматические мутации опухолей способствуют прогрессированию болезни и её более агрессивному (рецидивирующему и метастатическому) течению. Из-за индивидуальных различий на молекулярном уровне общеклинические стратегии лечения того или иного вида рака могут быть неэффективны для отдельных пациентов.
Чтобы максимально снизить риск рецидивов, улучшить качество жизни больных и увеличить её продолжительность, соматические мутации в опухолях в ответ на фармако- и химиотерапию необходимо учитывать. Для их выявления разработан инновационный метод исследования — молекулярное профилирование. Результаты этого вида диагностики позволяют врачу назначать наиболее оптимальное персонализированное лечение.
Герминальные мутации это что
МРЩЖ — медуллярный рак щитовидной железы
МЭН2А — синдром множественных эндокринных неоплазий 2А типа
МЭН2Б — синдром множественных эндокринных неоплазий 2Б типа
УЗИ — ультразвуковое исследование
СКГ — С-клеточная гиперплазия
АКТГ — адренокортикотропный гормон
Медуллярный рак щитовидной железы (МРЩЖ) происходит из С-клеток и на его долю приходится 5—10% всех случаев рака Щ.Ж. Одной из особенностей МРЩЖ является высокая частота (до 25%) наследуемых форм [1]. Причиной развития наследственного МРЩЖ является герминальная мутация в онкогене RET, активация которого приводит к пролиферации и опухолевой трансформации клеток [2]. На сегодняшний день в литературе описано более 100 мутаций гена RET, локализованных в экзонах 5, 8, 10, 11, 13—16. Большинство из них представлены точковыми миссенс-мутациями, реже — короткими делециями, дупликациями, инсерциями [3, 4]. Локализация мутации и тип замены аминокислоты влияют на клинические проявления МРЩЖ, включая возраст манифестации и агрессивность течения [3, 5]. При ряде мутаций, затрагивающих 10 и 11, реже 5, 8, 13 и 14 экзоны, МРЩЖ сочетается с феохромоцитомой и гиперпаратиреозом (синдром множественных эндокринной неоплазии типа 2А, МЭН2А). При наличии мутации в 16 экзоне, а иногда в 15 и 14 экзонах развивается синдром МЭН2Б, включающий, помимо МРЩЖ, феохромоцитому, ганглионейроматоз слизистой ЖКТ, губ и языка, а также специфические изменения внешности (марфаноподобный хабитус) [3, 5].
Двойные мутации гена RET, затрагивающие различные экзоны, встречаются крайне редко [6,7].Приводим описание семьи с тремя герминальными мутациями у ее членов.
Описание семьи
В клинику обратились родители 4-летнего мальчика для генетического консультирования. Из анамнеза известно, что мама ребенка в 24 года оперирована по поводу МРЩЖ и двусторонней феохромоцитомы. При проведении секвенирования гена RET у нее были выявлены две мутации в экзоне 11 (С634R) и экзоне 14 (I852M). У деда по материнской линии с синдромом МЭН2А (оперирован по поводу МРЩЖ и двусторонней феохромоцитомы соответственно в 35 и 45 лет), выявлена мутация С634R (рисунок). У бабушки по материнской линии исследование не проводилось. Таким образом, мутация I852M была унаследована матерью пробанда или от своей матери (бабушки пробанда), или возникла de novo.
При генетическом исследовании ребенка выявлены две герминальные мутации в экзоне 13 (Y791F) и экзоне 14 (I852M). Так как у матери мутация Y791 °F отсутствовала, генетическое исследование предложено отцу ребенка. При секвенировании гена RET у отца обнаружена герминальная мутация в экзоне 13 (Y791F). Таким образом, ребенок унаследовал одну мутацию (I852M) от матери, а другую (Y791F) от отца (см. рисунок).

Клиническое обследование ребенка 4 лет выявило повышение уровня кальцитонина (КТ) в сыворотке крови — 14 пг/мл (норма до 10 пг/мл). Учитывая наличие двух активирующих мутаций в гене RET, рекомендации Американской тиреоидологической ассоциации (АТА) и Российской ассоциации эндокринологов [4, 7], а также желание родителей мальчика, было решено провести профилактическую тиреоидэктомию до 5-летнего возраста. В возрасте 4 года 3 мес ребенку выполнена профилактическая тиреоидэктомия в хирургическом отделении № 1 (опухолей головы и шеи) НИИ ДОГ РОНЦ им. Н.Н. Блохина. При гистологическом исследовании удаленного препарата выявлены множественные очаги С-клеточной гиперплазии.
Клиническое обследование отца в возрасте 28 лет не выявило признаков заболевания (КТ 4,3 пг/мл, данные УЗИ шеи, брюшной полости и забрюшинного пространства — без патологии).
Обследование матери (с мутациями C634R+ I852M) в возрасте 28 лет не выявило признаков рецидива МРЩЖ (КТ 5,2 пг/мл), что указывает на своевременность проведенного хирургического лечения (в 24 года). При обследовании деда по материнской линии (мутация C634R) в 49 лет выявлены признаки персистенции МРЩЖ (КТ 180,4 пг/мл), что свидетельствует о запоздалом лечении и его нерадикальности.
Обсуждение
Герминальные мутации в гене RET, ответственные за развитие наследуемых форм МРЩЖ, встречаются у 20—25% больных МРЩЖ [1]. Крайне редко у пациента обнаруживают одновременно две и более мутации [6, 8—13]. У членов описанной семьи выявлено три мутации. Две из них (C634R и I852M) по материнской и одна (Y791F) — по отцовской линии.
К счастью, ребенок не унаследовал от матери наиболее патогенную мутацию C634R, ответственную за развитие синдрома МЭН2А с ранней манифестацией МРЩЖ, ранним метастазированием МРЩЖ и высокой пенетрантностью феохромоцитомы.
Мутация Y791 °F в экзоне 13 гена RET относится к типу АТА-А, которая приводит к наименее агрессивному МРЩЖ с низкой пенетрантностью, и в редких случаях — к синдрому МЭН2А [4, 7]. Хотя многие исследователи считают, что замену Y791 °F следует рассматривать как полиморфизм [14, 15], в последних рекомендациях NCCN, ATA, Американской ассоциации эндокринологов, а также Российской ассоциации эндокринологов (2015) роль Y791 °F не пересмотрена, и данную замену относят к мутации уровня ATA-А (АТА-MOD по классификации АТА, 2015), при которой рекомендовано проводить профилактическую тиреоидэктомию до 5 лет.
Мутация I852M в рекомендациях АТА, а следовательно, и всех ссылающихся на нее региональных рекомендациях, в том числе Российских, не упоминается. Впервые она была описана в 2001 г. у 20-летней больной МРЩЖ [16]. Однако, учитывая отсутствие МРЩЖ у ее 65-летней матери — носительницы аналогичной мутации, авторы предположили отсутствие связи данной мутации с синдромом МЭН2 или очень низкую пенетрантность МРЩЖ [16]. Позднее было рекомендовано отнести вариант I852M к мутации, соответствующей уровню АТА-А, и проводить профилактическую тиреоидэктомию до 10-летнего возраста с возможным увеличением этого срока, исходя из результатов определения уровня ТКТ и УЗИ шеи [17].
Встречаемость двух мутаций в гене RET довольно редка. Большая часть из них локализуется в одном аллеле, часть — в разных (см. таблицу). Вторая мутация может быть получена от второго родителя (разные RET-мутации у членов одной семьи) или возникать de novo. Немногочисленные сообщения о двойных мутациях противоречивы в отношении потенциирующего влияния второй мутации на клинические проявления, в том числе на возраст манифестации наследственного МРЩЖ и синдрома МЭН2А [8, 9, 11—13]. В ряде работ [6, 9, 13, 18—23] сообщается о более агрессивном течении МРЩЖ, более высокой пенетрантности феохромоцитомы, появлении ганглионейроматоза, характерного для синдрома МЭН2Б, эктопической продукции АКТГ опухолью (МРЩЖ или феохромоцитомой) у больных с множественными RET мутациями. Поэтому, хотя в данном случае роль каждой мутации в отдельности позволяла придерживаться тактики активного наблюдения, наличие одновременно двух мутаций послужило аргументом в пользу профилактической тиреоидэктомии. При гистологическом исследовании удаленной щитовидной железы выявлены множественные фокусы С-клеточной гиперплазии, что свидетельствует о высокой вероятности развития МРЩЖ, причем в более молодом возрасте.

Заключение
При обследовании больных МРЩЖ на предмет наличия герминальной RET-мутации необходимо иметь в виду возможность нескольких мутаций, локализующихся в разных экзонах, наследуемых как от одного, так и от обоих родителей, а также возникающих de novo. С развитием полноэкзомного секвенирования частота выявления случаев с множественными мутациями, вероятно, будет возрастать. Наличие нескольких мутаций может изменять клиническое течение МРЩЖ.
Финансирование работы. Работа проведена при финансовой поддержке ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина».
Конфликт интересов отсутствует. Медицинские данные пациентов публикуются с их письменного согласия.