Гепатоциты печени что это
Синдром печеночно-клеточной недостаточности
Сущность синдрома печеночно-клеточной недостаточности заключается в нарушении функционирования органа по причине повреждения гепатоцитов. Патология приводит к сбою белково-образующей, липидной, углеводной, пигментной, секреторной и обезвреживающей функций и, как следствие, к метаболическим расстройствам, интоксикации, нарушению деятельности центральной нервной системы, печеночной коме. Патологический процесс может развиваться по ряду причин, среди них: вирусные, бактериальные, паразитарные, аутоиммунные заболевания, нарушения обмена веществ, глистные инвазии, отравления, злоупотребление алкоголем и другие.
Классификация
Синдром принято классифицировать следующим образом.
По клинико-морфологическим признакам. При массовой гибели гепатоцитов констатируют эндогенную форму патологии, которая развивается при острых вирусных гепатитах, интоксикации печени. Экзогенная форма характеризуется нарушением циркуляции кровообращения, что приводит к движению крови из воротной вены без дезинтоксикации в печени сразу в общую систему. Причиной развития может стать шунтирование при портальной гипертензии и циррозе. Если синдром сочетает в себе патогенные механизмы эндогенной и экзогенной формы, то говорят о смешанном типе.
По характеру течения. Развитие хронической формы патологии обусловлено ухудшением состояния при хроническом заболевании печени (фиброзе, опухоли, циррозе и других). Острая печено-клеточная недостаточность проявляется не позднее двух месяцев с момента поражения печени. При молниеносном прогрессировании патологического процесса имеет место фульминантная форма.
По степени развития. Выделяют начальную, выраженную, терминальную дистрофическую стадии и печено-клеточную недостаточность.
Симптомы
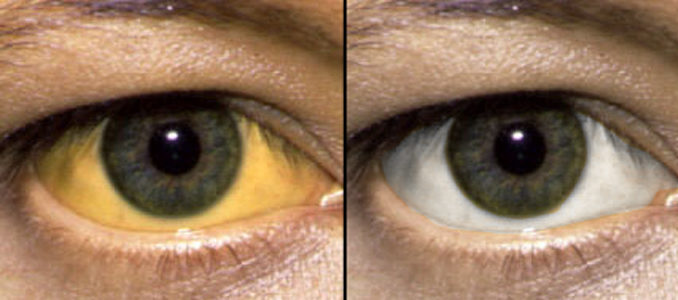
Заболевание на начальной стадии практически себя не проявляет. Больной может чувствовать небольшую слабость, сонливость, дискомфорт в правом подреберье. При прогрессировании патологии появляются следующие симптомы: желтушность кожи, слизистых, склер, зуд, снижение аппетита, нарушение сна, боль в правом подреберье, сильная тошнота с последующей рвотой, гипертермия, головные боли и другие. Дисфункция центральной нервной системы проявляется заторможенностью, нарушением координации движений, проблемами с речью, памятью, шумом в ушах, зрительными и слуховыми аномалиями (вплоть до галлюцинаций), головокружением и прочим. На последних стадиях нарушается функционирование практически всех систем организма и больной находится в бессознательном состоянии.
Лечение
Для стабилизации состояния, возобновления функционирования печени проводится терапия с применением гемодиализа, гемосорбции, плазмафереза и назначается специальная диета. Также осуществляются мероприятия с целью восстановления водно-электролитного и кислотно-щелочного баланса. Курс, методы и медикаментозные средства лечения определяются исходя из состояния больного, степени тяжести заболевания и других факторов.
Фокальная нодулярная гиперплазия
Фокальная нодулярная гиперплазия (ФНГ) является второй по частоте (после гемангиомы) доброкачественной опухолью печени. Частота ФНГ достигает 25% среди доброкачественных и 8% среди всех первичных новообразований печени. Опухоль встречается в любом возрасте, но чаще всего у женщин 30—40 лет (80—95%).
Причины возникновения
Однозначного мнения о причинах возникновения ФНГ не существует. Преобладание женщин, а также большая доля женщин (до 85%), употреблявших гормональные контрацептивы, долгое время поддерживали гипотезу о том, что данные препараты являются причиной заболевания. Однако обследование 216 женщин во Франции показало, что гормональные контрацептивы не оказывают влияния на частоту возникновения и размеры опухоли. В настоящее время считают, что ФНГ является реакцией гепатоцитов на локальные сосудистые мальформации (врожденные или приобретенные). Местные изменения кровотока ведут к появлению участков паренхимы с повышенным артериальным кровоснабжением и гиперплазии клеток печени. В пользу сосудистого генеза свидетельствует частое сочетание ФНГ с гемангиомами печени (до 23%) и различными сосудистыми аномалиями. Также отмечено появление ФНГ после травмы живота и химиотерапии, что связывают с повреждением внутрипеченочных сосудов.
ФНГ не трансформируется в злокачественную опухоль. Осложнения возникают крайне редко. В связи с доброкачественным характером и благоприятным прогнозом новообразования активного лечения не требуется. Необходимость в операции может возникнуть при увеличении размера, появлении симптомов или осложнений, а также при трудностях дифференциальной диагностики ФНГ и злокачественных опухолей печени.
Классификация
В гастроэнтерологии выделяют два типа нодулярной гиперплазии печени: классический (диагностируется в 80% случаев) и неклассический. Классический тип характеризуется наличием трех признаков: аномальной структуры дольки, извилистых толстостенных сосудов и гиперплазии желчных протоков; в 60% наблюдений обнаруживается центральный рубец с измененными сосудами разного калибра. При неклассическом типе всегда есть гиперплазия протоков, а один из оставшихся признаков (измененные сосуды или аномальная узловая архитектура) может отсутствовать. Неклассический тип подразделяют на три подтипа: аденоматозный гиперпластический, телеангиэктатический и нодулярную гиперплазию печени с клеточной атипией.
Токсическое поражение печени неуточненное (K71.9)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Общие положения
Общепризнанная классификация отсутствует.
Для описания процесса используются стандартные параметры (тип, тяжесть, форма, течение, осложнения). В случае достоверного установления той или иной морфологической формы заболевания, она выходит на первый план при классификации, поскольку определяет прогноз. Тяжесть процесса может определяться индексами и шкалами, принятыми для других форм заболеваний печени, или комплексными шкалами.
Классификация МКБ-10
Этиология и патогенез
I. Основные группы токсических агентов (в зависимости от вида гепатотоксического действия)
2.1 Лекарства, которые были связаны со своеобразными реакциями гиперчувствительности:
2.2 Наркотики, которые были связаны со своеобразными реакциями гиперчувствительности:
2.3.Травяные препараты или средства альтернативной (народной) медицины, с которыми были связаны своеобразные реакции гиперчувствительности:
1. Яды биологического происхождения (токсины). Поражение развивается в основном при лечении травами, приеме биологически активных добавок или при контакте с ядовитыми животными и растениями в дикой природе. Наиболее часто описываются случаи отравления бледной поганкой и травяными препаратами, используемыми в народной медицине.
2. Промышленные и бытовые химикаты:
— растворители, используемые в химчистке (производные четыреххлористого углерода);
— вещества, используемые в производстве пластмасс (винилхлорида);
— гербициды и группа промышленных химических веществ, называемых «полихлорированные бифенилы».
3. Лекарства: обезболивающие и жаропонижающие лекарственные средства, продающиеся без рецепта (аспирин, парацетамол, ибупрофен, антибиотики, противотуберкулезные средства, стероиды, эстрогены, ингаляционные анестетики и прочие). В настоящий момент описано более сотни препаратов, которые могут вызывать лекарственное поражение печени.
III. Формы повреждения.
Холестатический синдром. Редко встречается при острых токсических гепатопатиях и менее выражен в сравнении с цитолитическим синдромом. В качестве исключения выступают отравления лекарственными препаратами, для которых типичен холестатический гепатоз (фенотиазины, противотуберкулезные и антитиреоидные препараты; андрогены и анаболические стероиды, сульфаниламиды и другие).
Гранулёма. Медикаментозные печеночные гранулёмы обычно связаны с образованием гранулём в других тканях и пациенты с токсическим гранулематозным поражением печени, как правило, имеют признаки системного васкулита и гиперчувствительности. Более 50 препаратов были описаны как средства, вызывающие токсический гранулематоз печени (включая аллопуринол, фенитоин, изониазид, хинин, пенициллин, хинидин).
Новообразования. Новообразования были описаны при длительном воздействии некоторых лекарств или токсинов. Гепатоцеллюлярная карцинома, ангиосаркома и аденомы печени наиболее часто были ассоциированы с винилхлоридом, комбинированными оральными контрацептивами, анаболическими стероидами, мышьяком, диоксидом тория (рентгеноконтрастным веществом).
Лекарственные поражения печени
Оксана Михайловна Драпкина, исполнительный директор Интернет Сессии, секретарь межведомственного совета по терапии РАМН:
— Профессор Широкова Елена Николаевна. «Лекарственные поражения печени».
Елена Николаевна Широкова, доктор медицинских наук, профессор:
— Лекарственные поражения печени представляют собой различные клинико-морфологические варианты поражения печени, которые развиваются в ответ на прием лекарственных препаратов.
Эта тема становится все более и более актуальной в связи с тем, что на рынке появляется огромное количество новых лекарственных препаратов, эффективных, нужных нашим пациентам. В то же время мы все чаще сталкиваемся с реакциями на эти лекарственные препараты.
Трудность диагностики лекарственных поражений печени заключается в том, что они очень часто протекают под маской различных гепатопатий. Они не имеют характерной клинической картины.
Лекарственные поражения печени встречаются с частотой от одного случая на 1000 пациентов до одного случая на 100 000 пациентов, которые принимают лекарства в терапевтических дозах. В настоящее время зарегистрировано более 1000 препаратов, которые обладают способностью вызывать поражение печени.
Характерной клинической картины лекарственные поражения печени не имеют. Это может быть совершенно бессимптомное поражение, либо яркая клиническая манифестация вплоть до развития печеночной недостаточности. Как правило, пациенты могут предъявлять жалобы на кожный зуд, отсутствие аппетита, слезотечение, тошноту, в ряде случаев диарею.
Из лабораторных данных на помощь нам приходят следующие показатели. Это гамма-глутамилтранспептидаза. Ее повышение указывает на то, что система биотрансформации была задействована, активирована, как правило, в течение нескольких недель до повышения этого показателя. Естественно, должны быть исключены другие причины повышения гамма-ГТ.
Следует отметить, что данный показатель остается нормальным на фоне приема «Глотала». В ряде случаев контрацептивов. Аланиновая трансаминаза повышается, как правило, содружественно с аспарагиновой трансаминазой и указывает на воспалительное поражение печени. Коэффициент де Ритиса (отношения уровня аспарагиновой трансаминазы к уровню аланиновой трансаминазы), как правило, менее единицы (воспалительный тип ответа).
Снижение холинэстеразы указывает на то, что у пациента в результате токсического поражения снижается синтетическая функция печени. Повышение уровня щелочной фосфатазы указывает на развитие холестаза.
Считается, что определение трех первых параметров уровня гамма-ГТ, аланиновой трансаминазы, холинэстеразы является достаточно рациональным тестом, обладающим 95% чувствительности в диагностике лекарственных поражений печени. Исследования еще и уровня четвертого параметра (щелочной фосфатазы) повышает чувствительность до 96%.
В настоящее время принято оперировать классификацией лекарственных поражений печени, которая основана на повышении уровня основных биохимических проб. Выделяют гепатоцеллюлярное, холестатическое и смешанное лекарственное поражение печени.
Если уровень аланиновой трансаминазы повышен более чем в 5 раз от верхней границы нормы, и индекс R, который определяется как отношение уровня аланиновой трансаминазы к уровню щелочной фосфатазы, больше или равен 5, принято говорить о гепатоцеллюлярном поражении печени.
Если уровень щелочной фосфатазы повышен более чем в 2 раза, а индекс R меньше или равен 2, мы говорим о холестатическом поражении печени.
Если же и аланиновая трансаминаза и щелочная фосфатаза повышаются более чем в 2 раза от верхней границы нормы, а индекс R находится в диапазоне от 2 до 5, то мы говорим о смешанном поражении печени.
Следует сказать, что холестатические поражения печени протекают дольше, то есть разрешаются медленнее, чем гепатоцеллюлярные. В то же время тяжесть поражения гепатоцеллюлярных выше, чем у холестатических.
Данные регистра американских и испанских авторов, которые анализировали пациентов с лекарственными поражениями печени. В том и другом случае (в американском регистре были проанализированы истории болезни 300 пациентов, в испанском – более 600 пациентов) доминируют гепатоцеллюлярные поражения.
В американском исследовании их доля составляет 57%, а в испанском – 55%. Холестатические поражения представлены скромнее. Это 23% в американском исследовании, и 25% – в испанском. Смешанные поражения – 20% и 21% соответственно.
Интересен тот факт, что на фенотип лекарственного поражения печени оказывает влияние возраст пациента. По данным испанских авторов, опубликованным в журнале «Гепатология» в 2005-м году, было показано, что холестатические поражения чаще развиваются у мужчин старше 60-ти лет. В то же время гепатоцеллюлярные поражения чаще развиваются у женщин до 60-ти лет.
Тяжесть течения и исход лекарственного поражения печени во многом определяется типом поражения. Кумулятивная выживаемость при холестатических и смешанных лекарственных поражения печени существенно и достоверно выше, чем выживаемость больных, страдающих гепатоцеллюлярными поражениями печени.
Летальность в исследовании испанских авторов при гепатоцеллюлярном поражении печени составила 7%. В то время как при холестатическом – 5%, при смешанном поражении – 2%.
Аналогичное распределение было получено и по данным шведских авторов: 12,7% при гепатоцеллюлярном поражении, при холестатическом – 7,8%.
В испанском исследовании были определены предикторы развития фульминантной печеночной недостаточности при развитии лекарственного поражения. Ими оказались: высокий уровень билирубина, наличие гепатоцеллюлярного поражения и женский пол.
Другое соотношение. Это данные американского регистра изучения лекарственных поражений печени. Здесь летальность в основном превалировалась среди холестатических поражений – 14,3 против 7,5 при гепатоцеллюлярном поражении.
Но справедливости ради надо сказать, что эта группа пациентов с холестатическим поражением печени имела летальные исходы, которые не были связанны с развитием печеночной недостаточности, а с рядом других причин. Хотя при развитии печеночной недостаточности (естественно, превышение уровня билирубина) возрастает риск развития и почечной недостаточности и присоединение инфекционных осложнений. Это также утяжеляет прогноз пациента.
По данным шведских авторов независимый предиктор плохого прогноза, как при гепатоцеллюлярном, так и при холестатическом лекарственном поражении печени определял уровень билирубина в сыворотке крови.
До настоящего времени нет однозначного ответа на вопрос, какое лекарственное поражение печени следует считать хроническим. Показано, что уже через 3 месяца после дебюта лекарственного поражения печени может развиться фиброз. Значит логично считать 3 месяца тем временным интервалом, после которого можно говорить о развитии хронического лекарственного поражения печени.
В то же время было показано, что холестатические поражения текут значительно медленнее и разрешаются медленнее. Здесь сроки более продолжительные – 6 месяцев и более. В настоящий момент считается, что персистирующим поражением печени (в случае гепатоцеллюлярного) следует считать: если повышение уровня печеночных проб превышает интервал в 3 месяца. 6 месяцев – персистенция для холестатического поражения.
О хроническом поражении печени на фоне приема лекарственного препарата следует говорить тогда, когда измененные показатели функциональных проб печени фиксируются на протяжении более 12-ти месяцев.
Данные испанского исследования, когда проводилось длительное наблюдение за пациентами с лекарственными поражениями печени. Всего в исследовании приняло участие 258 пациентов. Излечение наблюдалось у половины пациентов (53%), хроническое течение лекарственное поражение печени приняло у 47%. Из них разрешение в период до года наблюдалось у 35% пациентов. Персистенция больше года – у большего количества (65%). Длительное разрешение из них наблюдалось у 48%, а длительная персистенция – более чем у половины пациентов (52%).
Интересные результаты: из этих 52% (из 38-ми человек) у 10-ти был диагностирован аутоиммунный гепатит. По-видимому, лекарственное поражение, прием лекарственного препарата выступил триггерным фактором для манифестации аутоиммунного гепатита. Среди оставшихся 28-ми у 10-ти диагностировано гепатоцеллюлярное поражение, у 18-ти холестатическое или смешанное поражение.
Выделяют два типа лекарственных реакций в ответ на прием лекарственного препарата. Тип А – это реакции дозозависимые, предсказуемые, характеризующиеся прямым повреждающим действием. Как пример, воздействие суррогатов алкоголя или парацетамол (фактически единственный препарат, для которого описано токсическое дозозависимое действие).
Второй тип реакции В – это дозонезависимые реакции, непредсказуемые. Как правило, мы сталкиваемся в нашей гистологической практике с реакциями типа В, реакциями гиперчувствительности. Они, в свою очередь, разделяются на аллергические реакции, реакции псевдоаллергические и реакции, которые протекают по типу идиосинкразии. Две последние наиболее часто встречающиеся реакции в практике терапевта.
Что касается морфологического эквивалента лекарственного повреждения печени, то в результате прямой гепатотоксичности мы можем наблюдать развитие некроза, стеатоза и холестаза. В ряде случаев мы сталкиваемся с развитием опухолевого процесса. При идиосинкратических реакциях мы сталкиваемся с развитием холестаза и некроза, либо некроза и стеатоза.
На практике часто бывает трудно выделить какой-то один вид поражения печени. Как правило, мы сталкиваемся с комбинированным поражением.
В качестве иллюстрации я привожу гистологический препарат развития холестатического гепатита. Представлены дегенеративные изменения эпителия желчных протоков. Но если мы будет апеллировать к мнению только морфолога, то, естественно, мы не получим ответ на вопрос: что явилось пусковым триггерным фактором на развитие данных изменений печени.
Их принято подразделять на две фазы. Первая фаза – это реакция окисления гидроксилирования. В результате образуются промежуточные метаболиты. Ряд из них может обладать токсическим свойством.
Эта схема иллюстрирует ряд переносчиков апикальной мембраны гепатоцита, которые обеспечивают выведение различных веществ из гепатоцита в желчные каналы. Слева вверху представлена экспортная помпа желчных кислот (так называемый BSEP), который кодируется геном ABCB11. Он ответственен за перенос желчных кислот.
Если нарушается функция этого переносчика, то происходит накопление желчных кислот, холестаз, повреждение гепатоцита. Переносчик множественной лекарственной резистентности MRP2 ответственен в основном за перенос конъюгированного связанного билирубина. Он также переносит ряд органических анионов и гепатоцитов в желчном канале.
Переносчик MDR3 – переносчик множественной лекарственной резистентности. Действуют как промежуточная фаза для фосфатидилхолина. Переносит фосфатидилхолин, который образует смешанные мицеллы холестериновой желчи.
Лекарственные препараты, преимущественно катионы, переносятся переносчиком множественной лекарственной резистентности под названием MDR1. Если есть какая-то генетическая предрасположенность, которая представлена нонсенс или миссенс-мутациями, то под действием ксенобиотиков выявляются нарушения работы этих транспортеров. Это, соответственно, ведет к накоплению токсических компонентов в гепатоците и к гибели гепатоцита.
В случае накопления токсических компонентов, лекарственных метаболитов, желчных кислот в гепатоците включаются альтернативные пути выведения. На базолатеральной мембране есть представители белков множественной лекарственной резистентности. В частности, это MRP3, MRP4.
В обычных условиях, когда печень функционирует нормально и ничто ей не угрожает, они фактически не активны. Но если нарушается работа других переносчиков апикальной мембраны, то они берут на себя новые функции. Они начинают работать с утроенной силой.
Что касается воздействия прямой токсичности различных метаболитов лекарственных веществ, которые происходят в печени, гепатоците. Они реализуют свое действие. Они могут повреждать ДНК. Они могут повреждать липиды и протеины. Они могут активировать процесс перекисного окисления липидов, истощать запасы АТФ, способствовать образованию свободных радикалов, нарушать нормальный цитоскелет и так далее.
За счет чего происходит реализация этих реакций прямой токсичности реактивных метаболитов? Происходит разрушение перекрестных связей между протеином, происходит расщепление микрофиламентов, что нарушает транспорт деления клетки. Фрагментация ДНК запускает каскад «Каспаз», который ведет к апоптозу, к программированной смерти клетки.
Помимо представленных действий токсических метаболитов описаны и другие механизмы лекарственного поражения печени. В частности, за счет нарушения гомеостаза кальция происходит нарушение сборки фибрилактина на поверхности мембраны гепатоцита. Образуются пузырьки воздуха. Пузырьки воздуха в мембране клетки ведут к нарушению ее целостности, что приводит к лизису клетки.
Под буквой В обозначены процессы, которые происходят на апикальном полисе гепатоцита. Транспортные мембраны, белки множественной лекарственной резистентности могут быть повреждены. Это способствует накоплению токсических элементов, желчных кислот в гепатоците и также приводит к повреждению печени.
Образующиеся с участием цитохрома P450 токсические метаболиты переносятся с помощью транспортеров эндоплазматического ретикулума на поверхность гепатоцита. Они могут выступать в роли антигенных мишеней для различных цитокинов.
Взаимодействие с рецепторами фактора некроза опухоли ИФАЗ приводит к запуску каскада «Каспаз» и к программируемой смерти клетки (к апоптозу). Ряд лекарственных препаратов может воздействовать на функцию митохондрии – угнетать бета-окисление. Нарушение метаболизма свободных жирных кислот приводит к накоплению лактата и свободных радикалов. Тем самым нарушается функция митохондрий.
Механизмы, которые влияют на развитие оксидативного стресса. С одной стороны, это фармакологическое воздействие. Это реактивные формы кислорода, которые продуцируются реактивными метаболитами лекарственных препаратов. С другой стороны, реактивная форма кислорода, которая может продуцироваться желчными кислотами.
Кроме того, имеют значение и генетические особенности. В митохондриях есть такой фермент, который называется супероксиддисмутаза. Это главный мусорщик супероксида, главный защитник клетки от разрушения. Есть также пероксидаза, которая способствует превращению перекиси водорода, восстановлению с образованием воды. Это второй главный защитник митохондрии клетки.
Если есть какие-то генетические особенности, которые приводят к нарушению работы этих ферментов, то в совокупности с фармакологическими воздействиями и воздействием внешних факторов это ведет к повреждению клетки.
Что же сделать в случае развития лекарственного поражения печени? Безусловно, необходима немедленная отмена препарата. При наличии реакции гиперчувствительности показаны глюкокортикостероиды. Если развивается холестаз, то здесь безусловным лидером является «Урсодезоксихолевая кислота».
Исходя из того, что мы с вами сейчас узнали о возможных механизмах развития лекарственного поражения печени, патогенетически обоснованным является применение препаратов, которые оказывают, соответственно, антиоксидантное, метаболическое действие, в том числе эссенциальных фосфолипидов.
На этой части мне хотелось бы остановиться несколько подробнее. Известно, что гепатоциты, другие клетки и различные органеллы имеют мембраны, которые в основном состоят из липидов (на 52 – 54%). 42 – 46% – это белки. Углеводы выступают как антенны для тканевых специфических рецепторов.
Площадь поверхности мембраны гепатоцита и органелл составляет 33 000 квадратных километров. Это в 5 раз превосходит площадь футбольного поля. Причем на долю базалотеральной мембраны приходится 85%. Остальная часть – это апикальная мембрана.
Основным компонентом мембраны являются фосфолипиды. 65% приходится на их долю. Фосфолипиды имеют различное строение. В основном, это фосфорные эфиры глицерина. В зависимости от состава холинсодержащие фосфолипиды располагаются на наружном слое мембраны. Внутренний слой – это аминосодержащие фосфолипиды.
Такое соотношение обеспечивает гибкость мембраны, ее текучесть, что позволяет мембране осуществлять свои свойства. Фосфолипиды образуют каркас мембраны, который необходим для нормального функционирования. Известно, что в водной среде фосфолипиды формируют двойной слой. Причем гидрофильные части молекулы расположены на наружной и внутренней стороне мембраны. Внутри находятся гидрофобные части.
Это обеспечивает непрерывность и текучесть мембраны. Обеспечивает как латеральное движение фосфолипидов и протеинов, так и движение по механизму «флип-флоп» между наружным и внутренним слоем мембраны.
Как действуют эссенциальные фосфолипиды? Чем привлекательны эти препараты для лечении лекарственных поражений печени?
Известно, что эссенциальные фосфолипиды обладают мембранопротективным свойством. Они нормализуют текучесть клеточных мембран. Они способствуют репарации гепатоцитов, восстанавливая поврежденные структуры для того, чтобы больная печень не затрачивала (это процесс энергоемкий) свои силы на восстановление поврежденных клеточных мембран.
Кроме того, эссенциальные фосфолипиды нормализуют окислительно-восстановительные процессы, то есть обладают антиоксидантным эффектом. Защищают клетку от окислительного стресса. Это фактически краеугольный камень развития лекарственного поражения печени – повреждение гепатоцитов.
Важно, что эссенциальные фосфолипиды обладают антифибротическим эффектом, воздействуя на звездчатые клетки и продукцию проколлагена.
Ферменты дыхательных путей митохондрии, которые призваны защищать клетку от повреждения. Их деятельность, их активность непосредственно связана с уровнем фосфолипидов. Уровень активности ферментов находится также в прямой зависимости от содержания полиненасыщенных жирных кислот в молекулах фосфолипидов.
Важно, что прием эссенциальных фосфолипидов позволяет быстрее справиться с патологическими изменениями биохимических показателей. Кроме того, эти препараты могут назначаться профилактически вместе с теми препаратами, которые часто приводят к развитию лекарственного поражения печени.
Как хорошо вам известно, в ряде случаев мы не можем отказаться от назначения противотуберкулезной, противоопухолевой терапии. Здесь нам нужны помощники – препараты, которые могли бы нивелировать токсические эффекты этих препаратов. Эссенциальные фосфолипиды хорошо работают и в этой ситуации.
В заключении мне еще раз хотелось бы подчеркнуть, что для определения причин гепатотоксичности необходим системный подход. Необходим тщательный анализ клинико-анамнестических лабораторно-нструментальных данных для того, чтобы судить о том, что явилось причиной поражения печени.
В настоящее время определен ряд универсальных молекулярных механизмов развития лекарственных поражений печени. На практике врачу целесообразно пользоваться биохимической классификацией лекарственных поражений печени.
Лекарственно-индуцированный холестаз протекает легче, но разрешается значительно медленнее, чем гепатоцеллюлярное поражение печени.
В качестве лечебной тактики (безусловно, если есть такая возможность) отменить препарат, который вызвал лекарственное поражение печени. Глюкокортикостероиды при реакции гиперчувствительности. «Урсодезоксихолиевая кислота» при развитии холестатического поражения. Препараты с антиоксидантным эффектом, мембранопротективным эффектом, в том числе и эссенциальные фосфолипиды также показаны в лечении лекарственного поражения печени.