Что влияет на активность ферментов
Ферменты

Этот термин постоянно на слуху, правда, далеко не все понимают, что такое фермент или энзим, какие функции выполняет это вещество, а также чем отличаются ферменты от энзимов и отличаются ли вообще. Все это сейчас и узнаем.
Без этих веществ ни люди, ни животные не смогли бы переваривать пищу. А впервые к применению ферментов в быту человечество прибегло более 5 тысяч лет тому назад, когда наши предки научились хранить молоко в «посуде» из желудков животных. В таких условиях под воздействием сычужного фермента молоко превращалось в сыр. И это только один из примеров работы энзима в качестве катализатора, ускоряющего биологические процессы. Сегодня ферменты незаменимы в промышленности, они важны для производства сахара, маргаринов, йогуртов, пива, кожи, текстиля, спирта и даже бетона. В моющих средствах и стиральных порошках также присутствуют эти полезные вещества – помогают выводить пятна при низких температурах.
История открытия
Энзим в переводе с греческого означает «закваска». А открытию этого вещества человечество обязано голландцу Яну Баптисту Ван-Гельмонту, жившему в XVI веке. В свое время он весьма заинтересовался спиртовым брожением и в ходе исследования нашел неизвестное вещество, ускоряющее этот процесс. Голландец назвал его fermentum, что в переводе означает «брожение». Затем, почти тремя веками позже, француз Луи Пастер, также наблюдая за процессами брожения, пришел к выводу, что ферменты – не что иное, как вещества живой клетки. А через некоторое время немец Эдуард Бухнер добыл фермент из дрожжей и определил, что это вещество не является живым организмом. Он также дал ему свое название – «зимаза». Еще несколькими годами позже другой немец Вилли Кюне предложил все белковые катализаторы разделить на две группы: ферменты и энзимы. Причем вторым термином он предложил называть «закваску», действия которой распространяются вне живых организмов. И лишь 1897 год положил конец всем научным спорам: оба термины (энзим и фермент) решено использовать как абсолютные синонимы.
Структура: цепь из тысяч аминокислот

Каждая аминокислота соединена с другой определенным типом химической связи, а каждый фермент имеет свою уникальную последовательность аминокислот. Для создания большинства из них используются примерно по 20 видов. Даже незначительные изменения последовательности аминокислот могут кардинально менять внешний вид и «таланты» фермента.
Биохимические свойства
Хотя при участии ферментов в природе происходит огромное количество реакций, но все они могут быть разделены на 6 категорий. Соответственно, каждая из этих шести реакций протекает под влиянием определенного типа ферментов.
Реакции при участии энзимов:
Ферменты, участвующие в этих реакциях, называются оксидоредуктазами. В качестве примера можно вспомнить как, алкогольдегидрогеназы преобразуют первичные спирты в альдегид.
Ферменты, благодаря которым происходят эти реакции, называются трансферазами. Они обладают умением перемещать функциональные группы от одной молекулы к другой. Так происходит, например, когда аланинаминотрансферазы перемещают альфа-аминогруппы между аланином и аспартатом. Также трансферазы перемещают фосфатные группы между АТФ и другими соединениями, а из остатков глюкозы создают дисахариды.

Этот вид реакций негидролитическим путем происходит при участии лиазы.
Во многих химических реакциях положение функциональной группы изменяется в пределах молекулы, но сама молекула состоит из того же количества и типов атомов, что были до начала реакции. Иными словами, субстрат и продукт реакции являются изомерами. Такого типа трансформации возможны под влиянием ферментов изомеразы.
Гидролазы разрушают связь, добавляя в молекулу элементы воды. Лиазы осуществляют обратную реакцию, удаляя водную часть из функциональных групп. Таким образом, создают простую связь.
Как работают в организме
Ферменты ускоряют практически все химические реакции, происходящие в клетках. Они имеют жизненно важное значение для человека, облегчают пищеварение и ускоряют метаболизм.
Некоторые из этих веществ помогают разрушать слишком большие молекулы на более мелкие «куски», которые организм сможет переварить. Другие наоборот связывают мелкие молекулы. Но ферменты, говоря научным языком, обладают высокой селективностью. Это значит, что каждое из этих веществ способно ускорять только определенную реакцию. Молекулы, с которыми «работают» ферменты, называются субстратами. Субстраты в свою очередь создают связь с частью фермента, именуемой активным центром.
Существуют два принципа, объясняющие специфику взаимодействия ферментов и субстратов. В так называемой модели «ключ-замок» активный центр фермента занимает в субстрате место строго определенной конфигурации. Согласно другой модели, оба участника реакции, активный центр и субстрат, меняют свои формы, чтобы соединиться.
По какому бы принципу ни происходило взаимодействие результат всегда одинаковый – реакция под воздействием энзима протекает во много раз быстрее. Вследствие такого взаимодействия «рождаются» новые молекулы, которые потом отделяются от фермента. А вещество-катализатор продолжает выполнять свою работу, но уже при участии других частиц.
Гипер- и гипоактивность
Бывают случаи, когда энзимы выполняют свои функции с неправильной интенсивностью. Чрезмерная активность вызывает чрезмерное формирование продукта реакции и дефицит субстрата. В результате – ухудшение самочувствия и серьезные болезни. Причиной гиперактивности энзима может быть как генетическое нарушение, так и избыток витаминов или микроэлементов, используемых в реакции.
Гипоактивность ферментов может даже стать причиной смерти, когда, например, энзимы не выводят из организма токсины либо возникает дефицит АТФ. Причиной такого состояния также могут быть мутированные гены или, наоборот, гиповитаминоз и дефицит других питательных веществ. Кроме того, пониженная температура тела аналогично замедляет функционирование энзимов.
Катализатор и не только

Энзимы – это биологические молекулы, жизненный цикл которых не определяется рамками от рождения и смерти. Они просто работают в организме до тех пор, пока не растворятся. Как правило, это происходит под воздействием других ферментов.
В процессе биохимической реакции они не становятся частью конечного продукта. Когда реакция завершена, фермент покидает субстрат. После этого вещество готово снова приступить к работе, но уже на другой молекуле. И так продолжается столько, сколько необходимо организму.
Уникальность ферментов в том, что каждый из них выполняет только одну, ему отведенную функцию. Биологическая реакция происходит только тогда, когда фермент находит правильный для него субстрат. Это взаимодействие можно сравнить с принципом работы ключа и замка – только правильно подобранные элементы смогут «сработаться». Еще одна особенность: они могут работать при низких температурах и умеренном рН, а в роли катализаторов являются более стабильными, чем любые другие химические вещества.
Ферменты в качестве катализаторов ускоряют процессы метаболизма и другие реакции.
Как правило, эти процессы состоят из определенных этапов, каждый из которых требует работы определенного энзима. Без этого цикл преобразования или ускорения не сможет завершиться.
Пожалуй, из всех функций ферментов наиболее известна – роль катализатора. Это значит, что энзимы комбинируют химические реагенты таким образом, чтобы снизить энергетические затраты, необходимые для более быстрого формирования продукта. Без этих веществ химические реакции протекали бы в сотни раз медленнее. Но на этом способности энзимов не исчерпываются. Все живые организмы содержат энергию, необходимую им для продолжения жизни. Аденозинтрифосфат, или АТФ, это своего рода заряженная батарейка, которая снабжает клетки энергией. Но функционирование АТФ невозможно без ферментов. И главный энзим, производящий АТФ, – синтаза. Для каждой молекулы глюкозы, которая трансформируется в энергию, синтаза производит около 32-34 молекул АТФ.
Помимо этого, энзимы (липаза, амилаза, протеаза) активно применяются в медицине. В частности, служат компонентом ферментативных препаратов, таких как «Фестал», «Мезим», «Панзинорм», «Панкреатин», применяемых для лечения несварения желудка. Но некоторые энзимы способны также влиять на кровеносную систему (растворяют тромбы), ускорять заживление гнойных ран. И даже в противораковой терапии также прибегают к помощи ферментов.
Факторы, определяющие активность энзимов
Поскольку энзим способен ускорять реакции во много раз, его активность определяется так называемым числом оборотов. Этот термин обозначает количество молекул субстрата (реагирующего вещества), которую способна трансформировать 1 молекула фермента за 1 минуту. Однако существует ряд факторов, определяющих скорость реакции:

Обычно повышение температуры ведет к ускорению реакций. Это правило работает для большинства ферментативных реакций, но только до тех пор, пока температура не поднимется выше 40 градусов по Цельсию. После этой отметки скорость реакции, наоборот, начинает резко снижаться. Если температура опустится ниже критической отметки, скорость ферментативных реакций повысится снова. Если температура продолжает расти, ковалентные связи рушатся, а каталитическая активность фермента теряется навсегда.
На скорость ферментативных реакций также влияет показатель рН. Для каждого фермента существует свой оптимальный уровень кислотности, при котором реакция проходит наиболее адекватно. Изменение уровня рН сказывается на активности фермента, а значит, и скорости реакции. Если изменения слишком велики, субстрат теряет способность связываться с активным ядром, а энзим больше не может катализировать реакцию. С восстановлением необходимого уровня рН, активность фермента также восстанавливается.
Ферменты для пищеварения
Ферменты, присутствующие в человеческом организме, можно разделить на 2 группы:
Метаболические «работают» над нейтрализацией токсических веществ, а также способствуют выработке энергии и белков. Ну и, конечно, ускоряют биохимические процессы в организме.
За что отвечают пищеварительные – понятно из названия. Но и здесь срабатывает принцип селективности: определенный тип ферментов влияет только на один вид пищи. Поэтому для улучшения пищеварения можно прибегнуть к маленькой хитрости. Если организм плохо переваривает что-то из еды, значит надо дополнить рацион продуктом, содержащим фермент, который способен расщепить трудно перевариваемую пищу.
Пищевые ферменты – катализаторы, которые расщепляют продукты питания до состояния, в котором организм способен поглощать из них полезные вещества. Пищеварительные энзимы бывают нескольких типов. В человеческом организме разные виды ферментов содержатся на разных участках пищеварительного тракта.
Ротовая полость

Желудок
Здесь пепсин расщепляет белки до состояния пептидов, а желатиназа – желатин и коллаген, содержащиеся в мясе.
Поджелудочная железа
На этом этапе «работают»:
Тонкая кишка
Над пищевыми частицами «колдуют»:
Толстый кишечник

Кроме названных энзимов, существуют еще:
Катализаторы в продуктах
Ферменты имеют решающее значение для здоровья, поскольку помогают организму расщеплять пищевые компоненты до состояния, пригодного для использования питательных веществ. Кишечник и поджелудочная железа производят широкий спектр ферментов. Но кроме этого, многие из полезных веществ, способствующих пищеварению, содержатся также и в некоторых продуктах.
Ферментированные продукты являются практически идеальным источником полезных бактерий, необходимых для правильного пищеварения. И в то время, когда аптечные пробиотики «работают» только в верхнем отделе пищеварительной системы и часто не добираются до кишечника, эффект от ферментативных продуктов ощущается во всем желудочно-кишечном тракте.
Например, абрикосы содержат в себе смесь полезных энзимов, в том числе инвертазу, которая отвечает за расщепление глюкозы и способствует быстрому высвобождению энергии.
Натуральным источником липазы (способствует более быстрому перевариванию липидов) может послужить авокадо. В организме это вещество производит поджелудочная железа. Но дабы облегчить жизнь этому органу, можно побаловать себя, например, салатом с авокадо – вкусно и полезно.
Кроме того, что банан, пожалуй, самый известный источник калия, он также поставляет в организм амилазу и мальтазу. Амилаза содержится также в хлебе, картофеле, крупах. Мальтаза способствует расщеплению мальтозы, так называемого солодового сахара, который в обилии представлен в пиве и кукурузном сиропе.
Другой экзотический фрукт – ананас содержит в себе целый набор энзимов, в том числе и бромелайн. А он, согласно некоторым исследованиям, еще и обладает противораковыми и противовоспалительными свойствами.
Экстремофилы и промышленность
Экстремофилы – это вещества, способны сохранять жизнедеятельность в экстремальных условиях.
Живые организмы, а также ферменты, позволяющие им функционировать, были найдены в гейзерах, где температура близка к точке кипения, и глубоко во льдах, а также в условиях крайней солености (Долина Смерти в США). Кроме того, ученые находили энзимы, для которых уровень рН, как оказалось, также не принципиальное требование для эффективной работы. Исследователи с особым интересом изучают ферменты-экстремофилы, как вещества, которые могут быть широко использованы в промышленности. Хотя и сегодня энзимы уже нашли свое применение в индустрии как биологически и экологически чистые вещества. К применению энзимов прибегают в пищевой промышленности, косметологии, производстве бытовой химии.
Более того, «услуги» ферментов в таких случаях обходятся дешевле, чем синтетических аналогов. Кроме того, натуральные вещества являются биоразлагаемыми, что делает их использование безопасным для экологии. В природе существуют микроорганизмы, способные расщепить ферменты на отдельные аминокислоты, которые затем становятся компонентами новой биологической цепочки. Но это, как говорится, уже совсем другая история.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
Научная электронная библиотека
Сергеева И. В., Демко И. В.,
Глава 3. СТРУКТУРНО-МЕТАБОЛИЧЕСКИЕ ХАРАКТЕРИСТИКИ КЛЕТОК И ИХ ФУНКЦИОНАЛЬНЫЕ ВОЗМОЖНОСТИ
Регуляция жизнедеятельности любой клетки осуществляется в основном за счет состояния структурных субъединиц мембраны, их взаимодействия и взаимного расположения [14, 15, 16, 17]. В результате структурных перестроек могут изменяться практически все функции биомембран, органелл и клетки в целом: активность мембраносвязанных ферментов, проницаемость и транспорт ионов и субстратов, активность генома, размножение.
Наибольшее количество исследований, посвященных изучению зависимости функциональных возможностей клеток от их метаболических характеристик, проведено на лимфоцитах. Это можно объяснить тем, что лимфоцит имеет сложный внутриклеточный обмен, отражающий практически все метаболические процессы, свойственные организму, в связи с чем Р.П. Нарциссов назвал лимфоцит – «ферментативным зеркалом организма» [16].
Лимфоциты, являясь основным морфологическим субстратом иммунной системы, определяют важнейшие параметры иммунореактивности организма. Реализация его защиты в виде образования антител и осуществления реакций клеточного иммунитета, а также выработка гуморальных факторов регуляции иммунного ответа определяются функциональными возможностями этих клеток, в основе которых лежат внутриклеточные метаболические реакции, что на сегодняшний день не вызывает сомнений и подтверждено многочисленными исследованиями [4, 14, 15, 16, 17].
Например, в лимфоцитах происходит конвейерное производство иммуноглобулинов, поэтому одной из особенностей их внутриклеточного обмена является наличие мощного аппарата синтеза белков, который по своим возможностям превосходит не только все другие клетки крови, но многие клетки других органов и тканей [4, 14, 15, 16, 17].
Внутриклеточный метаболизм лимфоцитов регулируется широким набором ферментов и это обеспечивает возможность выполнения клетками многообразных специфических функций [4, 14, 15, 16, 17].
Проявление ими функциональных возможностей в полном объеме лимфоцитов возможно лишь при соответствующем состоянии внутриклеточного обмена [4, 16]. Р.П. Нарциссов разработал спектр методов, позволяющих по активности ферментов в лимфоцитах осуществлять не только оценку их функциональной возможностей, диагностику различных патологических процессов, но и прогноз тяжести и длительности заболевания[16].
Ферментативная активность является чувствительным показателем функционального состояния лимфоцитов и эти показатели используются не только в диагностических, но и в прогностических целях. Ферментный состав лимфоцитов периферической крови позволяет наиболее полно оценить картину изменений в лимфоидной системе в процессе формирования иммунного ответа в норме или при развитии иммунопатологического процесса [7, 287, 301]. Установление закономерностей в направленности реакций гликолиза, пентозофосфатного пути, цикла Кребса, переаминирования и окислительного дезаминирования в лимфоцитах на отдельных этапах формирования иммунного ответа позволило рекомендовать ряд ферментативных показателей для оценки и прогнозирования иммунобиологической перестройки организма [4, 14, 15, 16, 17]. В настоящее время не вызывает сомнения, что проявление функциональных возможностей лимфоцитов происходит только при соответствующем состоянии внутриклеточных метаболических реакций.
При формировании иммунного ответа изменяется активность внутриклеточных ферментов лимфоцитов. Результаты изучения этих изменений позволяют использовать указанные показатели для оценки течения иммунопатологического процесса и в целом состояния иммунной системы человека [4, 14, 15, 16, 17]. На сегодняшний день изучена активность различных ферментов не только суммарной популяции лимфоцитов периферической крови [16], но и отдельно в Т- и В-лимфоцитах. Установлено, что эти клеточные популяции различаются по ряду ферментных параметров [16].
Метаболические изменения в лимфоцитах начинаются уже через несколько секунд после антигенной стимуляции рецепторов, находящихся на их клеточной мембране: активируется Na- и K-зависимые АТФазы, усиливается поступление ионов К+ в клетку, а из нее выходят ионы Na+, повышается активность мембранных метилтрансфераз, возрастает поток Са2+ внутрь клетки, участвующего в активации
гуанилатциклазы и ингибированию аденилатциклазы; перечисленные изменения запускают каскад внутриклеточных реакций с участием метаболических ферментов [4, 14, 15, 16, 17].
Перестройки внутриклеточного обмена, происходящие при стимуляции рецепторного аппарата лимфоцитов, приводят к очень существенным его изменениям. Например, стимуляция Т-лимфоцитов такими веществами, как форболовый эфир, 12-0-тетрадеканоил или форбол-13-ацетат, способна увеличивать концентрацию основных кофакторов ферментов НАД+ и НАДФ+ соответственно в 6–11
и 10–21 раз. В результате этого ферменты, катализирующие процессы внутриклеточного обмена, резко увеличивают свою активность, что и определяет повышение способности лимфоцитов участвовать в иммунном ответе [16].
Наиболее информативными для получения характеристики процессов внутриклеточного метаболизма считаются окислительно-восстановительные ферменты (оксидоредуктазы или дегидрогеназы)). Это связано с тем, что, являясь основными переносчиками электронов в клетке, они осуществляют ключевые реакции клеточного метаболизма и координируют сопряженные метаболические пути, участвуя как в энергетических, так и синтетических процессах [4, 14, 15, 16, 17].
Более широкие возможности для изучения особенностей внутриклеточных процессов появились с разработкой определения активности внутриклеточных ферментов методом биолюминесценции с бактериальной люциферазой.
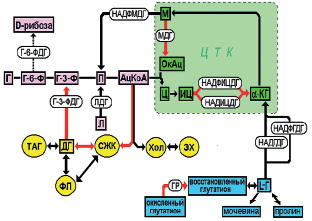
К числу наиболее информативно отражающих основные параметры внутриклеточного метаболизма лимфоцитов можно отнести несколько дегидрогеназ (рис. 3).
Глюкозо-6-фосфатдегидрогеназа (Г6ФДГ) – ключевой фермент пентозофосфатного пути (ПФП) и играет важную роль в метаболизме сахаров – от этого фермента зависит, подвергнется ли глюкоза гликолизу или будет утилизироваться в ПФП. Физиологическое значение последнего состоит в том, что в этом цикле, являющемся основным конкурентом гликолиза за глюкозо-6-фосфат образуются рибозо-5-фосфат и НАДФН, используемые в реакциях макромолекулярного синтеза: нуклеотидных коферментов, нуклеиновых кислот, жирных кислот, стероидов; кроме того НАДФН является кофактором для НАДФ-зависимых ферментов. Глюкозо-6-фосфатдегидрогеназа достаточно тесно взаимосвязана с ферментами антиоксидантной защиты и катаболизма ксенобиотиков (известно о кофакторной взаимосвязи между Г6ФДГ и глютатионредуктазой). Активность Г6ФДГ повышается в растущих и пролиферирующих клетках, как, например, в лимфоцитах при состоянии активации иммунной системы [55, 91, 101, 107, 172].
Рис. 3. Схема основных метаболических путей лимфоцитов
Глицерол-3-фосфатдегидрогеназа (Г3ФДГ), существует в двух формах – цитоплазматической и внутримитохондриальной. В цитоплазме НАД-зависимый фермент осуществляет взаимосвязь между системой липидного обмена и гликолизом через реакцию взаимообращения глицерол-3-фосфата и диоксиацетонфосфата. При взаимодействии НАД-зависимой Г3ФДГ и его внутримитохондриальной ФАД-зависимой формы осуществляется работа альфа-глицерофосфатного челночного механизма, обеспечивающего перенос водорода внутрь митохондрий; активность последнего зависит от наработки НАДФН в цитоплазме клеток и от окисления субстратов в митохондпиях. Отмечена активация ФАД-зависимой формы фермента под влиянием гормонов щитовидной железы и зависимость активности Г3ФДГ от уровня концентрации кортизола и инсулина в сыворотке крови [4, 16].
Лактатдегидрогеназа (ЛДГ) катализирует метаболизм лактата, регулируя тем самым внутриклеточное соотношение НАД/НАДФ. ЛДГ катализирует реакцию, находящуюся на разветвлении анаэробного и аэробного превращения пирувата. Большая часть этого НАД-зависимого фермента, существующего в пяти изоферментных формах, локализована в цитоплазматическом матриксе, меньшая – на мембранах митохондрий. В результате аэробной реакции ЛДГ (лактат-пируват), которая является одним из важных показателей обеспечиваемой гликолизом доли энергетического потенциала метаболизма в цитоплазме, нарабатывается основное количество НАДН. Важная роль гликолиза при состояниях функционального напряжения лимфоцитов (он выступает как «аварийный» механизм выработки АТФ в клетках), что подтверждается рядом авторов, установивших, например, его активацию при реакциях бласттрансформации лимфоцитов [4, 16].
Более продуктивным, чем гликолиз, с точки зрения выработки в клетках АТФ, является цикл трикарбоновых кислот (цикл Кребса). Характеристика реакций этого цикла может быть получена при исследовании показателей активности ферментов, катализирующих начальные (НАДИЦДГ и НАДФИЦДГ) и конечные (НАДМДГ и НАДФМДГ) его этапы. НАД- и НАДФ-зависимая изоцитратдегидрогеназы контролируют метаболизм изоцитрата в ЦТК, превращая его в α-кетоглутарат. Активность НАДИЦДГ отражает объем субстратного потока по циклу, который обеспечивает поддержание необходимой концентрации НАДН и энергетического потенциала митохондрий. При снижении интенсивности субстратного потока и недостатке водорода в митохондриях может включаться одна из дополнительных реакций цикла, регулируемая НАДФИЦДГ; которая катализирует приток в цикл субстрата из цитозоля клетки [4, 16, 58].
Два фермента функционируют на заключительном этапе ЦТК, они участвуют в реакциях метаболизма, образующегося в нем малата; это НАДМДГ и НАДФМДГ. Фермент НАДМДГ регулирует в цикле субстратный поток и влияет совместно с глутаматдегидрогеназами на окислительное фосфорилирование. Второй (НАДФМДГ или малик-фермент) контролирует одну из так называемых шунтирующих
реакций, активизирующихся при необходимости ускорения прохождения субстратов по метаболическим путям. В ходе этой реакции происходит превращение яблочной кислоты в пируват с восстановлением НАДФ+ до НАДФН, который затем используется в процессах синтеза. Как и другой уже упоминавшийся фермент – Г6ФДГ, участвующий в наработке НАДФН в клетке, НАДФМДГ имеет функциональные связи с внутриклеточными системами антиоксидантной защиты [4, 15, 16, 58].
Система глутаматдегидрогеназ осуществляет связь ЦТК с аминокислотным обменом, отражает перераспределение потоков субстратов между энергетическими и синтетическими реакциями внутриклеточного метаболизма. Процессы, контролируемые ферментами НАД- и НАДФ-зависимой глутаматдегидрогеназами (НАДГДГ и НАДФГДГ) относят к вспомогательным реакциям ЦТК, им принадлежит важная роль в регуляции его активности через изменения объемов субстратного потока. Определение активности этих ферментов в реакциях с использованием в качестве субстрата глутамата, позволяет оценить интенсивность поступления на ЦТК субстратов с аминокислотного обмена [4, 16].
Фермент глютатионредуктаза (ГР), который находится в прямой кофакторной связи с Г6ФДГ, участвует в двух важнейших внутриклеточных процессах: во-первых, обеспечивает превращение глутатиондисульфида в восстановленный глутатион, поддерживая тем самым функционирование глутатионовой системы антиоксидантной защиты клеток; во-вторых, участвует в активном транспорте в них аминокислот [16, 92, 93].
Таким образом, внутриклеточный метаболизм лимфоцитов регулируется широким набором ферментов и это обеспечивает возможность выполнения клетками многообразных специфических функций. Проявление ими функциональных возможностей в полном объеме лимфоцитов возможно лишь при соответствующем состоянии внутриклеточного обмена. Активность ферментов в лимфоцитах являются весьма чувствительными показателями их состояния, они используются для дифференциальной диагностики и разработки прогноза течения заболеваний.
На сегодняшний день изучена активность различных ферментов не только для суммарной популяции лимфоцитов периферической крови, но и отдельно для Т- и В-лимфоцитов. Две основные популяции
иммунной системы отличаются не только своими функциями, от полноценности которых зависит реализация иммунного ответа организма, но и метаболическими параметрами (Савченко А.А., 1989), что еще раз подтверждает зависимость функции от структуры [14].
Установлено, что при развитии реакции бласттрансформации лимфоцитов крови человека после их инкубации в течение 48–72 часов с фитогемагглютинином отмечается увеличение активности всех ферментов гликолиза и цикла Кребса, доказано влияние внутриклеточной концентрации аденозина и аденозиндифосфорной кислоты на экспрессию CD-антигенов на лимфоцитах крови [14].
При экспериментальной тимэктомии у крыс, сопровождающейся развитием иммунологической недостаточности, отмечено снижение активности митохондриальных форм липидзависимых шунтов – маликфермента, глицерол-3-фосфатдегидрогеназы, сопровождающееся увеличением содержания фосфатидилхолина, фосфатидилэтаноламина, сфингомиелина и снижением уровня кардиолипина в митохондриях печени [4, 16]
Петровым Р.В., Хаитовым Р.М. и Пинегиным Б.В., 1987, доказано, что причиной некоторых врожденных иммунодефицитных состояний являются генетически детерминированные дефекты ряда внутриклеточных ферментов. Известен иммунодефицит, развивающийся в результате недостаточной активности ферментов пуринового обмена, что приводит к избыточному накоплению АТФ в клетке, а это препятствует созреванию Т-лимфоцитов.
Доказано, что увеличение содержания АТФ в «метаболически здоровых» Т-лимфоцитах при инкубации с аденозином приводит к подавлению их Е-розеткообразующей функции [16].
Как известно, для развития вирусных инфекций характерно не только наличие выраженной реакции со стороны показателей иммунитета, но и изменения внутриклеточного метаболизма лимфоцитов. Так, например, при аденовирусной инфекции зарегистрировано повышение активности ЛДГ, в сочетании с повышением у больных числа Т-супрессоров. При обследовании лиц, часто и длительно болеющих вирусными респираторными заболеваниями, установлено повышение активности ферментов Г6ФДГ, Г3ФДГ, ЛДГ, НАДФГДГ, НАДФИЦДГ, НАДФМДГ в Т- и В-лимфоцитах. По мнению авторов, эти метаболические перестройки отражают уровень реагирования иммунной системы на развитие инфекции [16].
Исследования, проведенные у лиц с хронической герпесвирусной инфекцией, показали наличие снижения активности внутриклеточных ферментов Г3ФДГ, НАДГДГ, ЛДГ, МДГ и повышение активности НАДФМДГ и Г6ФДГ, что расценено как свидетельство угнетения функциональной активности иммунокомпетентных клеток [4, 16]. Предполагается, что активация последней происходит для обеспечения синтетических процессов при репликации вируса в клетке. Подобное повышение показателя ЛДГ установлено у больных с цитомегаловирусной инфекцией [16]. Повышенный уровень Г6ФДГ определяется функциональным напряжением адаптивных и защитных систем лимфоцитов, которое связано с переключением окислительных процессов на пентозофосфатный путь. Установлено, что у людей с врожденной ферментопатией по Г6ФДГ скорость реакции бласттрансформации лимфоцитов значительно замедлена, хотя розеткообразующая способность Т- и В-лимфоцитов повышена, у таких людей выявлена предрасположенность к инфекционным заболеваниям [4, 16].
Исследовались показатели внутриклеточного метаболизма нейтрофилов, лимфоцитов, эритроцитов и при вирусных гепатитах [16]. Эти показатели оказались наиболее информативными для характеристики тяжести и особенностей течения заболеваний. Например, А.В. Бахуташвили с соавторами в 1991 году отметили у больных острым вирусным гепатитом В нарушение метаболизма ц-АМФ в мононуклеарах периферической крови. При изучении внутриклеточного метаболизма лимфоцитов у больных острыми вирусными гепатитами А и В установлено, что наиболее значительные изменения ферментных показателей имеют место в разгар заболевания.
Киселев О.И. доказал, что именно глутатион способствует возникновению сигнального ответа клетки на гриппозную инфекцию [6].
Ферментный статус лимфоцитов исследован и при адаптационных реакциях человека в новых климато-географических условиях [4, 16]. Установлено, что в экстремальных экологических условиях Крайнего Севера увеличено потребление энергии, приводящее к снижению субстратного фонда НАД/Ф/-зависимых дегидрогеназ в лимфоцитах крови. Восполнение субстратных фондов энергетического обмена в клетках происходит за счет повышения аэробной реакции ЛДГ, увеличения использования продуктов катаболизма липидов и жирных кислот, снижения оттока субстратов на пентозофосфатный цикл. Булыгиным Г.В. в 1992 году доказано, что у коренных
жителей Заполярья, склонных к частым респираторным заболеваниям, отпределяется снижение активности Г6ФДГ и МДГ [4, 16]. У детей с низкой активностью дегидрогеназ и высокой активностью гидролаз наблюдается высокая подверженность инфекциям, однако такой энзиматический статус позволяет эффективнее приспособиться к экстремальным условиям среды за счет более быстрой мобилизации трофических ресурсов лимфоцитов [4, 16].
Реакция некоторых ферментов лимфоцитов на антигенные воздействия нередко одинакова, что объясняется не только их ролью в метаболизме (функционирование на одном метаболическом пути или путях, конкурирующих между собой за субстрат), но и общей внутриклеточной регуляцией [4, 16]. В связи с этим обнаруживается корреляционная зависимость между изменениями активности ферментов. Наиболее тесные связи наблюдаются среди митохондриальных ферментов; умеренная между ферментами глицерофосфатного шунта, а также цитоплазматическими ферментами, конкурирующими за пиридиннуклеотиды; более слабая связь отмечается между лизосомальными ферментами и дегидрогеназами. При этом, по мере утяжеления патологического процесса корреляционные зависимости между активностью отдельных ферментов увеличиваются [4, 16]. По мере нарастания интоксикации, возможно резкое снижение корреляционных связей, что связано, вероятнее всего, с нарушением внутриклеточной регуляции [4, 16].
Проявление в полном объеме функциональных возможностей лимфоцитов в процессах распознавания и формирования иммунного ответа происходит лишь при соответствующем состоянии внутриклеточного метаболизма. Последний, в значительной мере, обеспечивается определенным уровнем активности внутриклеточных ферментов. При врожденных или приобретенных ферментопатиях часто наблюдается не только поражение клеточного звена, но и развитие тяжелых комбинированных иммунодефицитов.
Таким образом, проведенный анализ изученной литературы российских и зарубежных авторов показал, что результаты исследований ферментов различных циклов внутриклеточного метаболизма лимфоцитов, подтверждение информативности этой группы показателей для характеристики иммунореактивности и резистентности организма и установления механизмов их нарушений позволяет рекомендовать энзиматические показатели в качестве параметров оценки и прогнозирования иммунологических изменений в организме.
На наш взгляд, проведение исследований активности ферментов, контролирующих реакции разных путей внутриклеточного обмена – цикла трикарбоновых кислот, пентозофосфатного цикла, гликолиза, необходимо для более полного объяснения патогенеза внебольничных пневмоний на фоне гриппа с целью подбора научно обоснованных схем терапии, прогнозирования результатов и контроля эффективности лечения.
Таким образом, на сегодняшний день не вызывает сомнения важная роль нарушений иммунной системы в развитии и течении внебольничной пневмонии на фоне гриппа. В связи с этим остается актуальным изучение иммунного статуса в зависимости от степени тяжести и в динамике заболевания, что может быть важным не только для оценки эффективности проводимых лечебных мероприятий, но и для прогноза течения внебольничной пневмонии.
Однако оценка иммунологического анализа не всегда позволяет объективно оценить функциональное состояние иммунной системы, что связано с вариабельностью иммунологических показателей, которые могут, не только качественно, но и количественно изменяться в разные стадии иммунологического ответа. Поэтому актуальным является определение функциональной активности иммунокомпетентных клеток по их структурно-метаболическим параметрам.
Установлено, что проявление в полном объеме функциональных возможностей ИКК в процессе формирования иммунного ответа происходит только при определенном состоянии внутриклеточного метаболизма, который в значительной мере обеспечивается определенным уровнем активности метаболических ферментов. Известно, что с первых минут развития иммунного ответа на проникновение в организм возбудителя изменяется энергетические и синтетические процессы, происходящие в лимфоците.
Однако до сих пор практически не анализировалась функциональная активность лимфоцитов в сопоставлении с иммунным статусом и продукцией цитокинов у больных с внебольничной пневмонией на фоне гриппа в зависимости от течения заболевания. На наш взгляд, проведение исследований активности ферментов, контролирующих реакции разных путей внутриклеточного обмена – цикла трикарбоновых кислот, пентозофосфатного цикла, гликолиза, необходимо для более полного объяснения иммунопатогенеза внебольничной пневмонии на фоне гриппа с целью прогнозирования течения заболевания.